Малоинвазивные технологии в лечении панкреатита
Острый панкреатит. Этиология, патогенез, классификация. Современные миниинвазивные методы лечения.
Острый панкреатит — заболевание поджелудочной железы, возникающее в результате аутолиза тканей поджелудочной железы липолитическими и активированными протеолитическими ферментами, проявляющееся широким спектром изменений — от отека до очагового или обширного жирового или геморрагического некроза. В большинстве случаев (около 75%) наблюдают незначительный аутолиз тканей, сопровождаемый только отеком поджелудочной железы и умеренными болями. В тяжелых случаях возникает жировой или геморрагический некроз ткани с тяжелыми метаболическими нарушениями, гипотензией, секвестрацией жидкости, полиорганной недостаточностью. После перенесенного острого панкреатита функции поджелудочной железы, как правило, приходят к норме. При хроническом панкреатите сохраняются остаточные явления с нарушением функций поджелудочной железы и периодическим обострением.
Этиология и патогенез
Существует более 40 причин развития острого панкреатита. Из них наиболее существенными являются 2 фактора: желчнокаменная болезнь и хронический алкоголизм, на долю которых приходится до 80-90% случаев всех причин возникновения острого панкреатита.
Другие факторы воспаления поджелудочной железы: наследственный панкреатит, стенозирующий папиллит, гиперкальциемия, гиперлипидемия, окклюзия верхней брыжеечной артерии и чревного ствола, портальная гипертензия, а также лекарственные повреждения (тиазидами, диуретиками, эстрогенами, азатиоприном, сульфонамидами, нитрофуранами).
Первые два этиологических фактора являются причиной аутолиза паренхимы поджелудочной железы, возникающего обычно на фоне гиперстимуляции экзокринной функции, частичной обтурации ампулы большого дуоденального сосочка, повышения давления в вирсунговом протоке, рефлюкса желчи в вирсунгов проток. Остро развивающаяся внутрипротоковая гипертензия вызывает повреждение и повышение проницаемости стенок терминальных протоков. Создаются условия для активизации энзимов, выхода их за пределы протоков, инфильтрации паренхимы и аутолиза ткани поджелудочной железы.
У больных желчнокаменной болезнью временное затруднение оттока желчи приводит к повышению давления и рефлюксу ее в панкреатический проток. Эти изменения связывают с миграцией мелких конкрементов или песка (микролитиазом). Благоприятное условие для желчной гипертензии — наличие общего канала (ампулы) для оттока желчи и панкреатического сока. В поддержку этой теории можно привести тот факт, что общий канал (ампула) по данным холангиографии у лиц, болевших панкреатитом, наблюдают почти в 90%, а у лиц с желчнокаменной болезнью, не имевших в анамнезе эпизодов панкреатита, — всего в 20-30% случаев.
Часто причина острого панкреатита — чрезмерное употребление алкоголя и прием жирной пищи. Известно, что алкоголь усиливает тонус и резистентность сфинктера Одди. Это может послужить причиной затруднения оттока экзокринного секрета поджелудочной железы и повышения давления в мелких протоках. Экспериментальными исследованиями доказано, что энтеральное введение алкоголя повышает давление в протоках поджелудочной железы и увеличивает проницаемость стенок мелких протоков для макромолекул панкреатического сока. Имеются сообщения, что крупные молекулы белка могут вызвать затруднение оттока панкреатического сока. Алкоголь усиливает секрецию желудочного сока и продукцию соляной кислоты, которая стимулирует продукцию секретина, вызывающего экзокринную гиперсекрецию поджелудочной железы, создает предпосылки для повышения давления в протоках. Таким образом, создаются условия для проникновения энзимов в паренхиму, активации протеолитических ферментов и аутолиза клеток поджелудочной железы.
В зависимости от причины внутрипротоковой гипертензии различают билиарный и алкогольный панкреатит. Эти разновидности панкреатита составляют 90% всех панкреатитов. Каждый из них имеет определенные особенности в клиническом течении и исходе болезни. К более редким причинам развития острого панкреатита относят открытые и закрытые травмы живота, интраоперационные повреждения ткани железы, атеросклеротическую окклюзию висцеральных ветвей абдоминального отдела аорты, портальную гипертензию, некоторые лекарственные препараты (глюкокортикоиды, эстрогенные контрацептивы и антибиотики тетрациклинового ряда).
Некроз панкреоцитов и клетчатки, окружающей дольки поджелудочной железы в самом начале процесса происходит под влиянием липазы. Липаза проникает внутрь клетки, гидролизует внутриклеточные триглицериды с образованием жирных кислот. В поврежденных клетках железы развивается внутриклеточный ацидоз со сдвигом рН до 3,5-4,5. В условиях ацидоза неактивный трипсиноген трансформируется в активный трипсин, который активирует фосфолипазу А, высвобождает и активирует лизосомальные ферменты (эластазу, коллагеназу, химотрипсин и др.). Содержание фосфолипазы А и лизолецитина в ткани поджелудочной железы при остром панкреатите существенно увеличивается. Это свидетельствует о ее роли в аутолизе ткани железы. Под воздействием липолитических, активированных протеолитических ферментов появляются микроскопические или макроскопически заметные очаги жирового некроза паренхимы поджелудочной железы. На этом фоне эластаза подвергает лизису стенки венул и междольковые соединительнотканные перегородки. В результате этого возникают обширные кровоизлияния, происходит трансформация жирового панкреонекроза в геморрагический. Таким образом, протеолитическая и липолитическая фазы развития острого деструктивного панкреатита взаимосвязаны друг с другом.
К очагам первичного некроза устремляются лейкоциты. Скопление лейкоцитов вокруг очагов некроза означает развитие защитной воспалительной реакции, сопровождаемой гиперемией и отеком. Для отграничения очагов некроза и элиминации некротической ткани макрофаги, лейкоциты, лимфоциты, клетки эндотелия выделяют провоспалительные (ИЛ-1, ИЛ-6, ИЛ-8) и антивоспалительные (ИЛ-4, ИЛ-10 и др.) ИЛ, активные кислородные радикалы. Небольшие очаги некроза в результате этой реакции отграничиваются, подвергаются лизису с последующей элиминацией продуктов распада. Эти процессы вызывают в организме умеренную местную реакцию на воспаление.
При обширном некрозе макрофаги, нейтрофилы, лимфоциты подвергаются избыточной стимуляции, продукция ИЛ и кислородных радикалов возрастает, выходит из-под контроля иммунной системы. Изменяется соотношение про- и антивоспалительных ИЛ. Они повреждают не только ткани железы, но и другие органы. Некроз тканей вызывают не столько сами ИЛ, сколько активные кислородные радикалы, NO и наиболее агрессивный пероксинитрил. ИЛ лишь подготавливают почву для этого: снижают тонус венозных капилляров, повышают их проницаемость, вызывают тромбоз капилляров. Изменения в микроциркуляторном русле вызываются преимущественно NO. Воспалительная реакция прогрессирует, зона некроза расширяется. Местная реакция на воспаление превращается в системную, развивается ССРВ. Тяжесть состояния больного коррелирует с высоким содержанием в крови ИЛ-6, ИЛ-8. При повышенной концентрации их в крови с высокой степенью вероятности можно прогнозировать полиорганную дисфункцию и недостаточность внутренних органов.
Изменения в микроциркуляторном русле приводят к перемещению значительной части жидкости организма в интерстициальное пространство. Происходит обезвоживание, снижается ОЦК, нарушаются водно-электролитный баланс и кислотно-основное состояние. На фоне повышенной концентрации ИЛ и гиперферментемии появляются очаги некроза на сальнике и брюшине. Выпот в брюшной полости содержит амилазу и другие энзимы поджелудочной железы в высокой концентрации. Токсичные продукты, циркулирующие в крови, оказывают прямое токсическое действие на сердце, почки, печень, ЦНС. Тяжесть синдрома системного ответа на воспаление возрастает в соответствии с нарастающей ишемией, увеличением концентрации NO, цитокинов, гипоксией и дистрофией в жизненно важных органах. Интоксикация в сочетании с гиповолемией быстро приводит к развитию шока. Возникают диссеминированное внутрисосудистое свертывание и полиорганная недостаточность.
В последующем (у некоторых пациентов с массивным панкреонекрозом) через 10-15 дней наступает фаза секвестрации и расплавления омертвевших участков. Секвестры и накопившаяся вблизи них жидкость могут некоторое время оставаться асептическими. Инфицирование и нагноение их с образованием парапанкреатических и забрюшинных абсцессов происходят в связи с транслокацией бактерий из просвета парализованного кишечника, возникающей в ответ на патологические изменения в поджелудочной железе и забрюшинной клетчатке. В позднем периоде в зоне некроза могут образовываться ложные кисты поджелудочной железы.
Классификация
По характеру изменений в поджелудочной железе выделяют:
• отечный, или интерстициальный, панкреатит;
Отечная, или абортивная, форма панкреатита развивается на фоне незначительного, микроскопического повреждения клеток поджелудочной железы. Фаза отека может в течение 1-2 дней превратиться в фазу некроза. При прогрессирующем панкреатите развивается жировой панкреонекроз, который по мере развития кровоизлияний превращается в геморрагический с образованием обширного отека в забрюшинной клетчатке и появлением геморрагического выпота в брюшной полости (панкреатогенный асептический перитонит). В ряде случаев наблюдают смешанные формы панкреатита: геморрагический панкреатит с очагами жирового некроза и жировой панкреонекроз с кровоизлияниями (рис. 14-2).
В зависимости от распространенности процесса различают очаговый, субтотальный и тотальный панкреонекроз.
По клиническому течению выделяют абортивное и прогрессирующее течение болезни. По фазам течения тяжелых форм острого панкреатита выделяют период гемодинамических нарушений — панкреатогенного шока, функциональной недостаточности (дисфункции) внутренних органов и период гнойных осложнений, наступающий через 10-15 дней.
Малоинвазивный метод — эндовидеохирургия/лапараскопия
1. Применение современных малоинвазивных технологий в различных комбинациях улучшает результаты лечения больных с острым деструктивным панкреатитом.
2. Эндовидеохирургические вмешательства являются операциями выбора при прогрессирующем ферментативном перитоните.
3. Использование пункционно-дренирующих операций с диагностической и лечебной целями оправдано в случаях формирования забрюшинных очагов деструкции при остром деструктивном панкреатите.
4. Малоинвазивные вмешательства при лечении больных с острым деструктивным панкреатитом в большинстве случаев являются эффективными и окончательными методами лечения. При необходимости они могут успешно дополнять традиционное лечение.
5. Пункционно-дренирующие операции являются самостоятельным и в большинстве случаев окончательным методом лечения псевдокист поджелудочной железы, в том числе и осложнённых. Традиционные оперативные вмешательства как операции резерва должны применяться только при неэффективности малоинвазивного лечения.
(РЕБРОВ Антон Александрович
МАЛОИНВАЗИВНЫЕ ВМЕШАТЕЛЬСТВА В ДИАГНОСТИКЕ И ЛЕЧЕНИИ ОСТРОГО ДЕСТРУКТИВНОГО ПАНКРЕАТИТА И ЕГО ОСЛОЖНЕНИЙ Санкт-Петербург 2007 автореферат)
Использованные источники:cyberpedia.su
Применение малоинвазивных технологий в лечении тяжелого острого панкреатита
В. А. Бомбизо, П. Н. Булдаков, А. Ю. Бердинских, А. В. Берестенников
КГБУЗ «Краевая клиническая больница скорой медицинской помощи» (г. Барнаул)
Цель: внедрение малоинвазивных технологий в работу хирургического стационара как наиболее результативных в лечении острого панкреатита. Материалы и методы.Проведено сравнительное изучение оперативных вмешательств у 390 пациентов с тяжелым острым панкреатитом в период с 2011 по 2013 год. Результаты.Более благоприятное течение у пациентов в группе оперированных малоинвазивными методами. Снижение среднего койко-дня на 14,2 дня. Применение малоинвазивных методик позволило снизить летальность.Выводы. Использование малоинвазивных технологий делает более достоверной диагностику при остром панкреатите, уменьшает количество традиционных вмешательств.
Ключевые слова: тяжелый острый панкреатит, панкреонекроз, лечение, малоинвазивные технологии.
Актуальность. Острый панкреатит, особенно его деструктивные формы, является тяжелым заболеванием органов брюшной полости, занимающим лидирующие позиции в клиниках неотложной хирургии [1, 2]. За острым панкреатитом прочно утвердилось третье место в структуре абдоминальной патологии — около 12,5 % [2]. Неуклонно растет количество деструктивных форм, и в настоящее время оно составляет до 5–10 % пациентов хирургического профиля. Отмечается старение пациентов с острым панкреатитом, в частности за последние 10 лет. Количество пациентов пожилого возраста (старше 70 лет) увеличилось на 30 % (данные авторов). Стабильно высокой остается летальность при тяжелом остром панкреатите — 20–45 %. При развитии инфекционных осложнений панкреонекроза летальность достигает 85 % [2, 3].
Одной из ключевых проблем является отсутствие точного алгоритма действий и единого подхода к лечению острого панкреатита на разных стадиях заболевания.
Цель исследования: разработка оптимального диагностического и лечебного подхода при остром панкреатите, позволяющего в кратчайшие сроки и с максимальной достоверностью определить тактический индивидуальный план ведения каждого пациента, внедрение малоинвазивных технологий в работу хирургического стационара как наиболее достоверных и результативных в лечении острого панкреатита.
Материалы и методы. В Краевой клинической больнице скорой медицинской помощи г. Барнаула в период с 2011 по 2013 год находились на лечении 390 пациентов с деструктивным панкреатитом (панкреонекрозом) (табл. 1).
Количество пациентов в Краевой клинической больнице скорой медицинской помощи
Использованные источники:www.medinfo22.ru
Источник
В настоящее время заболеваемость, инвалидизация и смертность от острого панкреатита и панкреонекроза занимает одно из ведущих мест среди острой хирургической патологии у лиц молодого возраста, преимущественно мужского пола. Одна из характерных черт последнего времени – заболевание отмечается у трудовостребованных лиц, что сопряжено с удовлетворительным материальным положением пациента и, вследствие этого, перееданием, злоупотреблением алкоголем и повышенной массой тела, что в свою очередь является пусковым механизмом заболевания и факторами, усложняющими все виды лечения и отягчающими прогноз заболевания. По литературным данным общая летальность от острого деструктивного панкреатита превышает 30%, а при развитии тяжелых форм осложнений достигает 100%.
По данным департамента здравоохранения Краснодарского края («Основные показатели здоровья и здравоохранения Краснодарского края за 6 месяцев 2005 года») демографическая ситуация в крае, как и в целом по РФ, остается сложной, вследствие нарастающей депопуляции населения. В общей структуре, смертность от болезней пищеварения увеличилась на 10,2 %. Рост общей смертности произошел за счет населения в трудоспособном и старше трудоспособного возрастах. Следует отметить рост смертности от болезней органов пищеварения в Краснодарском крае, превышает показатели по ЮФО в целом. Показатель выхода на инвалидность в крае в 2004 году увеличился в сравнении с 2002-2003 г.г. и составил 84,2 на 10 тыс. населения, превысив российский показатель на 11%. В структуре смертности по краю за 5 месяцев 2004-2005 г.г. от панкреатита умерло 274 пациента.
По данным медицинских учреждений, занимающихся проблемой деструктивного панкреатита, существенного прогресса и улучшения результатов лечения от повсеместного применения общепринятой тактики и методов хирургического лечения не наблюдается.
Считается, что основными элементами комплексного лечения острого панкреатита и панкреонекроза являются: интенсивная терапия и многочисленные открытые хирургические вмешательства на поджелудочной железе, забрюшинном пространстве и брюшной полости, в том числе, направленные на санацию гнойно-некротических очагов. Однако разрозненность в применении различных методик лечения этой крайне сложной хирургической патологии в клиниках края и отсутствие необходимого внимания со стороны руководителей учреждений здравоохранения обуславливают стабильность неутешительных показателей смертности и инвалидизации пациентов данной группы на протяжении последних десятилетий.
Более чем 13-летний опыт работы Российского центра функциональной хирургической гастроэнтерологии (ФГУ «РЦФХГ Росздрава»), на базе которого курировались тяжелейшие пациенты с острым деструктивным панкреатитом, панкреонекрозом, а так же литературные данные, свидетельствуют о необходимости внесения в базовые элементы комплексного лечения существенных дополнений, без которых невозможно преодолеть кризис в проблеме лечения этой патологии.
Наличие собственных научных фундаментальных, экспериментальных, клинических и практических разработок, квалифицированных врачебных кадров, способных выполнять весь спектр современных вмешательств на органах брюшной полости и забрюшинного пространства, проводить анестезиологическое пособие и интенсивную терапию, в сочетании с новейшими техническими достижениями инструментостроения, позволило ученым ФГУ «РЦФХГ Росздрава» сформировать новую функциональную единицу – «Инновационный Центр неотложной панкреатологии».
Центр по лечению неотложных состояний, связанных с патологией поджелудочной железы, является результатом сформировавшихся функциональных взаимодействий между клиническими и научными подразделениями ФГУ «РЦФХГ Росздрава», что обеспечивает постоянное обновление за счет непрерывного внедрения научных разработок и технических усовершенствований. Являясь структурной основой для применения современных медицинских технологий в лечении деструктивного панкреатита, инновационный центр аккумулирует основные инструменты визуализации и интраскопического манипулирования.
В основу панкреатологического центра положена измененная коренным образом идеология лечения деструктивного панкреатита, в основании которой следующие принципы:
Принцип минимальной инвазивности.
Основным хирургическим вмешательством является малоинвазивное (малотравматичное) хирургическое пособие под интраскопическим контролем (ультразвуковым, рентгенологическим, эндоскопическим).
Как известно, лапаротомия (вскрытие брюшной полости) и люмботомия (вскрытие забрюшиного прстранства) требовались для вскрытия гнойных очагов в поджелудочной железе и забрюшинной клетчатке, удаления некротизированных тканей и секвестров. Лапаротомия завершалась, обычно, формированием лапаростомы (швы на рану не накладывались, брюшная полость оставалась открытой), после чего обеспечивался отток воспалительного экссудата и панкреатического секрета, через лапаротомическую рану осуществлялся повторный доступ к железе для последующих секвестрэктомий (удаление некротезированных участков железы) и других санирующих процедур.
В настоящее время все эти задачи, возможно, решить, не прибегая к открытому вмешательству, а лапаротомия, люмботомия и лапаростомия перестают быть основой хирургии острого деструктивного панкреатита. Отказ от выполнения открытых вмешательств на органах брюшной полости и забрюшинного пространства и непосредственно на поджелудочной железе является основным психологическим барьером для всех хирургических учреждений, который потребовалось преодолеть. Именно сама лапаротомия, как тяжелейший травматический фактор на фоне имеющейся катастрофы и полиорганной недостаточности, многочисленные осложнения виде кишечных свищей и кровотечения от прямого открытого вмешательства на измененных тканях и органах, являются одними из основных причин неблагоприятного исхода.
Современный уровень развития медицинской техники (технологический прогресс) позволяет применять исключительно оборудование для закрытых вмешательств на всех органах. Возникающие в процессе малоинвазивного хирургического лечения кишечные, желчные, панкреатические свищи не требуют выполнения открытых хирургических вмешательств, а доступны консервативному лечению.
Таким образом, осуществляется перевод открытых вмешательств на брюшной полости и органах забрюшинного пространства при данной патологии из ранга основных во второстепенные.
Принцип опережения
Малоинвазивное хирургическое вмешательство с установкой дренажных систем в область преимущественного поражения поджелудочной железы осуществляется в максимально ранние сроки госпитализации, а не в фазу гнойных осложнений, как принято в большинстве лечебных учреждений.
Принцип обязательной панкреатической протоковой декомпрессии
Эндоскопические методы восстановления пассажа панкреатического сока в 12-перстную кишку (рассечение большого дуоденального сосочка, рассечение главного панкреатического протока, удаление камней из желчного протока) являются ключевыми факторами успешного лечения, поскольку без устранения протоковой гипертензии нет возможности прервать патологический процесс в поджелудочной железе или заживить панкреатические свищи.
Принцип индивидуальной курации
При панкреонекрозе нет одного (однократного) окончательного хирургического вмешательства, позволяющего излечить пациента. Хирургическая технология включает множественные этапные малоинвазивные вмешательства на выводных протоках поджелудочной железы, печени, на свободной брюшной полости, на забрюшинных некротических тканях и очагах гнойного поражения.
Принцип параллельности
Лечебные мероприятия проводятся в полном объеме с первых часов поступления пациента в стационар, не дожидаясь результатов от воздействия одного, отдельно взятого, из примененных методов (хирургической детоксикации, эфферентной детоксикации и т.д.).
Принцип каскадности
Малоинвазивные хирургические манипуляции выполняются непрерывно, окончание одной процедуры является стартом последующей.
Развитие постнекротических осложнений рассматривается как единый, неразрывный, идущий одновременно с изменениями в поджелудочной железе и окружающих тканях патологический процесс, а определяющей лечебную тактику особенностью течения острого деструктивного панкреатита является множественное протеолитическое поражение органов и токсическое поражение систем организма. Поэтому, основную часть времени пациент проводит в отделении интенсивной терапии, а в крайне тяжелых случаях – в реанимационном отделении, где с первых суток пребывания пациента применяют комплекс хирургических и терапевтических мероприятий:
Посиндромная коррекция сердечно-сосудистых, дыхательных нарушений (дыхательная аппаратура нового поколения — Пуритан, Пульмонетик и т.д.), лечение шока и полиорганной недостаточности.
Современные методики экстакорпоральной детоксикации (эфферентные методики – плазмоферез, плазмофильтрация, гемодиафильтрация, гемосорбция, ультрафильтрация).
Антибиотикотерапия выбора — последние поколения антибиотиков широкого спектра действия (карбопенемы, фторхинолоны (пефлоксацин) + антианаэробные препараты; цефалоспорины III–IV поколений + антианаэробные препараты), вплоть до получения результатов чувствительности микрофлоры.
Раннее полное парентеральное (внутривенное) питание до восстановления полноценного зондового питания и раннее энтеральное питание.
Отличительной особенностью нового подхода к интенсивной терапии является применение антибиотиков последних поколений с первых суток госпитализации и раннее питание пациентов. Замена дыхательной и следящей аппаратуры на самые современные устройства и применение всего спектра эфферентных методов детоксикации позволяют осуществлять функциональную поддержку на этапе полиорганной недостаточности.
При обращении пациента в первые часы заболевания, когда не представляется возможным однозначно оценить по какому «сценарию» в забрюшинном пространстве потечет заболевание у конкретного пациента и будет процесс ограниченным или распространенным, первичное хирургическое малоинвазивное вмешательство под ультразвуковым контролем (превентивное «мелкокалиберное» парапанкреатическое «дренирование») выполняется с целью хирургической детоксикации и профилактики гнойно-септических осложнений. При этом возможно введение лекарственных веществ через дренажные трубки, осуществление объективного контроля зоны патологических изменений по наличию и изменению характеристик экссудата. Посредством превентивных «мелкокалиберных» дренажей осуществляется первичный отток воспалительного экссудата.
В случае, когда заболевание у пациента при поступлении в центр уже достигло фазы гнойно-септических осложнений, то малоинвазивное оперативное вмешательство рассматривается как основной хирургический метод санации гнойно-некротических очагов.
Интраскопические хирургические технологии
При ультразвуковом исследовании выявляют скопления ферментативного выпота в брюшной полости, сальниковой сумке, забрюшинном пространстве и характерные для каждой формы поражения зоны пропитывания забрюшинной клетчатки.
В указанные области устанавливают дренажи диаметром 3 мм по принципу «не менее двух в один объект дренирования».
После фистулографии, на которой производится оценка характера распространения процесса в фазе некроза, под рентгенологическим контролем выполняют замену дренажей на двухпросветные большего диаметра. Данную процедуру необходимо повторять ежедневно, через день-два, в зависимости от конкретной клинической ситуации и состояния пациента. В конечном итоге, в зависимости от размера дренируемых полостей, дренажи могут достигать диаметра 5 – 20 мм.
В дальнейшем, при помощи видеоэндоскопа, выполняется чресфистульная санация забрюшинных некротических полостей, секвестральных «полей», с коррекцией и заменой дренажей. При этом удаляются некротизированные ткани и сформировавшиеся секвестры.
Чем больше количество «мелкокалиберных» (тонких – 1,5 – 3,3 мм диаметром) дренажей первично устанавливается в каждую область распространения экссудата и некроза, тем легче в дальнейшем выполнять санирующие процедуры, т.к. не всегда расположение трубки позволяет изменить ее направление или заменить «крупнокалиберной» (более широкой – 5 – 20 мм). К тому же, в случае возникновения свища полого органа от пролежня, один из дренажей можно удалить без ущерба для дренирования данной полости.
Применение видеофиброэндоскопа позволяет визуализировать пораженное забрюшинное пространство, поджелудочную железу и объективно оценить адекватность удаления некротизированных тканей с возможным проведением следующего двухпросветного «крупнокалиберного» дренажа в труднодоступный «карман», даже под острым углом к траектории первого «мелкокалиберного» дренажа.
По мере очищения полостей и уменьшения их размера, происходит обратный процесс замены дренажей на меньший диаметр и постепенное их удаление до закрытия свищевых ходов.
Одновременно с внедрением новых технологических приемов, требуется перестройка врачебного и сестринского ухода, изменение некоторых ключевых принципов формирования медицинского персонала и инструментального обеспечения:
Принцип высококвалифицированной врачебной универсальности.
Новые технологии лечения требуют проведения врачом практически ежедневных малоинвазивных хирургических вмешательств (основных хирургических вмешательств) по санации очагов некроза и нагноения под сочетанным сонографическим, эндоскопическим и рентгенологическим контролем в условиях рентгеноперационной под общей анестезией. Таким образом, врач, осуществляющий лечение деструктивного панкреатита по современным методикам, должен в совершенстве владеть несколькими специальностями – хирургия, интенсивная терапия, ультразвуковая диагностика, рентгенодиагностика, эндоскопия.
Иной подход – несколько специалистов, каждый из которых владеет только своей специальностью, не позволяет проводить лечение на требуемом современном уровне, сохранять преемственность этапов лечения и целостность понимания проблем пациента со скрытой от достоверной визуализации патологией забрюшинного пространства. Использование для решения поставленных задач одного универсального специалиста отвечает требованиям интенсивного технологического подхода к комплексному минимально инвазивному хирургическому лечению панкреонекроза.
Принцип манипуляционной иерархии.
Малоинвазивная технология лечения деструктивного панкреатита требует проведения ежечасных санационных хирургических манипуляций в палате интенсивной терапии (вспомогательных хирургических вмешательств). Данная хирургическая манипуляция основана на санации дренажных систем, установленных у пациента в очагах некроза и гнойного процесса. В промежутках времени между врачебными хирургическими вмешательствами проводится промывание, санация зон поражения, коррекция дренажных систем медицинским персоналом палаты.
Для этих целей требуется высокоспециализированный помощник врача. В его роли может выступать: медицинская сестра со специальным хирургическим образованием (в настоящее время формируется система получения средним медперсоналом высшего медицинского сестринского образования на базе медицинских ВУЗов); помощник врача (хирургическая сестра с высшим образованием; студент медицинского ВУЗа 3-6 курсов); младший врач (интерн, клинический ординатор, аспирант, врач на стажировке, врач со стажем до 3 лет). Особенностью хирургического ухода является контроль и проведение активных фракционных и постоянных дренажно-промывных и корригирующих процедур в течение 24 часов с минимальным перерывом 30-60 мин.
Принцип инструментальной аккумуляции.
Поскольку методики малоинвазивного лечения панкреонекроза требуют комбинации нескольких способов интраскопии, оснащение операционной и всего лечебного процесса должно отвечать современным стандартам. Основное инструментальное оборудование операционной для манипуляций под интраскопическим контролем включает хирургический ультразвуковой сканер, рентгентелевизионную установку и эндоскопическую стойку с системой жестких и гибких эндоскопов.
В комплекс средств визуализации требуемых технологией лечения панкреонекроза в обязательном порядке входят компьютерная или магнитнорезонансная томографии, как незаменимый этап диагностики некоторых зон некротического и гнойного поражения, не доступных сонографическим методикам.
Необходимым условием осуществления вышеуказанных принципов является изменение психологии врача для приобретения навыков малоинвазивных хирургических вмешательств на поджелудочной железе и забрюшинной клетчатке при панкреонекрозе под комбинированным интраскопическим контролем.
Объективным результатом работы новой функциональной единицы в ФГУ «РЦФХГ Росздрава» явилось неуклонное снижение летальности. В период превалирования открытых методов хирургического лечения панкреонекроза, при несущественной доле малоинвазивных технологий, летальность в этой группе пациентов была более 50%. При этом треть пациентов погибала в первые 10 суток после госпитализации от прогрессирующего циркуляторно-токсического шока, 28% больных погибали в сроки более 60 суток от аррозивного кровотечения. Остальными причинами летальности в основном были сепсис и синдром полиорганной недостаточности.
На этапе постепенного отказа от открытых операций летальность получила достаточно устойчивую тенденцию к снижению и, несмотря на «запущенность» поступающих в панкреатологический центр пациентов, колеблется от 4% до 8% в период 2003 — 2005 г.г.
Открытые оперативные вмешательства на брюшной полости и органах забрюшинного пространства остались на вооружении хирургов Центра только как средство борьбы с массивным аррозивным кровотечением, неподдающемся консервативным и ангиорентгенхирургическим методам гемостаза, или для выполнения коло- и илеостомии при острой кишечной непроходимости.
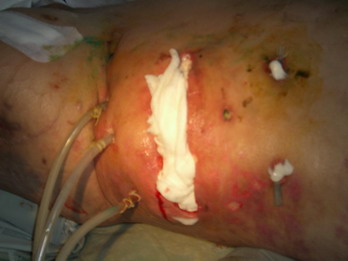
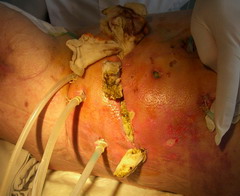
Лечение панкреонекроза
традиционным способом
Лечение панкреонекроза
малоинвазивными технологиями
Резюме
Преимущества комплексной малоинвазивной хирургической технологии лечения острого деструктивного панкреатита:
- Предотвращение развития панкреонекроза и гнойных осложнений при деструктивном панкреатите (абортивное течение острого панкреатита).
- Снижение летальности, причинами которой являются кровотечения, гнойно-септические осложнения, общая операционная травма.
- Уменьшение количества осложнений, связанных с интраоперационным кровотечением.
- Уменьшение количества вторичной внутрисекреторной недостаточности.
- Уменьшение инвалидизации пациентов.
- Хороший косметический эффект (отсутствуют лапаротомные и люмботомные рубцы, в том числе от ран, заживших вторичным натяжением, отсутствует необходимость в последующей пластике кожных ран и грыж).
Автор к.м.н. Новиков С.В.
Для получения более полной информации или очной консультации, с автором можно связаться по тел. +79851952791 или по электроной почте (medbaza23@mail.ru)
Источник