Современные принципы лечения острого панкреатита
За последнее десятилетие тактика ведения больных острым панкреатитом эволюционировала от агрессивной хирургической до консервативной выжидательной. Современный подход к лечению больных острым панкреатитом диктует необходимость привязки проводимой терапии к стадийным особенностям течения панкреатита с учетом данных динамического обследования — лабораторных анализов, УЗИ, КТ и пр.
Большинство больных поступает в клиники в фазе токсемии. Первоочередными лечебными задачами в этой стадии являются: антиферментная терапия, коррекция гиповолемии и микроциркуляторных нарушений, водноэлектролитных расстройств, профилактика функциональной недостаточности кишечника, профилактика септических осложнений.
В клиническую стадию образования инфильтратов на первое место выходит антибактериальная и противовоспалительная терапия.
В стадии гнойных осложнений наряду с консервативной антибактериальной терапией целесообразно использование хирургического лечения — малоинвазивных вмешательств под контролем УЗИ и КТ с целью пункционно-дренажного лечения гнойников, эндоскопической санации абсцессов, традиционных хирургических вмешательства для проведения санации и дренирования брюшной полости из лапаротомного доступа как «по требованию», так и программируемых.
Патогенетически обоснованной терапией у больных с деструктивным панкреатитом в фазу токсемии является антиферментная терапия. Максимальный лечебный эффект достигается при синергичном подавлении синтеза ферментов на уровне поджелудочной железы и выведении и инактивации уже циркулирующих в крови энзимов.
Подавление функции железы осуществляется путем создания ее физиологического покоя благодаря назогастральной интубации, локальной желудочной гипотермии, строгим ограничением приема пищи. Из фармакологических средств наиболее эффективны аналоги соматостатина (октреотид, сандостатин). Сандостатин — синтетический октапептид, является производным естественного гормона соматостатина. К основным его направлениям действиям относятся ингибирование базальной и стимулированной секреции поджелудочной железы, желудка, тонкой кишки, регуляция активности иммунной системы, выработки цитокинов, цитопротективный эффект. Обычный режим дозирования сандостатина 300-600 мкг/сут при трехкратном внутривенном или подкожном введении. Длительность терапии сандостатином обычно не привышает 4-7 су-ток и зависит от продолжительности фазы токсемии.
Не утратили своего значения цитостатики (5-фторурацил) и агонисты опиоатных рецепторов (даларгин), избирательно накапливающиеся в панкреатоцитах и угнетающие синтез проферментов. Близким по механизму действием обладает рибонуклеаза, разрушающая матричную РНК клеток, за счет чего поджелудочной железе предоставляется функциональный покой.
Одним из мощнейших способов блокады желудочной секреции является применение Н2-гистаминоблокоторов: фамотидина (квамател, гастросидин), ранитидина (зантак, ранигаст, ранисан) и блокаторов протонной помпы: омепразола (омез), рабепразола (париет). Ранитидин является блокатором Н2 гистаминовых рецепторов, подавляет базальную и стимулированную гистамином, гастрином, ацетилхолином, раздражением барорецепторов, пищевой нагрузкой секрецию соляной кислоты. Обычный режим дозировки при остром панкреатите не отличается от такового при язвенной болезни двенадцатиперстной кишки и составляет 300-450 мг в сутки при пероральном приеме. Фамотидин обладает сходным с ранитидином механизмом действия и большей продолжительностью антисекреторного эффекта. К главным достоинствам фамотидина относится отсутствие взаимодействия с системой цитохрома P-450 печени, благодаря чему он не оказывает влияния на метаболизм ряда лекарственных препаратов и не вызывает их кумуляции. Кроме того, фамотидин также не усиливает секреции пролактина и не вызывает антиандрогенного эффекта, не взаимодействует с алкогольной дегидрогеназой печени. При остром панкреатите возможен однократный прием препарата 40 мг/сут.
Омепразол и рабепразол являются производными бензимидазола и оказывают антисекреторное действие за счет ингибирования К+/HЧ-АТФазы (протонного насоса) париетальных клеток слизистой оболочки желудка. Препараты снижают базальную и стимулированную желудочную секрецию независимо от природы раздражителя. Их клиническая эффективность — самая высокая среди противоязвенных средств. Омепразол обладает высокой липофильностью, легко проникает в париетальные клетки слизистой оболочки желудка, где накапливается и активируется при кислом значении pH. У рабепразола, по сравнению с омепразолом, более короткая длительность действия. In vitro рабепразол по антисекреторной активности в 2-10 раз превосходит омепразол. Особенностью рабепразола является отсутствие побочных эффектов со стороны ЦНС, сердечно-сосудистой и дыхательной системы. При остром панкреатите суточная доза препаратов составляет для омепразола 40 мг, а для рабепразола 20 мг.
Инактивация циркулирующих ферментов производится с помощью внутривенного введения антиферментных препаратов — апротинина (гордокс, ингитрил, контрикал, трасилол). Свойством апротинина является инактивация важнейших протеиназ (плазмин, кининогеназы, трипсин, химотрипсин) плазмы, клеток крови и тканей, образование с ними стойких нейтральных комплексов, что позволяет быстро вывести больного из шока и токсемии. Апротинин влияет на каталитическое взаимодействие между различными факторами свертывания и фибринолизом, а также на процесс свертывания крови, что существенно в терапии расстройств микроциркуляции при остром панкреатите. Суточная доза составляет не менее 1 млн. КИЕ препарата.
Немаловажным является выведение уже циркулирующих в кровеносном русле ферментов из организма. Это достигается внутривенным форсированным диурезом, в тяжелых случаях — плазмосорбцией, гемосорбцией, плазмаферезом, перитонеальным диализом.
Одним из патофизиологических механизмов усиления интоксикации при остром панкреатите является включение и самоподдержание механизма функциональной недостаточности кишечника. Усугублению тяжести водно-электролитных расстройств способствуют потери жидкости и солей при рвоте. Порочный круг патофизиологических механизмов, включающий рефлекторное нарушение моторики, угнетение всасывания и эвакуации и последующие метаболические расстройства требует терапии, корригирующей данные расстройства и предупреждающей их. Основными средствами, регулирующими моторику ЖКТ, применяемыми с этой целью являются антагонисты дофаминовых рецепторов: домперидон (мотилиум), метоклопрамид (перинорм, реглан, церукал), спазмолитики. Механизм действия метоклопрамида обусловлен блокадой дофаминовых рецепторов и повышением порога возбудимости хеморецепторов триггерной зоны. Таким образом, препарат способствует уменьшению тошноты, рвоты, стимулирует опорожнение желудка и перистальтику кишечника. Метоклопрамид используется для внутримышечного и внутривенного введения в суточной дозе не превышающей 30 мг. Домперидон (мотилиум) блокирует преимущественно периферические и, в меньшей степени, центральные дофаминовые рецепторы, оказывая сходное с метоклопрамидом действие, однако более эффективен. Он плохо проникает через гемато-энцефалический барьер, однако у него имеется противорвотное действие, обусловлен-ное нормализацией тонуса и моторики ЖКТ. Применяется перорально, до 40 мг/сут
Наиболее распространенный спазмолитик, традиционном применяемый в хирургической практике — дротаверин (ношпа, беспа, веро-дротаверин и т.д.). Данный препарат является спазмолитиком миотропного действия. Основным его свойством является понижение тонуса гладкой мускулатуры внутренних органов, снижение ее двигательной активности, что способствует нормализации моторики ЖКТ в сочетании с другими препаратами, оказывает обезболивающий эффект. По сравнению с папаверином, дротаверин обладает более продолжительным действием, не оказывает влияние на вегетативную нервную систему и ЦНС. Обычный режим дозирования препарата — 40-80 мг 1-3 раза в сутки внутримышечно или внутривенно. При тяжелой неукротимой рвоте возможно применение в малых дозах седативного нейролептика хлорпромазина (аминазина). Однако, существуют ограничения его применения в хирургической практике, такие как ЖКБ, МКБ, обострение эрозивно-язвенных заболеваний ЖКТ. С другой стороны, учитывая наиболее распространенную этиологическую причину панкреонекрозов в нашей стране, седативное и небольшое антипсихотическое действие аминазина востребовано при алкогольных психозах, нередко дополняющих клиническую картину заболевания.
Одной из причин стресса и, как следствие, шока является боль. Купирование боли в терапии панкреонекроза является не только гуманным по отношению к больному актом, но и профилактикой расстройств кровообращения. Ощущение боли приводит к рефлекторной активации симпатической нервной системы и, как следствию, спазму сосудов. Регионарное и системное ухудшение трофики тканей, централизация кровообращения за счет гиповолемии и нарушения микроциркуляции усугубляют общую клиническую картину, вызванную токсемией.
Наиболее целесообразным является комбинация внутривенного способа восполнения дефицита ОЦК, обеспечивающего быструю коррекцию водно-электролитных расстройств путем введения полиионных сред и плазмозаменителей, с последующей внутриартериальной водной нагрузкой, обеспечивающей вывод токсинов. С целью обезболивания традиционно применяются как неопиоидные, так и опиоидные аналгетики. Из неопиоидных наиболее широкое применение нашли производные пирролизинкарбоксиловой кислоты: кеторолака трометамин (кетанов, кеторол), дериваты пропионовой кислоты: кетопрофен (кетонал, флексен), а также метамизол (анальгин). Среди опиоидных анальгетиков со смешанным механизмом действия часто применяется трамадол (маброн, трамал). Анальгезирующие эффекты НПВС (кетопрофен, кеторолак) обусловлены двумя механизмами — периферическим, через подавление синтеза простагландинов и кининогенов и центральным, через ингибирование синтеза простагландинов и субстанции Р в центральной и периферической нервной системе. Кетопрофен, кроме того, ингибируют липоксигеназу и стабилизирует лизосомальные мембраны. Суточные дозы для препаратов НПВС при двух и трехкратном внутримышечном введении составляют до 300-400 мг. Метамизол натрия является производным пиразолона. Обладая достаточно слабым по сравнению с вышеперечисленными препаратами обезболивающим эффектом, метамизол успешно применяется как базовая обезболивающая терапия. Совместное использование метамизола с другими препаратами из группы НПВС усиливает его токсические эффекты, а применение совместно с опиоидными аналгетиками (например трамадолом), усиливает и пролонгирует обезболивающее действие. Таким образом, противовоспалительные эффекты препаратов этой группы, наряду с обезболивающим действием, являются основанием для их назначения в клиническую стадию образования инфильтратов в комплексе с антибактериальными средствами.
Трамадол является производным циклогексанона. В основе его механизма действия лежит взаимодействие с тормозными опиатными рецепторами в ЦНС. Трамадол используется в терапии сильных и умеренных болевых синдромов. Из его побочных действий при лечении панкреонекрозов значимы тошнота и рвота, что может ограничивать применение препарата. Обычно трамадол вводится внутримышечно трехратно 150-200мг/сут.
Эффективно дополняют традиционное обезболивание такие лечебные манипуляции, как внутривенное вливание глюкозо-новокаиновой смеси, паранефральная новокаиновая блокада, эпидуральная блокада.
На любой стадии заболевания при проявляющихся признаках билиарной гипертензии или в случае острого холецистита, выраженном увеличении головки поджелудочной железы целесообразно дополнение консервативной схемы лечения дренированием желчного пузыря или его пункцией (эндоскопические методы, манипуляции под контролем ультразвука). Для обеспечения оттока панкреатического секрета в случае необходимости производится эндоскопическая папиллосфинктеротомия, извлечение ущемленного конкремента, аспирация панкреатического сока, что позволяет осуществить декомпрессию протоковой системы и уменьшить поступление ферментов в кровь и лимфу.
Одной из наиболее важных задач в лечении панкреонекроза является профилактика развития гнойных осложнений. Целесообразно использовать антибактериальные препараты уже на ранних этапах лечения. Спектр действия антибиотиков должен включать грамотрицательные и грамположительные аэробные и анаэробные микроорганизмы.
Среди современных антибактериальных препаратов в зависимости от пенетрирующей способности в ткани поджелудочной железы выделяют 3 группы: 1 — препараты, концентрация которых в ткани поджелудочной железы не достигает минимальной подавляющей концентрации (МПК) для большинства бактерий (аминогликозиды, аминопенициллины, цефалоспорины I поколения). 2 группа — концентрация препаратов после внутривенного введения превышает МПК для некоторых, но не всех встречающихся при панкреатической инфекции микроорганизмов (защищенные пенициллины широкого спектра — тазобактам + клавуланат; цефалоспорины III поколения). 3 группа — антибактериальные препараты, концентрации которых в тканях поджелудочной железы превышают МПК для большинства микроорганизмов, являющихся возбудителями панкреатогенной инфекции (фторхинолоны — ципрофлоксацин, офлоксацин, пефлоксацин и карбапенемы — меропенем, имипенем).
В качестве компонента комбинированной антибактериальной терапии может быть использован метронидазол, также достигающий бактерицидной концентрации в тканях поджелудочной железы для анаэробных возбудителей.
Наиболее распространенная схема выбора антибактериальной терапии включает внутривенное применение пефлоксацина (абактал) 800-1200 мг/сут и метронидазола (метрогил) 1000 мг/сут при 2х-3х разовом режиме введения. В дальнейшем антибактериальная терапия корригируется с учетом результатов посева и определения чувствительности к антибиотикам патогенной микрофлоры.
Среди гнойный осложнений панкреонекроза наиболее частыми являются постнекротические псевдокисты поджелудочной железы и флегмоны забрюшинной клетчатки, формирующиеся в сроки от 2 до 3 недель от момента заболевания за счет ауто-инфекции или вторичного инфицирования после хирургических вмешательств. Наряду с хирургическим лечением (традиционные санационные мероприятия «по требованию» или программируемые, миниинвазивные эндоскопические вмешательства, пункции гнойников под контролем УЗИ и КТ), целесообразна комбинированная антибиотикотерапия со сменой препаратов в сочетании с метронидазолом и деконтаминацией кишечника. Наиболее эффективным традиционно считается регионарное введение лекарственных препаратов в аорту или чревный ствол, что позволяет создать оптимальную концентрацию препарата в очаге повреждения.
Применение современных антиферментных, антисекреторных препаратов с учетом стадийности заболевания, совершенствующиеся методы диагностики и детоксикации, своевременная профилактика гнойных осложнений панкреонекрозов позволяют улучшить результаты лечения больных деструктивным панкреатитом, сократить пребывание больных в стационаре, уменьшить частоту инвазивных методов лечения, снизить летальность.
Список литературы:
1. Бондаренко И.М. Влияние сандостатина на внешнесекреторную функцию желудка, печени и поджелудочной железы.// Рос. журнал гастроэнтерол. гепатол.колопроктол.-1995,т.5, №3, прилож.№ 1, с.36
2. Вашетко Р.В., Толстой А.Д., Курыгин А.А., Стойко Ю.М., Краснорогов В.П. Острый панкреатит и травмы поджелудочной железы: руководство для врачей.- Спб.:издательство «Питер», 2000, с.320
3. Гельфанд Б.Р., Бурневич С.З., Брюхов А.Н., Бражник Т.Б. Селективная деконтаминация желудочно-кишечного тракта в интенсивной терапии у больных хирургического профиля// Consilium medicum, 2002, №1, c.14-18
4. Дубров Э.Я. Акилин К.А., Алексеечкина О.А. Ультразвуковая диагностика и показания к малоинвазивным вмешательствам при панреонекрозе. Роль и место малоинвазивных вмешательств при лечении острого панкреатита /Материалы городского семинара. Том 162. М: НИИ скорой помощи им. Н.В. Склифосовского , 2003,с 38-40.
5. Костырной А.В. Современные подходы к консервативному лечению гнойно-некротических осложнений острого панкреатита// Клиническая хирургия , 2000, №8, с.8-10
6. Савельев В.С., Гельфанд Б.Р., Филимонов М.И., Бурневич С.З., Орлов Б.Б. Цыденжанов Е.Ц. Оптимизация лечения панкреонекроза: роль активной хирургической тактики и рациональной антибактериальной терапии// Анналы хирургии — 2000, № 2, с 12-16.
7. Слабожанкин А.Д., Гольцов В.Р., Назаров В.Е. Применение кваматела при лечении острого панкреатита на ранней стадии заболевания . Актуальные вопросы диагностики и лечения в многопрофильном лечебном учреждении /V Всерос-сийская научно-практическая конференция. Тезисы докладов. — СПб., 2001. — с.244-245.
8. Саенко В.Ф., Ломоносов С.П., Зубков В.И. Антибактериальная терапия больных с инфицированным некротическим панкреатитом // Клин.хирургия, 2002, №8, с.5-8
9. Bassi C., Falconi M., Talomini F. Controlled clinical trial of pefloxacin versus. Imipenem in sever acute pancreatitis.// Gastroenterology. — 1998. — V.115. — p1513-1517.
10. Buchler M.W., Malferstheiner P. Acute pancreatitis: Novel concepts in biology and therapy.-Berlin; Vienna: Blackwell Wissen-Schafts-Verlag, 1999.-548 р.
11. Gullo L. Somatostatin analogues and exocrine pancreatic secretion.// Digestion — 1996, Vol. 57, suppl. 1, P. 14-19
12. Kramer K.M., Wevy H. Prophylactic antibiotics for severe acute pancreatitis: the beginning of an era. // Pharmacotherapy — 1999, N 19, P. 592-602
13. Wyncoll D.W. The management of severe acute necrotizing: an evidence-based review of the literature.//Intensive Care Med.,1999, vol.25,№2, P146-56
14. Widdison A.L., Haranjia N.D. Pancreatic infection complicating acute pancreatitis.// Br. I. Surg. — 1993, N 50, P. 148-154
Источник
Лечебная тактика
при остром панкреатите.
Больные с подозрением на
острый панкреатит должны быть в
экстренном порядке
госпитализированы в
хирургический стационар.
Пациенты с деструктивной формой острого
панкреатита нуждаются в лечении в
условиях реанимационного отделения.
Основными задачами лечения острого
панкреатита являются:
1. Подавление аутоферментной агрессии
и воспалительного процесса в ткани
поджелудочной железы.
2. Предупреждение и лечение панкреатогенной
токсемии, осложнений и нарушений всех
видов обмена.
3. Профилактика и лечение перитонита и
парапанкреатита.
4. Предупреждение и лечение постнекротических
осложнений.
Основные
направления и методы комплексной терапии
деструктивного панкреатита включают:
1.Интенсивную
корригирующую терапию
(поддержание оптимального уровня
доставки кислорода с помощью инфузионной,
кардиотонической и респираторной
терапии).
2.Методы
экстракорпоральной детоксикации
(гемо- и
лимфосорбция, гемо- и плазмофильтрация,
плазмаферез) и энтеросорбции. Однако,
в настоящее время алгоритм экстракорпоральной
и энтеральной детоксикации окончательно
не разработан, что требует проведения
дальнейших доказательных исследований.
3.
Блокаду секреторной функции ПЖ и
медиатоза.
С этой целью в первую очередь целесообразно
применение препаратов соматостатина/октреотида.
При отсутствии этих средств возможно
использование антиметаболитов
(5-фторурацил). Отсутствие доказательных
данных об эффективности ингибиторов
протеаз при
панкреонекрозе не позволяет рекомендовать
в настоящее время их дальнейшее
клиническое применение.
4.Антибактериальная
профилактика и терапия.
Данные
микробиологических исследований
являются основой выбора антибактериальных
препаратов при панкреонекрозе, спектр
действия которых должен охватывать
грамотрицательные и грамположительные
аэробные и анаэробные микроорганизмы
— возбудителей
панкреатогенной инфекции. Это соответствует
выбору эмпирического режима
антибактериальной профилактики и
терапии при панкреонекрозе.
Важнейшей
детерминантой эффективности действия
антибиотиков является их способность
селективно проникать в ткани ПЖ через
гемато-панкреатический барьер.
В зависимости от
различной пенетрирующей способности
в ткани ПЖ выделяют три группы
антибактериальных препаратов:
Группа
I.
Концентрация аминогликозидов,
аминопенициллинов и цефалоспоринов
первого поколения после внутривенного
введения не достигает в тканях
поджелудочной железы минимальной
подавляющей концентрации (МПК) для
большинства бактерий.
Группа
II
представлена антибактериальными
препаратами, концентрация которых после
внутривенного введения превышает МПК,
которая эффективна для подавления
жизнедеятельности некоторых, но не всех
часто встречающихся при панкреатической
инфекции микроорганизмов
— защищенные
пенициллины широкого спектра:
пиперациллин/тазобактам и
тикарциллин/клавуланат; цефалоспорины
III поколения:
цефоперазон и цефотаксим; цефалоспорины
IV поколения
(цефепим).
III
группу
составляют фторхинолоны (пипрофлоксацин,
офлоксацин и особенно пефлоксацин) и
карбапенемы (меропенем, имипенем/циластатин),
которые создают максимальные концентрации
в панкреатических тканях, превышающие
МПК, для большинства возбудителей
инфекции при панкреонекрозе. Метронидазол
также достигает бактерицидной концетрации
в тканях ПЖ для анаэробных бактерий,
поэтому может быть использован как
компонент комбинированной антибактериальной
терапии (цефалоспорин
+ метронидазол).
• При
отечном панкреатите антибактериальная
профилактика не показана.
• Диагноз
панкреонекроза является абсолютным
показанием к назначению антибактериальных
препаратов (группа
II и
III), создающих
эффективную бактерицидную концентрацию
в зоне поражения со спектром действия
относительно всех этиологически значимых
возбудителей.
• Дифференцировать
сразу цель назначения антибиотиков при
панкреонекрозе
-профилактическую
или лечебную
— во многих
случаях крайне сложно, учитывая высокий
риск инфицирования некротической ПЖ и
сложности его документации
клинико-лабораторными и инструментальными
методами в реальном режиме времени.
• Развитие
при панкреонекрозе нередко фатального
сепсиса требует немедленного назначения
антибактериальных средств с максимальным
эффектом и минимальным побочным
действием.
• Фактор
эффективности должен доминировать по
отношению к фактору
стоимости.
Препаратами выбора
как для профилактического, так и лечебного
применения являются:
• карбапенемы,
• фторхинолоны
(особенно пефлоксацин)+метронидазол,
• цефалоспорины
Ш-ГУ поколения+метронидазол,
• защищенные
пенициллины (пиперациллин/тазобактам,
тикарциллин/клавуланат).
Принимая
во внимание роль интестиногенной
транслокации бактерий в патогенезе
инфекционных осложнений панкреонекроза,
в схему антимикробной терапии целесообразно
включение режима селективной деконтаминации
кишечника (в частности, пероральное
введение фторхинолонов (пефлоксацин,
ципрофлоксацин)).
Панкреонекроз
является фактором риска развития
грибковой суперинфекции, что определяет
целесообразность включения антифунгальных
средств (флуконазол) в программу лечения
больных панкреонекрозом.
Продолжительность
антибактериальной терапии при
панкреонекрозе определяется сроками
полного регресса симптомов системной
воспалительной реакции.
Учитывая
динамику патологического процесса при
панкреонекрозе от стерильного к
инфицированному и часто многоэтапный
характер оперативных вмешательств для
эффективной антибактериальной терапии
следует предусмотреть возможность
смены нескольких режимов.
5.
Нутритивная поддержка при остром
панкреатите
Нутритивная
поддержка показана при тяжести состояния
больного панкреатитом по шкале Ranson
>2 баллов, по шкале АРАСНЕ
II > 9
баллов, при верификации клинического
диагноза панкреонекроза и/или наличие
полиорганной недостаточности. При
верификации отечной формы панкреатита
и наличие положительной динамики в его
комплексном лечении в течение
48-72 часа,
через
5-7 дней
показано естественное питание.
Эффективность
полного парентерального питания при
панкреонекрозе сомнительна. Это
объясняется следующими отрицательными
эффектами полного парентерального
питания: усиление энтерогенной
транслокации бактерий, развитие
ангиогенной инфекции, имун-носупрессии
и высокой стоимости метода. В этой связи,
на сегодняшний день, более целесообразным
и эффективным при панкреонекрозе считют
проведение энтерального питания в
ранние сроки заболевания через
назоеюнальный зонд установленный
дистальнее связки Трейца эндоскопическим
путем или во время операции. В случае
развития толерантности к энтеральному
питанию (увеличение уровней амилаз- и
липаземии, стойкий парез кишечника,
диарея, аспирация), у больных панкреонекрозом
показано проведение тотального
парентерального питания.
Хирургическое
лечение панкреонекроза.
В
отношении принципов дифференцированного
хирургического лечения панкреонекроза
и его септических осложнений имеются
принципиальные различия. Они касаются
оптимальных сроков и режимов оперативного
вмешательства, доступов, видов операций
на ПЖ, желчевыводящей системе, методов
дренирующих операций забрюшинного
пространства и брюшной полости.
Показанием к
операции при панкреонекрозе является:
• Инфицированный
панкреонекроз и/или панкреатогенный
абсцесс, септическая флегмона забрюшинной
клетчатки, гнойный перитонит независимо
от степени полиорганных нарушений.
• Стойкая
или прогрессирующая полиорганная
недостаточность, независимо от факта
инфицирования, несмотря на комплексную
интенсивную консервативную терапию в
течение
1-3 суток,
что свидетельствует об обширном некрозе
ПЖ и забрюшинной клетчатки или высоком
риске развития панкреатогенной инфекции.
• Оперативное
лечение показано больным, у которых по
данным КТ-ангиографии масштаб некроза
превышает
50% паренхимы
ПЖ и/или диагностировано распространение
некроза на забрюшинное пространство,
что соответствует высокому риску
инфицирования и фатальных системных
осложнений.
• Панкреатогенный
(ферментативный, абактериальный)
перитонит является показанием к
лапароскопической санации и дренированию
брюшной полости.
Факт
инфицирования некротических тканей
является важным, но не единственным
показанием к операции, особенно в ранние
сроки заболевания.
Большую
роль в объективизации показаний к
операции играет использование интегральных
шкал оценки тяжести состояния больного
с деструктивным панкреатитом.
Методы
хирургического лечения широко варьируют,
что определяется динамикой
патоморфологического процесса в ПЖ,
забрюшинной клетчатке и брюшной полости.
Техническое решение этапа некрсеквестрэктомии
однотипно, поэтому особое значение
необходимо придавать выбору метода
дренирующих операций в забрюшинном
пространстве, так как избранный уже на
первой операции метод дренирования
существенно определяет выбор режима
оперативной тактики.
В
настоящее время используют три основных
метода
дренирующих операций
при панкреонекрозе, которые обеспечивают
различные условия для дренирования
забрюшинного пространства и брюшной
полости в зависимости от масштаба и
характера поражения ПЖ, забрюшинной
клетчатки и брюшной полости.
Предлагаемые
методы дренирующих операций включают
определенные технические способы
наружного дренирования различных
отделов забрюшинной клетчатки и брюшной
полости, что обязательно предполагает
выбор определенных тактических
режимов повторных вмешательств:
• программируемых
ревизий и санаций всех зон некротической
деструкции и инфицирования в различных
отделах забрюшинного пространства («по
программе»)
• неотложных
и вынужденных повторных вмешательств
(«по требованию») вследствие
имеющихся и/или развившихся осложнений
(продолжающаяся секвестрация, неадекватное
дренирование, кровотечение и т.д.) в
динамике патоморфологической трансформации
зон некроза/инфекции в забрюшинном
пространстве и брюшной полости.
Методы
дренирующих операций забрюшинного
пространства при панкреонекрозе
классифицируют следующим образом:
• «Закрытый»
• «Открытый»
• «Полуоткрытый»
I.
«Закрытый»
метод дренирующих операций
включает активное дренирование
забрюшинной клетчатки и брюшной полости
в условиях анатомической целостности
полости сальниковой сумки и брюшной
полости. Это достигается имплантацией
многоканальных,
силиконовых дренажных конструкций для
введения антисептических растворов
фракционно или калельно в очаг деструкции
(инфекции) с постоянной активной
аспирацией. «Закрытый» метод
дренирования предполагает выполнение
повторных вмешательств только «по
требованию». Контроль за очагом
деструкции/инфекции и функцией дренажей
осуществляется по результатам УЗИ, КТ,
видеооптической техники, фистулографии.
Целесообразно
применение методов лапароскопической
«закрытой» бурсооментоскопии и
санации сальниковой сумки. С использованием
лапароскопической техники выполняют
лапароскопию, декомпрессию желчного
пузыря, санацию и дренирование брюшной
полости, и далее с использованием
специально разработанного инструментария
из мини-лапаротомного доступа осуществляют
осмотр ПЖ, некрсеквестрэктомию в полном
объеме и формируют панкреатооментобурсостостому.
Начиная с
3-5 дня после
операции, с интервалом
1-3 суток
выполняют этапную санацию. В межоперативном
периоде проводят лаваж полости сальниковой
сумки.
Применяют
методы эндоскопического дренирования
и санации забрюшинного пространства
через поясничный внебрюшинный доступы.
Все большее распространение получают
малоинвазивные хирургические методы
чрескожного пункционного дренирования
парапанкреатической зоны и других
отделов забрюшинной клетчатки, желчного
пузыря под контролем УЗИ и КТ. Малоинвазивные
вмешательства легко выполнимы,
малотравматичны и эффективны при
обоснованном показании и соблюдении
методологии. При неэффективности
вышеперечисленных методов дренирования
при панкреонекрозе показана лапаротомия.
Основными
показаниями к «открытому» и
«полуоткрытому» методу дренирования
забрюшинного пространства являются:
• крупномасштабные
формы панкреонекроза в сочетании с
поражением забрюшиннойой клетчатки;
• инфицированный
панкреонекроз и панкреатогенный абсцесс
в сочетании с крупноочаговыми формами
инфицированного панкреонекроза;
• релапаротомия
после неэффективного «закрытого»
или «полуоткрытого» методов
дренирования.
II.
«Открытый» метод дренирующих
операций
при панкреонекрозе предполагает
выполнение программируемых ревизий и
санаций забрюшинного пространства и
имеет два основных варианта технических
решений, определяемых преимущественным
масштабом и характером поражения
забрюшинного пространства и брюшной
полости. Этот метод включает:
• панкреатооментобурсостомию+люмботомию
(рис. 13, 14);
• панкреатооментобурсостомию
+лапаростомию.
Показанием
к панкреатооментобурсостомии+люмботомии
является инфицированный и стерильный
распространенный панкреонекроз в
сочетании с поражением парапанкреатической,
параколической и тазовой клетчатки.
Панкреатооментобурсостому формируют
путем подшивания фрагментов
желудочно-ободочной связки к париетальной
брюшине в верхней трети лапаротомной
раны по типу марсупиализации и
дренированием всех зон некроза/инфекции
дренажами Пенроза в комбинации с
многопросветными трубчатыми конструкциями.
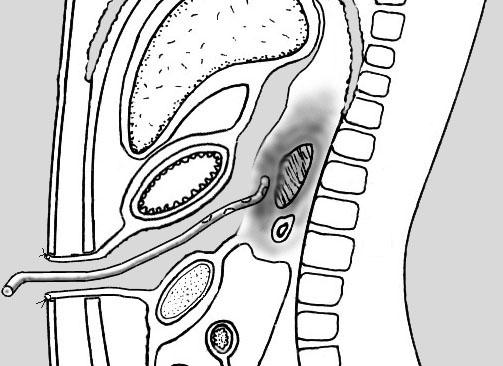
Рис.
13. Дренирование сальниковой сумки через
оментопанкреатобурсостому.
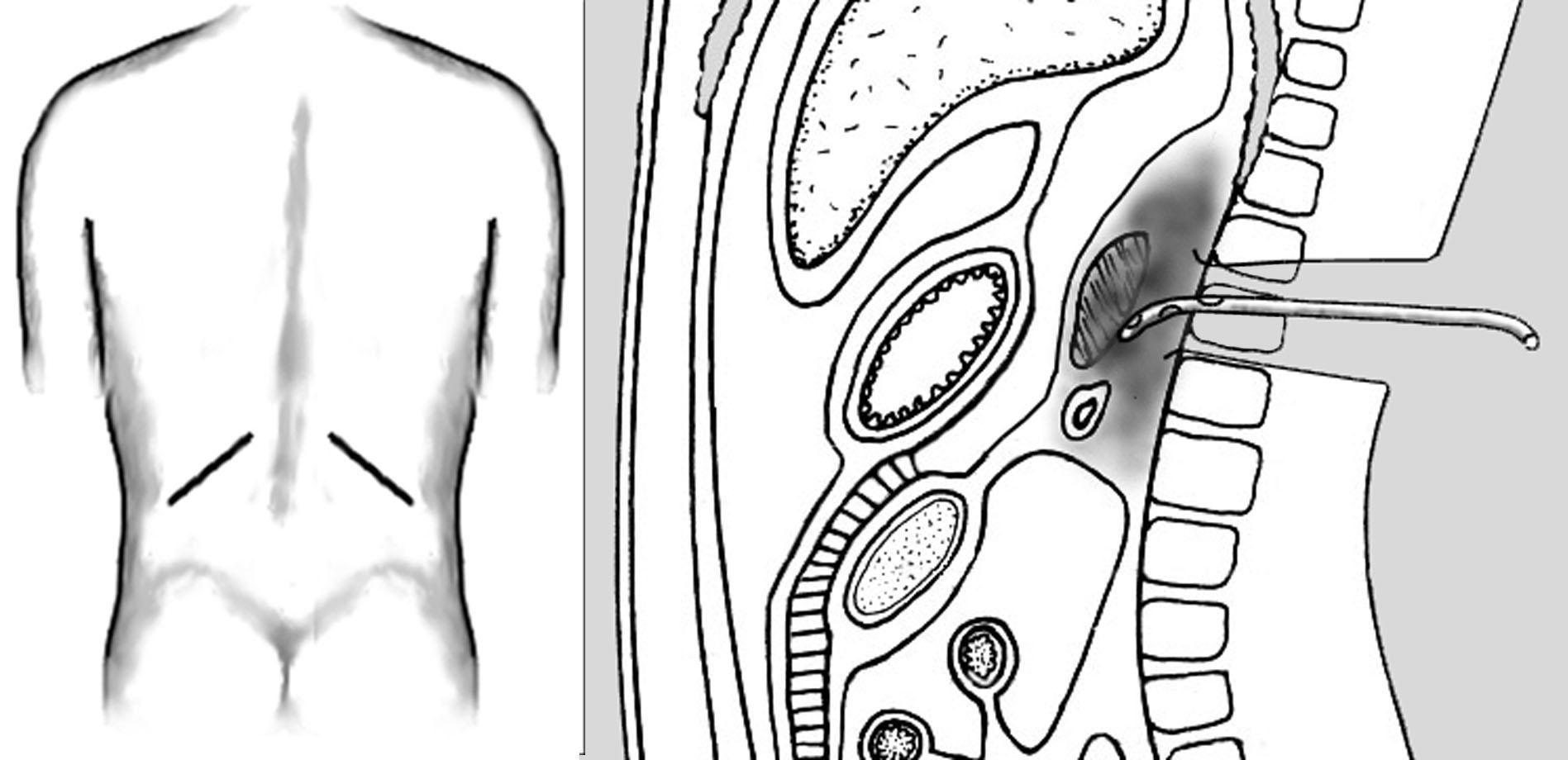
Рис.
14. Дренирование парапанкреатических
пространств (Б) через поясничный доступ
(А).
Дренаж
Пенроза, именуемый в отечественной
литературе как «резиново-марлевый
тампон», пропитывают антисептиками
и мазями на водорастворимой основе
(«Левосин», «Левомеколь»). Такая
хирургическая тактика обеспечивает в
последующем беспрепятственный доступ
к этим зонам и выполнение адекватных
некрсеквестрэктомий в программируемом
режиме с интервалом
48-72 часа.
Этапная замена дренажей Пенроза позволяет
устранить их существенный недостаток,
связаный с кратковременной дренажной
функцией и экзогенным (ре)инфицированием.
По мере очищения забрюшинной клетчатки
от некрозов и детрита, при появлении
грануляционной ткани показан переход
к «закрытому» методу дренирования.
При
развитии распространенного гнойного
перитонита и крайней степени тяжести
состояния больного при распространенном
и/или инфицированном панкреонекрозе
(тяжелый сепсис, септический шок, АРАСНЕ
II > 13
баллов, Ranson
> 5 баллов)
показана лапаростомия. проведение
программируемых санаций забрюшинной
клетчатки и брюшной полости через
12-48 часов.
III.
«Полуоткрытый» метод дренирования
при панкреонекрозе предполагает
установку -рубчатых многопросветных
дренажных конструкций в комбинации с
дренажем Пенроза. В этих условиях
лапаротомную рану ушивают послойно, а
комбинированную конструкцию дренажей
выводят через широкую контраппертуру
в пояснично-боковых отделах живота
(люмботомия). Такого рода операции
получили название «традиционных»,
когда смена дренажных конструкций, как
правило, отсрочена на
5-7 суток.
При крупномасштабном некрозе и
секвестрации, сложной топографии
формируемых каналов зачастую создаются
условия для неадекватного дренирования
очагов некроза/инфекции и повторные
операции у 30-40%
больных выполняют с опозданием во
времени в режиме «по требованию».
Поэтому для предупреждения этих
осложнений потенциал дренирования
забрюшинной клетчатки можно повысить,
если производить адекватную замену
дренажей в режиме «по программе»,
т.е. не реже чем через
48-72 часа,
пропитывать дренаж Пенроза антисептическими
растворами, совмещать с сорбентами или
мазями на водорастворимой основе
(«Левосин»/»Левомеколь»).
Реализация адекватной хирургической
тактики в условиях -«полуоткрытого»
метода наружного дренирования при
панкреонекрозе достигается выполнением
только программируемых оперативных
вмешательств. Режим «по требованию
в этой ситуации следует признать не
эффективным, не имеющим ни теоритического,
ни практического обоснования.
Следует
особо отметить, что представленные
методы «закрытого» и «открытого»
дренирования забрюшинной клетчатки не
являются конкурирующими, так как при
соблюдении методологии и обоснованных
показаниях призваны обеспечить адекватную
и полную санацию всех зон некротической
деструкции и панкреатогенной инфекции.
В
заключении необходимоособо
отметить,
что дальнейший прогресс в улучшении
результатов комплексноголечения
деструктивного панкреатита определяется
совместной работой хирургических
коллективов Российской Федерации.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник


