Послеоперационный период острого панкреатита
После операций,
произведенных на органах брюшной полости
(на самой железе, резекция сигмовидной
кишки, спленэктомия, аппендикулярный
перитонит и др.), острый панкреатит у
детей возникает чаще, чем диагностируется.
Обычно панкреатит развивается при
непрямой операционной травме вследствие
нарушения кровотока и микротромбозов
в лод-желудочной железе из-за нарастающего
токсикоза, травматичных манипуляций
на брыжейке, пареза кишечника. Приведенные
причины не могут являться единственным
этиологическим фактором в развитии
острого панкреатита, Определенную роль
играет, по всей видимости, наследственная
предрасположенность к появлению этого
осложнения, связанная с индивидуальными
особенностями строения большого сосочка
двенадцатиперстной кишки и кровоснабжения.
Клиническая
картина. Острый
послеоперационный панкреатит развивается
на 2—6-й день после хирургического
вмешательства. Его клиническая картина
не имеет характерных особенностей и
обычно сочетается с проявлениями других
осложнений послеоперационного периода,
а также маскируется применяемыми
лекарственными средствами или проводимыми
лечебными мероприятиями. Вместе с тем
внимательное наблюдение за ребенком и
определенная настороженность в отношении
возможности развития этого осложнения
позволяют правильно трактовать симптомы.
Панкреатит обычно
возникает в тот период, когда общее
состояние ребенка несколько улучшается.
На фоне улучшения больной начинает
жаловаться на усиление болей в животе,
которые носят постоянный характер. Дети
младшего возраста не локализуют бодь
или указывают на область операционной
раны. Старшие более точно определяют
ее локализацию— в верхних отделах
живота, левом подреберье. Общее состояние
заметно ухудшается Ребенок беспокойно
спит, появляется рвота застойным
содержимым. Язык обложен, суховат. Живот
вздувается в надчревной области Плохи
отходят газы, стула нет. Уменьшается
количество мочи. Температура тела
повышается, иногда до высоких показателей.
Пульс
частый, одышка. Пальпация живота
болезненна в верхних отделах, но этот
симптом обычно мало помогает диагностике,
так как ребенок сопротивляется осмотру
из-за болей в,
области
операционной раны. Перкуторно выявляется
тимпанит, иногда может быть незначительное
притупление в отлогих местах.
Отмечаются
лейкоцитоз до (15—20) х 10 9/л,
нейтрофилез со сдвигом в формуле влево,
повышение СОЭ, гипокальциемия, уменьшение
количества альбуминов и увеличение
глобулинов; красная кровь не изменяется.
При
легкой форме панкреатита у детей хирург
обычно не придает значения некоторому
ухудшению общего состояния больного и
появившимся нерезко выраженным симптомам.
Осложнение остается нераспознанным,
однако прогноз, как правило, благоприятный
благодаря активному лечению основного
заболевания (жидкостная терапия, щадящая
диета, обезболивающие средства,
эпидуральная блокада и др.). В тяжелых
случаях неожиданное ухудшение состояния
должно натолкнуть лечащего врача на
мысль о развивающемся панкреатите.
Особую настороженность вызывают
появляющиеся у ребенка нарушения психики
(ферментная интоксикация)—делирий,
галлюцинации и др., Наибольшее значение
для диагностики имеют данные об активности
трипсина и амилазы в крови, амилазы в
моче, определяемые в динамике. Необходимо
учитывать, что возникновение отечной
формы панкреатита в послеоперационном
периоде может указывать на тяжелое
течение основного заболевания. В таких
случаях мы наблюдали в дальнейшем
развитие оментита при перитоните,
эвентрацни после инвагинации кишечника
и т. д.
Дифференциальную
диагностику проводят
с другими осложнениями послеоперационного
периода.
Послеоперационный
перфоративный
перитонит или
недостаточность швов анастомоза
проявляется быстро нарастающими
известными симптомами этого осложнения.
Помогают дифференциальной диагностике
обзорные рентгенограммы брюшной полости,
на которых при перфорации в большинстве
случаев можно выявить свободный газ
под диафрагмой. Исследование крови и
мочи на активность амилазы позволяет
уточнить диагноз. При невозможности
исключения перитонита показана срочная
релапаротомия.
Спаечно-паретическая
непроходимость развивается
постепенно, на фоне тяжелого общего
состояния и постоянных болей в животе;
стула нет, газы не отходят. Живот вздут
и напряжен во всех отделах, видны
перерастянутые петли Тонкой кишки.
Рвота частая, обильная, с застойным
содержимым, чего обычно не наблюдается
при послеоперационном панкреатите.
Сомнения разрешаются лабораторными
исследованиями и динамическим наблюдением.
Послеоперационное
внутрибрюшное
кровотечение сопровождается
коллаптоидным состоянием, что при
возникновении панкреатита наблюдается
в редких случаях. Дифференциальную
диагностику проводят, принимая во
внимание общеизвестные симптомы
кровотечения
и данные лабораторных
исследований. В сложных случаях прибегают
к микролапаротомии с применением
методики ^шарящего катетера».
Следует подчеркнуть,
что выявленное при лабораторном
исследовании увеличение активности
амилазы и липазы является у детей одним
из достоверных данных, свидетельствующих
о присоединении послеоперационного
панкреатита.
Лечение.
При
диагностированном послеоперационном
панкреатите проводят, как правило,
консервативное лечение. Больному следует
продолжить или назначить продленную
эпидуральную анестезию, отменить
кормление через рот, адекватно вводить
жидкость внутривенно и др. Особенно
важно немедленно применить в максимальных
дозах траси-лол или контрикал. Обычно
подобное лечение приводит к улучшению
общего состояния, снижению активности
амилазы и трипсина в крови, что позволяет
воздержаться от ревизии поджелудочной
железы.
Если
при неясном диагнозе хирург решается
на пробную релапарото-мию и во время
вмешательства не находит подозреваемого
осложнения (спаечная непроходимость,
недостаточность анастомоза, кровотечение
и др.), и при этом в брюшной полости
имеется геморрагический выпот, то
следует думать о панкреатите. Жидкость
срочно посылают в лабораторию для
исследования на активность амилазы. Не
разрушая имеющихся спаек, производят
ревизию сальниковой сумки и осматривают
поджелудочную железу. Чаще всего
обнаруживают отек, реже — геморрагический
некроз. Хирургическая тактика такая
же, как при идиопатическом панкреатите.
При дальнейшем
ведении больного необходимо проводить
лечение и основного заболевания, и
острого панкреатита.
Для
предупреждения послеоперационного
панкреатита лапаротомия, производимая
с травматичными манипуляциями на органах
брюшной полости либо на фоне перитонита,
должна в послеоперационном периоде
«прикрываться» продленной эпидуральной
блокадой для обеспечения физиологического
покоя поджелудочной железе. У детей,
поступающих на лапаротомию в тяжелом
состоянии из-за основного или сопутствующего
заболевания, контролируют активность
амилазы в крови и моче перед операцией
и после нее. При повышенной активности
амилазы целесообразно в пред- и
послеоперационное лечение включить
ингибиторы протеаз и контролировать
активность амилазы в ближайшие 3—4 дня
послеоперационного периода. Можно
предположить, что однократный подъем
активности амилазы в крови и моче у
оперированного ребенка не является
патогномоничным показателем патологических
изменений в поджелудочной железе, однако
указывает на индивидуальную «ранимость»
железы и повышение давления в ее
внутрипротоковой системе. При лечении
таких больных в послеоперационном
периоде необходимо настойчиво
предупреждать парез кишечника, расширять
энтеральное питание с ограничением
углеводов и постоянно контролировать
активность амилазы в крови и моче.
Источник
После операций, произведенных на органах брюшной полости (на самой железе, резекция сигмовидной кишки, спленэктомия, аппендикулярный перитонит и др.), острый панкреатит у детей возникает чаще, чем диагностируется. Обычно панкреатит развивается при непрямой операционной травме вследствие нарушения кровотока и микротромбозов в лод-желудочной железе из-за нарастающего токсикоза, травматичных манипуляций на брыжейке, пареза кишечника. Приведенные причины не могут являться единственным этиологическим фактором в развитии острого панкреатита, Определенную роль играет, по всей видимости, наследственная предрасположенность к появлению этого осложнения, связанная с индивидуальными особенностями строения большого сосочка двенадцатиперстной кишки и кровоснабжения.
Клиническая картина. Острый послеоперационный панкреатит развивается на 2—6-й день после хирургического вмешательства. Его клиническая картина не имеет характерных особенностей и обычно сочетается с проявлениями других осложнений послеоперационного периода, а также маскируется применяемыми лекарственными средствами или проводимыми лечебными мероприятиями. Вместе с тем внимательное наблюдение за ребенком и определенная настороженность в отношении возможности развития этого осложнения позволяют правильно трактовать симптомы.
Панкреатит обычно возникает в тот период, когда общее состояние ребенка несколько улучшается. На фоне улучшения больной начинает жаловаться на усиление болей в животе, которые носят постоянный характер. Дети младшего возраста не локализуют бодь или указывают на область операционной раны. Старшие более точно определяют ее локализацию— в верхних отделах живота, левом подреберье. Общее состояние заметно ухудшается Ребенок беспокойно спит, появляется рвота застойным содержимым. Язык обложен, суховат. Живот вздувается в надчревной области Плохи отходят газы, стула нет. Уменьшается количество мочи. Температура тела повышается, иногда до высоких показателей.
Пульс частый, одышка. Пальпация живота болезненна в верхних отделах, но этот симптом обычно мало помогает диагностике, так как ребенок сопротивляется осмотру из-за болей в, области операционной раны. Перкуторно выявляется тимпанит, иногда может быть незначительное притупление в отлогих местах.
Отмечаются лейкоцитоз до (15—20) х 10 9/л, нейтрофилез со сдвигом в формуле влево, повышение СОЭ, гипокальциемия, уменьшение количества альбуминов и увеличение глобулинов; красная кровь не изменяется.
При легкой форме панкреатита у детей хирург обычно не придает значения некоторому ухудшению общего состояния больного и появившимся нерезко выраженным симптомам. Осложнение остается нераспознанным, однако прогноз, как правило, благоприятный благодаря активному лечению основного заболевания (жидкостная терапия, щадящая диета, обезболивающие средства, эпидуральная блокада и др.). В тяжелых случаях неожиданное ухудшение состояния должно натолкнуть лечащего врача на мысль о развивающемся панкреатите. Особую настороженность вызывают появляющиеся у ребенка нарушения психики (ферментная интоксикация)—делирий, галлюцинации и др., Наибольшее значение для диагностики имеют данные об активности трипсина и амилазы в крови, амилазы в моче, определяемые в динамике. Необходимо учитывать, что возникновение отечной формы панкреатита в послеоперационном периоде может указывать на тяжелое течение основного заболевания. В таких случаях мы наблюдали в дальнейшем развитие оментита при перитоните, эвентрацни после инвагинации кишечника и т. д.
Дифференциальную диагностику проводят с другими осложнениями послеоперационного периода.
Послеоперационный перфоративный перитонит или недостаточность швов анастомоза проявляется быстро нарастающими известными симптомами этого осложнения. Помогают дифференциальной диагностике обзорные рентгенограммы брюшной полости, на которых при перфорации в большинстве случаев можно выявить свободный газ под диафрагмой. Исследование крови и мочи на активность амилазы позволяет уточнить диагноз. При невозможности исключения перитонита показана срочная релапаротомия.
Спаечно-паретическая непроходимость развивается постепенно, на фоне тяжелого общего состояния и постоянных болей в животе; стула нет, газы не отходят. Живот вздут и напряжен во всех отделах, видны перерастянутые петли Тонкой кишки. Рвота частая, обильная, с застойным содержимым, чего обычно не наблюдается при послеоперационном панкреатите. Сомнения разрешаются лабораторными исследованиями и динамическим наблюдением.
Послеоперационное внутрибрюшное кровотечение сопровождается коллаптоидным состоянием, что при возникновении панкреатита наблюдается в редких случаях. Дифференциальную диагностику проводят, принимая во внимание общеизвестные симптомы кровотечения
и данные лабораторных исследований. В сложных случаях прибегают к микролапаротомии с применением методики ^шарящего катетера».
Следует подчеркнуть, что выявленное при лабораторном исследовании увеличение активности амилазы и липазы является у детей одним из достоверных данных, свидетельствующих о присоединении послеоперационного панкреатита.
Лечение. При диагностированном послеоперационном панкреатите проводят, как правило, консервативное лечение. Больному следует продолжить или назначить продленную эпидуральную анестезию, отменить кормление через рот, адекватно вводить жидкость внутривенно и др. Особенно важно немедленно применить в максимальных дозах траси-лол или контрикал. Обычно подобное лечение приводит к улучшению общего состояния, снижению активности амилазы и трипсина в крови, что позволяет воздержаться от ревизии поджелудочной железы.
Если при неясном диагнозе хирург решается на пробную релапарото-мию и во время вмешательства не находит подозреваемого осложнения (спаечная непроходимость, недостаточность анастомоза, кровотечение и др.), и при этом в брюшной полости имеется геморрагический выпот, то следует думать о панкреатите. Жидкость срочно посылают в лабораторию для исследования на активность амилазы. Не разрушая имеющихся спаек, производят ревизию сальниковой сумки и осматривают поджелудочную железу. Чаще всего обнаруживают отек, реже — геморрагический некроз. Хирургическая тактика такая же, как при идиопатическом панкреатите.
При дальнейшем ведении больного необходимо проводить лечение и основного заболевания, и острого панкреатита.
Для предупреждения послеоперационного панкреатита лапаротомия, производимая с травматичными манипуляциями на органах брюшной полости либо на фоне перитонита, должна в послеоперационном периоде «прикрываться» продленной эпидуральной блокадой для обеспечения физиологического покоя поджелудочной железе. У детей, поступающих на лапаротомию в тяжелом состоянии из-за основного или сопутствующего заболевания, контролируют активность амилазы в крови и моче перед операцией и после нее. При повышенной активности амилазы целесообразно в пред- и послеоперационное лечение включить ингибиторы протеаз и контролировать активность амилазы в ближайшие 3—4 дня послеоперационного периода. Можно предположить, что однократный подъем активности амилазы в крови и моче у оперированного ребенка не является патогномоничным показателем патологических изменений в поджелудочной железе, однако указывает на индивидуальную «ранимость» железы и повышение давления в ее внутрипротоковой системе. При лечении таких больных в послеоперационном периоде необходимо настойчиво предупреждать парез кишечника, расширять энтеральное питание с ограничением углеводов и постоянно контролировать активность амилазы в крови и моче.
Дата добавления: 2015-05-25; просмотров: 1797; Опубликованный материал нарушает авторские права? | Защита персональных данных | ЗАКАЗАТЬ РАБОТУ
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: При сдаче лабораторной работы, студент делает вид, что все знает; преподаватель делает вид, что верит ему. 9611 — | 7390 — или читать все…
Читайте также:
Источник
Библиографическое описание:
Ибадильдин А. С., Джакашева Ж. А., Апырбаев О. Н. Современные принципы диагностики и лечения послеоперационного панкреатита // Молодой ученый. 2015. №11. С. 655-658. URL https://moluch.ru/archive/91/19574/ (дата обращения: 27.01.2020).
Актуальность: быстрый темп развития компьютерных технологий в медицине и новейших методов обследования пациентов позволяет нам в кратчайшие сроки установить диагноз послеоперационных осложнений. Одним из таких осложнений является послеоперационный панкреатит.
В большинстве случаев послеоперационный панкреатит развивается в первые 3–4 суток после операции. Частота данного осложнения после лапаротомий составляет 0,7–25,6 %, а при операциях на поджелудочной железе возрастает до 32,7–50 % (Б. И. Альперович 1991 г., Р. В. Вашетко с соавт.) [1].
Клиника послеоперационного панкреатита вариабельна, каких-либо патогномоничных симптомов не имеет. Этим объясняется постоянный поиск новых, информативных методов распознавания его [2].
Выявление гомеостазиологических нарушений, их коррекция, своевременная релапаротомия предопределяют исход заболевания больных послеоперационным панкреатитом и являются актуальными проблемами [3].
Летальность при послеоперационном панкреатите остается высокой — 24,5 %, а при деструктивных формах достигает 50–60 % и не имеет тенденции к снижению (Р. В. Вашетко).
Цель исследования: оптимизировать алгоритм диагностики, лечения послеоперационного панкреатита и определить оптимальные сроки релапаротомии для снижения летальности.
Задачи:
— изучить частоту развития панкреатита после операции на органах брюшной полости,
— выявить частоту клинико-лабораторных проявлений послеоперационного панкреатита,
— определить значимость неинвазивных и малоинвазивных методов диагностики послеоперационного панкреатита,
— определить необходимость и оптимальные сроки релапаротомии,
— разработать эффективные способы санации брюшной полости.
Материалы и методы. Мы проанализировали результаты лечения 6689 больных оперированных в военном госпитале г. Алматы с 1982 по 2012 гг. по поводу заболеваний и травм органов брюшной полости.
Операции были проведены на следующих органах: поджелудочной железе — 253(10 случаев послеоперационного панкреатита — 4 %), желудке и двенадцатиперстной кишке — 1268 (24 случая — 1,9 %), билиарном дереве — 3152 (28 случаев — 0,9 %), печени — 1231 (3 случая — 0,2 %), селезенке и прочих органах — 785 (6 случаев — 0,8 %) (см. Диаграмма 1).
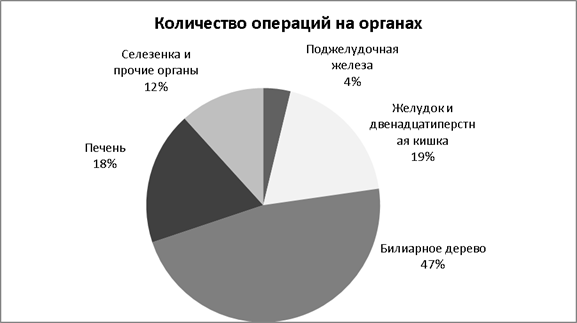
Рис. 1.
Послеоперационный панкреатит развился у 71 больного (1,1 %). Мужчин — 59 (83 %), женщин — 12 (17 %). Возраст больных колеблется в пределах от 25 до 74 лет.
Клинически, лабораторно и УЗИ-подтвержденный послеоперационный панкреатит возник на 3–4 сутки, только у 8 человек на 7–8 сутки. Клиническая картина его характеризовалась скудностью и непостоянством симптоматики.
Частыми клиническими проявлениями были: боль в верхних отделах живота — 68 (95,8 %); тахикардия — 64 (90 %); парез кишечника, не поддающийся лечению — 52 (73,2 %); рвота — 47 (66,2 %); гипертермия — 38 (53,5 %); напряженный мышечный дефанс в эпигастрии — 33 (46,5 %); иктеричность кожи — 28 (39,4 %); положительный симптом Щеткина-Блюмберга — 25 (35,2 %); коллапс — 12 (16,9 %); психоз — 12 (16,9 %); икота — 10 (14 %) (см. Диаграмма 2).
В общем анализе крови отмечался выраженный лейкоцитоз в 62 (81,3 %) случаях, сдвиг лейкоцитарной формулы влево в 30 (42,3 %) случаях, токсическая зернистость лейкоцитов в 22 (31 %) случаях. Биохимический анализ крови показал гипербилирубинемию за счет прямой фракции у 25 (35 %) пациентов, повышение уровня АЛТ и АСТ у 21 (30 %), гипергликемию у 15 (21 %) и повышение амилазы у 32 (45 %) пациентов. Диастазурия имелась в 35 (49 %) случаях, но только у 23 (32 %) больных достигла значительных цифр.
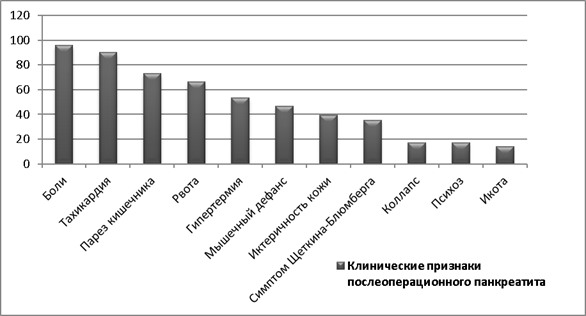
Рис. 2.
Вышеперечисленный симптомокомплекс показывает глубину гомеостатических нарушений и не является патогномоничным для данного осложнения. Для облегчения постановки диагноза, мы выделили основные симптомы, такие как: боли в верхних отделах живота, выраженный парез кишечника, тахикардия, гипертермия. Значительную роль в диагностике сыграла диастазурия и использование специальных методов исследования. При рентгенологическом обследовании у 32 (45 %) больных выявлены косвенные признаки панкреатита: вздутие поперечно-ободочной кишки, левосторонний реактивный плеврит, симптом «дежурной кишки», симптом «вырезанной кишки», симптом «отсеченной ободочной кишки». Ультразвуковое исследование позволяет выявить увеличение размеров, размытость контуров поджелудочной железы, наличие выпота в сальниковой сумке. После операции на органах верхнего отдела брюшной полости не всегда удается визуализировать поджелудочную железу: из 68 обследованных больных ценная информация получена у 41. Наиболее информативными являются компьютерная томография и диагностическая видеолапароскопия.
В клинике мы начинаем лечение с функционального покоя поджелудочной железы: декомпрессии желудка, локальной гипотермии, парентерального, а в последние годы и энтерального питание. Проводим коррекцию нарушений гемостаза, детоксикацию, улучшение реологии крови, купирование проявлений синдрома системного воспалительного ответа. Широко используем управляемую гемодилюцию с форсированным диурезом [4].
Особое значение мы придаем мероприятиям по блокированию повреждающего воздействия ферментативного токсического экссудата, играющего важную роль на ранних стадиях тяжелого послеоперационного панкреатита и применению различных методик выведения токсических компонентов из тканевых депо.
При проведении курса интенсивной консервативной терапии у 49 (69 %) из 71 больных отмечалось субъективное и объективное улучшение состояния через 36–48 часов от начала лечения: купировались признаки интоксикации, нормализовались показатели крови и диастазы.
В 22 (31 %) случаях консервативное лечение не имело эффекта. Прогрессивное ухудшение состояния пациентов, нарастание симптомов ферментной токсемии, появление признаков перитонита явились показанием к релапаротомии. 16 пациентов взяты на операцию с диагнозом послеоперационный панкреатит. У 6 больных был выставлен диагноз: высокая тонкокишечная непроходимость (4), недостаточность швов анастомоза (2).
Релапаротомии произведены в следующие сроки с момента появления симптомов осложнения: через 6–24 часов — у 9 больных, на 2–4 сутки — у 12, на 5 сутки — у 1 (см. Диаграмма 3). При релапаротомии диагностированы жировой панкреонекроз у 14, геморрагический панкреонекроз у 8 больных. Перитонит диагностирован в 19 случаях (86,4 %).
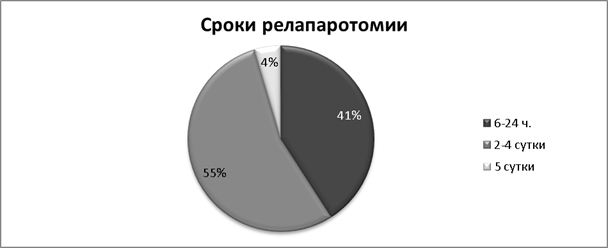
Рис. 3.
Во время операции по поводу тяжелого послеоперационного панкреатита хирург должен решить несколько проблем. Наиболее сложной и ответственной является выбор рациональной хирургической тактики.
У 12 больных после релапаротомии проводилась программированная видеолапароскопическая санация брюшной полости по нашей методике с использованием специального лапаропорта (патент № 19772 от 28.05.2008г.). Лапаропорт устанавливали и фиксировали на передней брюшной стенке. Через него выполнялась ревизия и санация брюшной полости эндохирургической стойкой фирмы «Карл Шторц». После окончания лечения лапаропорт удаляли, а фиксирующие его нити завязывали, закрывая дефект передней брюшной стенки [5].
Больные получали внутриаортальную инфузию лекарственных средств, антибиотикотерапию, управляемую гемодилюцию с форсированным диурезом. На фоне послеоперационного тяжелого течения с явлениями интоксикации, пареза кишечника у 10 (45,4 %) больных развились осложнения: у 5 (22,7 %) пневмония, у 3 (13,6 %) плеврит, у 2 (9,1 %) флегмона брюшной стенки. Двое (9,1 %) повторно 2 раза оперированы по поводу спаечной кишечной непроходимости и абсцессов брюшной полости. Проводилась иммунокоррегирующая и иммунозаместительная терапия. При анемии переливали свежецитратную кровь. Применяли анаболические гормоны и пиримидиновые производные, антистафилококковую плазму, антистафилококковый гамма-глобулин.
Умерло 6 больных, что составило 8,4 % от всех случаев послеоперационного панкреатита и 27,2 % после релапаротомий. У 5 на вскрытии геморрагический панкреонекроз, у 1 — жировой с распространением некротического процесса на забрюшинную клетчатку. Причиной летального исхода явилось у 5 больных прогрессирование панкреонекроза, у 1 профузное кровотечение из магистральных артериальных сосудов.
Выводы:
1. Доминирующими клиническими проявлениями послеоперационного панкреатита явились болевой синдром, выраженный парез кишечника, тахикардия, гипертермия;
2. Для ранней диагностики и коррекции лечения информативными оказались неинвазивные методы мониторирования — рентгенологическое, ультразвуковое исследования, компьютерная томография, клинико-лабораторные данные;
3. Неэффективность консервативной терапии в течении суток должна явиться показанием для релапаротомии;
4. Операция должна быть минимальной по объему;
5. Применение лапароскопического мониторирования позволило своевременно санировать и купировать прогрессирование послеоперационного панкреатита.
Литература:
1. Басенов Л. Н. Неотложная хирургия груди и живота. Руководство для врачей. СПб, Гиппократ, 2002 г.
2. Макаренко Г. П. Ведение больных общехирургического профиля в послеоперационном периоде, 1989 г.
3. Клиническая хирургия: Национальное руководство, 3 т. (редакция Савельев В. С., Карпенко А. И., Гальперин Э. И., Милонов О. Б.) — Медиа, 2002г., том — 2.
4. Неотложная хирургия органов брюшной полости (клиническое руководство) под редакцией Кондратенко П. Г., Русина В. И. Донецк, 2013 г.
5. Ибадильдин А. С.. Хирургические болезни. Алматы, 2010.
Основные термины (генерируются автоматически): послеоперационный панкреатит, брюшная полость, больной, поджелудочная железа, тяжелый послеоперационный панкреатит, передняя брюшная стенка, парез кишечника, компьютерная томография, верхний отдел живота, форсированный диурез.
Источник


