Острый панкреатит с острой полиорганной недостаточностью
Библиографическое описание:
Нестеренко С. П. Оценка полиорганной недостаточности при остром панкреатите // Молодой ученый. 2014. №19. С. 112-115. URL https://moluch.ru/archive/78/13569/ (дата обращения: 23.01.2020).
Изучено функциональное состояние органов/систем при различных клинико-морфологических формах острого панкреатита. Установлены сроки и последовательность поражения органов и систем при данной патологии.
Ключевые слова: острый панкреатит, полиорганная недостаточность.
Синдром полиорганной недостаточности в настоящее время определяется как универсальное поражение двух и более органов и систем организма в результате тяжёлой неспецифической стресс-реакции на множественные этиологические факторы, когда нарушения физиологических функций отдельных органов и систем не могут спонтанно восстанавливаться путём ауторегуляции и требуют частичной или полной коррекции или протезирования утраченных функций [1].
Несмотря на определенные достижения последних лет в улучшении диагностики, прогнозирования и лечения, острый панкреатит остается одной из актуальных проблем неотложной хирургии и интенсивной терапии, что обусловлено неуклонным ростом заболеваемости, увеличением доли случаев некротического панкреатита и стабильно высокими показателями летальности [1,3,6,7].
Согласно сборной статистике, в зависимости от демографических и этнических особенностей, уровня экономического и социального развития региона число случаев острого панкреатита варьирует от 5 до 80 на 100 тыс. населения в год [2,3,4]. В структуре острой хирургической патологии органов брюшной полости общехирургических стационаров острый панкреатит вышел на первое место по частоте, опережая по темпам роста заболеваемости прочие нозологические формы [3,5,6,7], при этом удельный вес больных острым панкреатитом составляет 10–25 % [4,5,6,7], а по отдельным сведениям достигает 40 % [4]. В литературных источниках последних лет достаточно полно освещены этиологические моменты, приводящие к развитию острого панкреатита, однако патогенетические механизмы развития заболевания до конца не раскрыты. Одним из недостаточно изученных остается вопрос содружественного поражения различных органов. Поэтому разработка новых схем лечения этой грозной патологии не может не базироваться на знаниях этого аспекта болезни
Цель: установить последовательность поражения органов при различных формах острого панкреатита.
Задачи:
1. Оценить функциональное состояние органов и систем при различных формах острого панкреатита по В. В. Чаленко (1998);
2. Установить сроки поражения органов в зависимости от момента начала заболевания.
Материал и методы
В основу работы положен ретроспективный анализ историй болезни 77 пациентов с острым панкреатитом, находившихся на лечении в 432 ГВКМЦ г. Минска с 2007 по 2013 гг.
Результаты и обсуждения
При анализе историй болезни пациентов было установлено следующее: мужчины чаще заболевают панкреатитом (примерно 90 %, соответственно 10 % — женщины). Средний возраст 50 лет±5 лет. Алкоголь как этиологический фактор стоит на первом месте, патология билиарного тракта на втором (у женщин на первом месте заболевания билиарной системы). 50 % больных при отечном панкреатите поступают до 1 суток; 30 % больных при неинфицированном панкреатите поступают до 1 суток, 37 %-позже 3 суток; 100 % больных при инфицированном панкреатите поступают позже 3 суток (таблица 1).
Таблица 1
Характеристика сравниваемых групп
Показатель | Отечный | Неинфицированный | Инфицированный |
Пол: 1. мужчины 2. женщины | 90 % 10 % | 91,5 % 8,5 % | 89 % 11 % |
Возраст | 57±5лет | 50±5лет | 46±5лет |
Этиология: 1. алиментарный 2. билиарный 3. прочие причины | 66 % 11 % 23 % | 71 % 24 % 5 % | 77 % — 23 % |
Сроки от начала заболевания: 1. до 12 ч 2. 13–24 ч 3. 25–72 ч 4. позже 72 ч | 55 % — 33 % 12 % | 33 % 15 % 15 % 37 % | — — — 100 % |
Для оценки функционального состояния органов и систем использовали классификацию по В. В. Чаленко (1998), согласно которой выделяют удовлетворительную функцию, компенсированную недостаточность, несостоятельность функции органа.
Функцию печени оценивали по показателям:
1. Билирубина;
2. АсАТ/АлАТ (коэффициент де Ритиса).
Поступление больных в разные сроки позволило нам выявить развитие органной недостаточности (рис. 1).
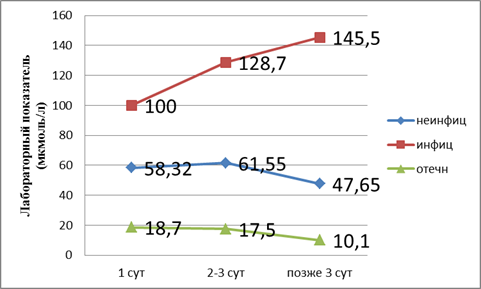
Рис. 1. Показатели билирубина в динамике
Из графика следует, что, согласно классификации по В. В. Чаленко, при отечном панкреатите развивается дисфункция печени, так как лабораторные показатели в пределах верхней границы нормы. При неинфицированном — компенсированная недостаточность. При инфицированном панкреатите развивается декомпенсированная недостаточность печени. Поражение печени при неинфицированном панкреатите происходит на третьи сутки. Далее при адекватном лечении процесс купируется. При инфицированном панкреатите мы наблюдаем рост показателей билирубина.
Если оценку произвести по коэффициенту де Ритиса (рис. 2), то можно сказать, что, как и при оценке показателя билирубина, при отечном панкреатите развивается дисфункция печени, так как лабораторные показатели в пределах верхней границы нормы. При неинфицированном — компенсированная недостаточность. При инфицированном панкреатите развивается декомпенсированная недостаточность печени.
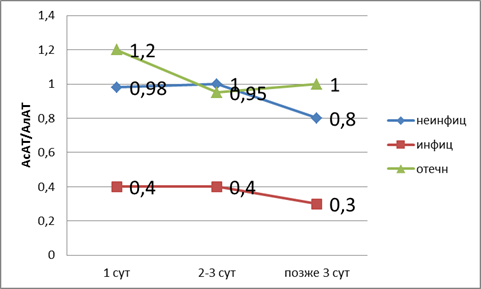
Рис. 2. Показатели коэффициента де Ритиса
Функцию почек оценивали по показателям креатинина и мочевины в крови (таблица 2).
Таблица 2
Изменение показателей креатинина и мочевины
Срок от момента заболевания | Отечный | Неинфицированный | Инфицированный | |||
Креатинин (мкмоль/л) | Мочевина (ммоль/л) | Креатинин (мкмоль/л) | Мочевина (ммоль/л) | Креатинин (мкмоль/л) | Мочевина (ммоль/л) | |
1 сутки | 110 | 8,025 | 128,44 | 8,5 | 143,2 | 9,7 |
2–3 сутки | 100,54 | 7,55 | 145,6 | 9,8 | 162,5 | 10,26 |
Позже 3 сут | 80,75 | 6,3 | 100,3 | 7,2 | 204,86 | 11,3 |
При отечном панкреатите развивается дисфункция почек, так как лабораторные показатели в пределах верхней границы нормы. При неинфицированном-компенсированная недостаточность почек. При инфицированном панкреатите развивается декомпенсированная недостаточность. Поражение почек происходит при неинфицированном панкреатите на третьи сутки, но при адекватной терапии процесс купируется. При инфицированном панкреатите мы наблюдаем рост лабораторных показателей креатинина и мочевины.
Функцию легких оценивали по показателям pCO2, pO2 в венозной крови и рентгенологическому признаку. В результате исследования установлено, что при отечном панкреатите развивается дисфункция легких, так как лабораторные показатели в пределах верхней границы нормы. При неинфицированном развивается компенсированная недостаточность, а при инфицированном панкреатите развивается декомпенсированная недостаточность легких. Поражение легких происходит при неинфицированном панкреатите через 24 часа с момента заболевания, но при адекватной терапии процесс купируется. При инфицированном панкреатите мы наблюдаем рост лабораторных показателей. Рентгенологически при отечном панкреатите изменений со стороны легких не выявлено. При неинфицированном рентгенологически встречаются в 39 % реактивный плеврит, 4 % составили пневмонии. При инфицированном панкреатите в 68 % встречается реактивный плеврит, пневмонии составили 7 %.
Выводы:
1. При панкреатите возникает поражение органов-мишеней: легких, печени и почек с нарушением функции;
2. Поражение легких возникает одним из первых (через 24 часа от момента заболевания) и проявляется развитием РДСВ;
3. Вовлечение в патологический процесс печени и почек происходит позднее — через 72 часа от начала заболевания;
4. При отечном панкреатите, который носит абортивное течение, развивается дисфункция органа. При неинфицированном — компенсированная недостаточность, а при инфицированном панкреатите развивается декомпенсированная недостаточность функции органа.
Литература:
1. Голуб, И. Е. Полиорганная недостаточность: Учебное пособие / И. Е. Голуб, Л. В. Сорокина, Е. С. Нетесин. — Иркутск: ИГМУ. — 2011. — 25 с.
2. Рузавина, А. В. Системные факторы прогрессирования острого панкреатита: автореф. дис. канд. мед. наук: 14.01.17 / А. П. Власов. — Ульяновск, 2012. — 17с.
3. Семенова, А. С. Оценка эндогенной интоксикации при остром панкреатите / А. С. Семенова // Поколение СГМУ 2003: новые рубежи: Сб. научно-практической конференции СГМУ. — Саратов, 2003. — С. 44.
4. Багненко, С. Ф. Хирургическая панкреатология / С. Ф. Багненко, А. А. Курыгин, Г. И. Синченко. — СПб.: Издательство «Речь», 2009. — 603 с.
5. Балныков, С. И. Прогнозирование исхода заболевания у больных некротическим панкреатитом / С. И. Балныков, Т. Ф. Петренко // Хирургия. — 2010. — № 3. — С. 57–59.
6. Гальперин, Э. И. Панкреонекроз: неиспользованные резервы лечения (дискуссионные вопросы к круглому столу) / Э. И. Гальперин, Т. Г. Дюжева // Анналы хирург. гепатологии. — 2007. — Т. 12, № 2. — С. 46–51.
7. Клиническая хирургия: национальное руководство: в 3 т. / под ред. В. С. Савельева, А. И. Кириенко. — М.: ГЭОТАР-Медиа, 2009. — т. 2. — 832 с.
Основные термины (генерируются автоматически): острый панкреатит, инфицированный панкреатит, отечный панкреатит, компенсированная недостаточность, верхняя граница нормы, неинфицированный панкреатит, момент заболевания, показатель, сутки, функциональное состояние органов.
Источник
Эпидемиологические исследования последних десятилетий свидетельствуют о неуклонном росте заболеваемости острым панкреатитом (ОП) во всем мире [10]. Приблизительно у 80% больных отмечаются легкие формы ОП, не требующие интенсивного лечения (летальность не превышает 3%), однако в случае развития системных осложнений заболевания госпитальная летальность может достигать 69% [7]. Особенностью эпидемиологической ситуации в нашей стране является высокий показатель заболеваемости среди трудоспособного населения, так, по данным А.С. Ермолова и соавт., в течение анализируемого периода 1993-2007 гг. отмечено увеличение числа больных молодого возраста, поступивших с диагнозом ОП в стационары Москвы [2].
В опубликованном в 2009 г. популяционном исследовании (проанализировано 1024 летальных исхода за период 2002-2006 гг.) D. Mole и соавт. [12] сделали заключение, что для ОП характерна ранняя летальность — медиана интервала между началом заболевания и летальным исходом составила 6 дней (интерквартильный размах 17 дней). Авторы также отмечают главенствующую роль полиорганной недостаточности (ПОН) в развитии неблагоприятных исходов — медиана интервала между манифестацией ПОН и летальным исходом составила 3 дня (интерквартильный размах 7 дней). Второго пика летальности, обусловленного неблагоприятными исходами на фоне гнойно-септических осложнений и описанного C. McKay и A. Buter в 2003 г. [15], не было выявлено.
Динамика ПОН в течение первых 72 ч госпитализации, по заключению ряда авторов, является важнейшим диагностическим маркером тяжелого течения ОП. Приблизительно у 50% больных с прогнозируемым тяжелым течением панкреатита органная дисфункция имеет транзиторный характер и на фоне своевременно начатой интенсивной терапии, к 3-м суткам заболевания состояние больных стабилизируется, а летальность не превышает 1,4%. В случае, если ПОН в течение первых дней заболевания сохраняется или прогрессирует, летальность достигает 55% [9, 13].
Патогенез ПОН у больных ОП тесно связан с развитием системной воспалительной реакции, высвобождением медиаторов воспаления, гиповолемией, синдромом ишемии-реперфузии, бактериальной транслокацией и др. [6].
Эффективность коррекции возникших нарушений гомеостаза в ранний период (формирования некрозов и манифестации системных осложнений), профилактика развития поздних осложнений, по данным экспериментальных исследований, зависит от сроков ее начала — так называемое «открытое терапевтическое окно», ограниченное первыми 72 ч после индукции ОП [11, 14, 16].
Таким образом, раннее выявление больных с высоким риском развития прогрессирующей ПОН, своевременная их госпитализация и начало комплексного консервативного лечения в отделениях интенсивной терапии могут способствовать улучшению результатов лечения этой наиболее тяжелой категории больных.
Цель исследования — выявить диагностические критерии тяжелого ОП с ранней прогрессирующей ПОН.
Для решения поставленной задачи было проведено комплексное клинико-лабораторное обследование 152 больных тяжелым острым панкреатитом (ТОП) [8], госпитализированных не позднее 4-х суток от начала заболевания в отделение реанимации и интенсивной терапии для больных с острыми эндотоксикозами НИИ СП им. Н.В. Склифосовского с 2002 по 2009 г. Из исследования были исключены больные с травматическим панкреатитом и больные, переведенные из других медицинских учреждений.
При анализе анамнестических данных медиана интервала между началом заболевания и поступлением больного в стационар составила 24 ч (9;48 ч).
Средний возраст больных 43±14 лет. Среди больных преобладали мужчины — 123 (81%). Двумя основными причинами развития ТОП были злоупотребление алкоголем и заболевания билиарного тракта — 92 (60,5%) и 32 (21,1%) больных соответственно. Среди других этиологических факторов (n=16) отмечены гиперхолестеринемия, синдром приводящей петли, ятрогенные осложнения после проведения ретроградной холангиопанкреатографии и эндоскопической папиллосфинктеротомии. У 12 (7,9%) больных причина ОП не была выявлена.
При поступлении в реанимационное отделение тяжесть состояния больных по шкале APACHE II составляла 13 (8;18) баллов, по шкале Ranson — 6 (3;11), тяжесть органной дисфункции по шкале SOFA — 4 (2;6). Наиболее часто у больных встречались признаки острой дыхательной недостаточности (69%), острого почечного повреждения (67%) и печеночной недостаточности (63%). В день госпитализации медиана количества поврежденных органов соответствовала нарушению функции 3 (2;4) органов или систем ≥1 баллу по критериям шкалы SOFA.
В зависимости от распространенности некроза ткани поджелудочной железы больные распределились следующим образом: тотальный или субтотальный панкреонекроз был у 33 (22%), крупноочаговый — у 55 (36%), мелкоочаговый — у 64 (42%).
Для статистического анализа полученных данных использовали пакет программ SPSS 15.0 (SPSS, Inc.) и STATISTIKA 6.0 (Stat.Soft , Inc.). При распределении, отличном от нормального, для несвязанных выборок использовали непараметрический критерий Манна-Уитни, для связанных выборок — критерий Вилкоксона. Рассчитывали медиану, 25- и 75-процентные перцентили. Для сравнения номинативных данных использовали критерий хи-квадрат с поправкой Йетса. Оценку качества прогностических моделей, уровня их чувствительности и специфичности проводили с использованием ROC-анализа [1, 5].
С целью исследования роли ПОН в развитии фатальных осложнений нами были выбраны две группы больных — ТОП с ранней сохраняющейся или прогрессирующей ПОН (n=106) и без признаков ПОН (n=46) в первые 72 ч после поступления. Сравнительная оценка динамики ПОН в течение ранней фазы заболевания выявила, что на протяжении всего исследуемого периода тяжесть ПОН в группах статистически достоверно различалась (р<0,05; рис. 1). Рисунок 1. Динамика тяжести полиорганной недостаточности у больных тяжелым острым панкреатитом.
Рисунок 1. Динамика тяжести полиорганной недостаточности у больных тяжелым острым панкреатитом.
При построении кривой выживаемости Каплана-Майера (рис. 2) Рисунок 2. Выживаемость (60-дневная) больных тяжелым острым панкреатитом. также констатированы статистически значимые различия в группах (р=0,000). Следует отметить, что в группе больных без ранней ПОН не было ни одного летального исхода в первые 14 дней госпитализации.
Рисунок 2. Выживаемость (60-дневная) больных тяжелым острым панкреатитом. также констатированы статистически значимые различия в группах (р=0,000). Следует отметить, что в группе больных без ранней ПОН не было ни одного летального исхода в первые 14 дней госпитализации.
На фоне интенсивной терапии в реанимационном отделении состояние 46 больных ТОП без ранней ПОН стабилизировалось уже в течение первых 2 сут госпитализации. Летальные исходы были обусловлены гнойно-септическими осложнениями на 3-й неделе заболевания и позднее (тяжелый сепсис, септический шок, арозионные кровотечения).
В группе с ранней сохраняющейся или прогрессирующей ПОН 48% (из умерших) больных умерли в течение 1-й недели заболевания.
Таким образом, от своевременного выявления больных с высоким риском развития неблагоприятного исхода в течение ранней фазы заболевания во многом зависят эффективность проводимой интенсивной терапии и результаты лечения в целом.
Сравнительная характеристика основных показателей в группах больных ТОП без ранней ПОН и больных с прогрессирующей ПОН представлена в табл. 1.
В группе с ранней прогрессирующей ПОН отмечалось статистически достоверно более тяжелое состояние при поступлении, более длительный период нахождения в реанимационном отделении, значимо большее число больных с гнойно-септическими осложнениями. В связи с высокой ранней летальностью в этой группе больных различия в длительности госпитализации не были статистически значимы. Исходы (ранняя и госпитальная летальность) в сравниваемых группах также статистически достоверно различались.
Для верификации больных с высоким риском развития прогрессирующей ПОН в качестве критериев диагностики нами были выбраны многофакторные шкалы APACHE II, Ranson, SOFA, а также количество пораженных органов. Построение ROC-кривых для анализируемых маркеров свидетельствовало о высокой прогностической чувствительности и специфичности данных показателей (рис. 3). Рисунок 3. ROC-кривые для моделей многофакторных шкал и количества поврежденных органов.
Рисунок 3. ROC-кривые для моделей многофакторных шкал и количества поврежденных органов.
Как видно из представленных в табл. 2 данных, по степени убывания предсказательной способности моделей показатели распределись следующим образом: шкала APACHE II, затем количество поврежденных органов и шкала SOFA. Предсказательная способность шкалы Ranson была наименьшей.
данных, по степени убывания предсказательной способности моделей показатели распределись следующим образом: шкала APACHE II, затем количество поврежденных органов и шкала SOFA. Предсказательная способность шкалы Ranson была наименьшей.
Используя ROC-анализ, определили следующие критерии для выявления больных с высоким риском развития ранней прогрессирующей ПОН (показатели в баллах): APACHE II≥12 (чувствительность 0,786, специфичность 0,878), повреждение двух и более органов (чувствительность 0,816, специфичность 0,805), SOFA≥4 (чувствительность 0,709, специфичность 0,854), Ranson≥6 (чувствительность 0,583, специфичность 0,854).
Высокая ранняя (первые 14 дней) и госпитальная летальность в группе выявленных больных с прогрессирующей ПОН свидетельствует о необходимости своевременного использования у данной категории больных всего комплекса интенсивной терапии, направленной на коррекцию возникших нарушений и предупреждение фатальных осложнений.
Использование данных критериев в клинической практике позволило выявить больных ТОП с риском развития ПОН и госпитализировать их в отделение реанимации для раннего начала комплексного интенсивного лечения. Интенсивная терапия таких больных включала следующие компоненты: адекватную оксигенацию (инсуффляция увлажненного кислорода, неинвазивная или искусственная вентиляция легких), обезболивание наркотическими анальгетиками, а при сохраняющемся болевом синдроме, признаках нарастания органной недостаточности, повышении внутрибрюшного давления применяли эпидуральную анестезию.
Основой для проведения инфузионной терапии служили сбалансированные по электролитному составу бикарбонатные замещающие растворы. Из группы коллоидных растворов применяли 6% растворы среднемолекулярных гидроксиэтилкрахмалов (130/0,4), а также при наличии показаний свежезамороженную плазму. В первые 48 ч после поступления средняя скорость инфузии составляла 250-300 мл/ч.
Для оценки адекватности проводимой инфузионной терапии, особенно у больных с сердечно-сосудистой, дыхательной, почечной недостаточностью, регулярно мониторировали среднее артериальное давление, центральное венозное давление, гематокрит, объем диуреза, рентгенологические признаки гипергидратации. С целью снижения секреторной активности поджелудочной железы и профилактики развития рецидивов болевого синдрома на фоне раннего начала энтерального питания применяли октреотид. Коррекцию гипергликемии осуществляли дробным подкожным введением инсулина или непрерывной его инфузией (при постоянном контроле гликемического профиля). Для улучшения реологических свойств крови применяли гепарин в дозе 15 000 ЕД в сутки. С первых часов госпитализации проводили лечебные мероприятия для коррекции энтеральной недостаточности. С этой целью использовали назогастральную и/или назоинтестинальную интубацию как для аспирации застойного содержимого, так и для последующего введения электролитных растворов и энтерального питания. Применяли деэскалационную схему антибактериальной терапии (имипенем+циластатин) и иммунокорригирующую терапию, включавшую внутривенное введение иммуноглобулина 3-5 мл/кг/сут в течение 3 дней. Среди экстракорпоральных методов гемокоррекции на фоне интенсивной инфузионной терапии (целевой гематокрит 30-35%) использовали плазмообмен (0,7-0,8 объема циркулирующей плазмы) и постоянную вено-венозную гемофильтрацию (доза >30 мл/кг/ч).
Своевременное начало всего комплекса лечебных мероприятий позволило значимо снизить раннюю летальность (первые 14 дней госпитализации), при этом также была отмечена тенденция снижения госпитальной летальности [3, 4].
Таким образом, группой риска летального исхода в ранней фазе заболевания и в фазе гнойно-септических осложнений являлись больные тяжелым острым панкреатитом с ранней прогрессирующей полиорганной недостаточностью. Диагностические критерии данной категории больных при поступлении (показатели в баллах): тяжесть состояния по шкале APACHE II≥12, тяжесть полиорганной недостаточности по шкале SOFA≥4, повреждение двух и более органов, тяжесть острого панкреатита по шкале Ranson≥7. Наиболее значимые показатели — тяжесть состояния больного по шкале APACHE II и количество поврежденных органов/систем, оцененное по критериям шкалы SOFA.
Источник
