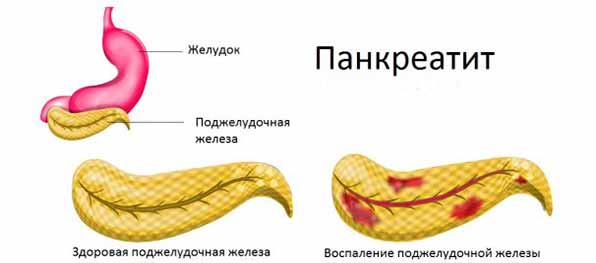
Острое жидкостное скопление что это при панкреатите

Формирование любых объемных процессов в полости внутренних органов, способствует патологическому нарушению их работоспособности и снижению уровня функциональности. Появившаяся жидкость в поджелудочной железе может свидетельствовать о развитии кистозного поражения, имеющего паралогическую полость. Скопление жидкости в полости кисты ограничивается стенками соединительных тканей. Активное формирование данной патологии ведет к интенсивному разрушению тканей поджелудочной железы, уменьшению ее уровня выработки гормонов и пищеварительных ферментов, что снижает качество жизненно-важных процессов в организме и ухудшает общее состояние пациента. Лишь своевременное выявление данной патологии и правильная постановка диагноза могут способствовать разработке наиболее эффективной схемы лечения и восстановления функциональности паренхиматозного органа.
Причины и процесс формирования кистозного поражения
Одной из основных причин, способствующих развитию кистозного поражения поджелудочной железы, является наличие панкреатической патологии острой либо хронической формы течения. При остром панкреатическом воспалении паренхиматозного органа развитие кисты возникает, примерно в 18-20% случаев, а при хронической форме панкреатита, осложнение в виде развития кисты проявляется в 45-75%. В качестве основного этиологического фактора, в большинстве случаев, выступает панкреатит на фоне алкогольной интоксикации организма.
В более редких случаях, формирование кисты может возникнуть вследствие воздействия следующих факторов:
- получения травматизации эпигастральной области живота;
- развития патологического нарушения функциональности желчного пузыря и желчевыводящих протоков;
- обострения хронической формы обструктивной панкреатической патологии с нарушениями проходимости вирсунгового протока;
- опухоль в зоне локализации дуоденального соска и сфинктера Одди;
- инвазия отдельными представителями гельминтов.
Современное общество ведущих специалистов хирургического профиля выделило 5 основных причин, способствующих развитию кистозного поражения паренхиматозного органа:
- Чрезмерный уровень потребления алкоголесодержащей продукции с высокой крепостью составляет 63% из всех случаев с поражением поджелудочной железы, ведущим к развитию кистозного образования.
- Развитие сахарного диабета, имеющего второй тип прогрессирования, составило 14%.
- Патологическое изменение метаболических процессов в организме, в комбинации с преобладанием большого количества лишних килограммов – 32%.
- Последствия хирургических вмешательств по проведению операционных мероприятий на любой части поджелудочной железы.

Рассмотрим подробнее процесс формирования кистозного поражения паренхиматозного органа при наличии панкреатической патологии. При повреждении тканевых структур железы, происходит локальное скопление лимфоцитов и нейтрофилов наряду с развитием деструктивного и воспалительного процесса. Но, пораженная область железы отделена от всей паренхимы, расположенной вокруг. В ней идет интенсивное распространение соединительных тканей и формирование грануляций, посредством чего происходит постепенное разрушение тканевых элементов в центре очага поражения клетками иммунной системы защиты, что ведет к образованию полости кисты.
При сообщении кистозного поражения поджелудочной железы с ее протоковой системой, то в сформированной кистозной полости может происходить накопление панкреатического сока, воспалительных экссудатов, а также некротических элементов тканевых структур. Если повреждаются кровеносные сосуды, то в полости развивающейся кисты идет накопление жидкости в виде крови.
В том случае, если нарушается пассаж общего панкреатического протока паренхиматозного органа, происходит формирование кистозного образования с эпителиальной выстилкой, в полости которого идет скопление панкреатического сока. В основе их патогенетического механизма образования лежит процесс внутрипротоковой гипертензии. Существует научное доказательство того, что внутреннее давление кистозной полости превосходит в трижды естественный уровень показателей внутреннего давления в протоках железы.
Классифицирование кистозных поражений паренхиматозного органа
Согласно морфологическим показателям, все разновидности кистозных поражений поджелудочной железы подразделяются на две основные типологии:
- Образовавшиеся в ходе осложнения образованные в ходе развития воспалительного заболевания паренхиматозного органа, без эпителиальной выстилки, именуемые как псевдокисты.
- Образовавшиеся при обструктивных процессах в полости протоков железы с характерной эпителиальной выстилкой, именуемые как истинные кисты, или ретенционные.
В большинстве случаев, для оценки кистозного поражения поджелудочной железы, сформировавшегося, как отягощение развития острой панкреатической патологии, используется атланское классифицирование, согласно которому выделяются следующие разновидности этой патологии:
- острое жидкостное поражение;
- подострая форма со скопившейся жидкостью;
- развитие абсцесса железы.
Резко развивающиеся кисты с острым течением, имеют не до конца сформированные стенки своей полости, в качестве которых могут быть задействованы парапанкреатическая клетчатка, панкреатические протоки и сама паренхима поджелудочной. А вот кистозные образования, сформированные при хроническом течении панкреатической патологии, обладают стенками из фиброзных и грануляционных тканевых структур.
Абсцессом же называют полость, заполненную гнойным содержимым, образовавшимся при развитии панкреонекроза либо нагноения кистозного поражения.
Кисты могут локализоваться как в области головки железы, ее тела, так и в зоне хвоста. Помимо всего прочего, выделяется также неосложненное развитие панкреатической кисты и осложненное. Осложниться кистозное поражение может развитием таких процессов, как:
- перфорация;
- нагноение;
- образование свищей;
- кровоизлияние;
- прогрессирование перитонита;
- малигнизация.

Симптоматические проявления
Симптоматика прогрессирования кистозного поражения поджелудочной железы может быть абсолютно различной в зависимости от провоцирующего фактора, зоны локализации, а также внешних параметров и размеров кисты.
Очень часто бывают случаи, когда развитие панкреатической кисты не способствует проявлению какого-либо симптоматического признака, так как образования, имеющие диаметр, не превышающий 5,5 сантиметров, не соприкасается с рядом расположенными внутренними органами и не давит на нервные волокна, поэтому не возникает никакого дискомфортного чувства у пациента.
При приобретении кистой крупного размера, основным признаком ее наличия становится интенсивная болезненность в области эпигастрия.
Наибольшей интенсивностью болезненного проявления обладает симптоматический признак развития ложной кисты на фоне острого панкреатического заболевания либо обостренной стадии хронической патологии воспалительного характера течения, так как происходят деструктивные изменения в паренхиматозном органе. С течением времени, активность болезненных проявлений стихает, болевой синдром приобретает тупой характер проявления, а может остаться и вовсе только чувство легкого дискомфортного ощущения.
В некоторых случаях, на фоне маловыраженных симптоматических проявлений, могут развиться приступы боли, вызванные внутрипротоковой гипертензией. Появление резкой выраженной боли может свидетельствовать о прорыве кистозного образования. Постепенный характер усиления болевого синдрома на фоне повышенной температуры тела и признаков интоксикации организма, могут свидетельствовать о нагноении кисты.
Существенные отличия симптоматических признаков кистозного поражения паренхиматозного органа проявляются в случаях сдавливания им солнечного сплетения. Происходит проявление выраженной жгучей боли с постепенной иррадиацией в область спины, с увеличением интенсивности проявления даже от тесной одежды. Облегчить состояние больного поможет коленно-локтевой позы, а лечение проявлений боли производится посредством наркотических анальгетиков.
Симптоматическими признаками данной патологии могут выступать следующие проявления:
- чувство тошноты;
- отхождение рвотных масс;
- слабость во всем организме
- потеря сознания
- сухость слизистых поверхностей ротовой полости
- учащение позывов к мочеиспускательному акту и числа испражнений мочевого пузыря;
- возможные потери сознания;
- развитие диареи либо запора.

Прогрессирующая стадия кисты может способствовать возникновению синдрома сдавленности рядом расположенных органов.
Методы лечения
Консервативное лечение данной патологии возможно, если состояние пациента соответствует следующим требованиям:
- имеется четкое ограничение патологического очага;
- небольшие размеры патологии, не более 2-х см в диаметре;
- единичное образование;
- отсутствие болезненности и признаков желтухи.
В остальных случаях требуется лишь оперативное лечение путем хирургического вмешательства.
В первые два дня лечение заключается в соблюдении голодной диеты, а в последующем идет полное ограничение употребления жареных и соленых блюд, а также пищи с высоким процентом жирности и остроты. Это обусловлено тем, что подобные продукты питания способствуют стимуляции секреторных возможностей поджелудочной железы и повышение интенсивности разрушительных процессов в тканевых структурах данного органа.
После госпитализации, больному назначается 10-ти дневный постельный режим с полным исключением употребления алкоголесодержащих напитков и табакокурения.
Медикаментозное лечение заключается в назначении антибактериальных препаратов из ряда тетрациклинов и цефалоспоринов, действие которых направлено на оказание профилактического эффекта от проникновения бактериальных микроорганизмов инфекционной природы в полость кистозного поражения и наполнения ее гнойным содержимым. При отсутствии применения данных медикаментов может развиться процесс расплавления стенок кисты и ее моментального распространения по всей полости рассматриваемого органа и на соседние ткани.
Купировать боль и уменьшить скорость секреторной функциональности поджелудочной железы могут помочь ингибиторы протонной помпы, среди которых наибольшей эффективностью отличаются такие медикаментозные препараты, как:
- Рабепразол;
- Омез;
- Омепразол.
Для нормализации пищеварительного тракта, назначаются лекарственные средства, в состав которых входят два активных компонента, такие как липаза и амилаза, но нет желчных кислот. К числу таких препаратов относится Креон и Панкреатин.
Важно понимать, что при отсутствии положительной динамики консервативного лечения на протяжении 4-х недель, необходимость проведения хирургического вмешательства по ликвидации данной патологии становится первостепенной задачей, требующей немедленного исполнения.
Кистозное поражение паренхиматозного органа является сравнительно редким патологическим процессом, но, не смотря на это, все симптоматические признаки данного заболевания, способствуют заметному ухудшению качества жизни больного. Поэтому так необходимо своевременное ее выявление и разработка наиболее эффективной схемы лечения. Вовремя обнаружив данную патологию, есть все шансы на выздоровление без применения хирургического вмешательства.
Список литературы
- Калинин А.В. Нарушение полостного пищеварения и его медикаментозная коррекция. Клинические перспективы гастроэнтерологии, гепатологии. 2001 г. №3, стр.21–25.
- Коротько Г.Ф. Секреция поджелудочной железы. М.: «ТриадаХ» 2002 г. стр. 223.
- Кучерявый Ю. А., Маев И. В. Болезни поджелудочной железы. В 2 томах (комплект из 2 книг) Медицина, Шико М. 2008 г.
- Решетников Е.А., Бачилов В.П., Малиновский Н.Н. и др. Клиника и лечение деструктивного панкреатита. Хирургия. 1998 г. № 6 стр. 81–84.
- Хендерсон Д.М. Патофизиология органов пищеварения. М. СПб. Бином-Невский Диалект, 1997 г.
- Бойко Ю. Г. Патологическая анатомия и патогенез острого панкреатита. Минск, 1970 г.
Источник
Введение. Острый панкреатит является заболеванием с высоким уровнем летальности, особенно при возникновении синдрома системного воспалительного ответа и полиорганной дисфункции. Клиническое течение острого панкреатита может быть разнообразным — от легкого до тяжелого, угрожающего жизни. После инициации заболевания тяжесть патологического процесса обусловлена сложной цепью медиаторов воспаления, такими как цитокины, протеолитические ферменты, свободные радикалы кислорода, фрагменты комплемента, эйкозаноиды, которые способствуют переходу местного повреждения к системному процессу с возникновением полиорганной дисфункции, сепсиса.
Появление панкреатогенного асцита и парапанкреатические скоплений жидкости является характерным проявлением острого деструктивного панкреатита [6]. Экспериментальные исследования показывают, что панкреатогенный асцит способствует нарастанию тяжести полиорганной дисфункции [2]. Панкреатогенная жидкость (ПАЖ — панкреатит- ассоциированная жидкость) повышает сосудистую проницаемость в различных органах. Этот эффект частично осуществляется через экспрессию молекул адгезии, в частности, IСАМ-1. Было показано, что экспрессия молекул адгезии индуцируется in vitro в сосудистом эндотелии панкреатогенной жидкостью [4]. Satake K. с соавт. [5] показали, что интраперитонеальная инъекция ПАЖ приводит к гистологическим изменениям в легких и повышает летальность, а Denham W. с соавт. [1], что ее введение индуцирует острый респираторный дистресс-синдром вследствие активации фактора некроза опухолей (ФНО) и интерлейкина-1 (ИЛ-1). ПАЖ может также вызвать гепатоцеллюлярную дисфункцию [7].
Целью работы было определение влияния ПАЖ на органную дисфункции при остром панкреатите.
Материалы и методы. Работа основывается на проспективном обследовании 267 больных острым панкреатитом. Диагноз острого панкреатита (ОП) устанавливали на основании анамнеза, объективного обследования, результатов лабораторного, рентгенологического, ультрасонографического (УСГ) обследований, компьютерной томографии (КТ).
В формулировке диагноза использовали Международную классификацию острого панкреатита, принятую в Атланте (США) в 1992 г. Согласно Международной классификации легкое течение панкреатита верифицировано у 126 (47,2%) больных, тяжелое — у 141 (52,8%). Тяжелое течение устанавливали при органной дисфункции, после обнаружения при УСГ, КТ некротических изменений в поджелудочной железе, скоплений жидкости в парапанкреатических участках или в свободной брюшной полости, наличия парапанкреатического инфильтрата.
Мужчин было 188 (70,4%), женщин — 79 (29,6%). Возраст больных был в пределах от 17 до 87 лет и в среднем составил 43,3 ± 0,9 года. Основным этиологическим фактором заболевания был алкоголь у 178 (66,7%) больных, в частности, у 96 (68,1%) больных с тяжелым ОП и у 82 ( 65,1 %) — легким.
Острый билиарный панкреатит (ОБП) диагностирован у 65 (24,3%) пациентов, среди них — у 36 (55,4%) больных был отечный панкреатит и у 29 (44,6%) — некротический. У одного (0,4%) больного верифицирован острый посттравматический панкреатит, возникший в результате закрытой травмы живота, у 23 (8,6%) больных причину ОП установить не удалось.
С помощью соответствующих стандартных наборов фирмы Eagle Diagnostics (США ) на анализаторе Technicon RA- 1000 определяли активность в сыворотке крови лактатдегидрогеназы, АсАТ, АлАТ, -глютамилтранспептидазы, щелочной фосфатазы, амилазы.
При обследовании части больных ОП также определяли уровень цитокинов (ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-18). Для исследования использовали стандартные коммерческие наборы фирм Boehringer Mannheim (ФРГ), R&D System GmbH (ФРГ), MBL (Япония), Diaclone (Франция) с определением на анализаторах COBAS EIA („Roche”, Франция) и Fascan Flow Cytometry („Becton Dickinson”, США).
Статистическую обработку показателей проводили с помощью стандартных компьютерных программ (Statistica Version 6, StatSoft, Inc.) с определением среднего арифметического (Х), ошибки среднего арифметического (m). Разницу между показателями вычисляли по Student, Mann-Whitney или критерию χ 2 Pearson и считали достоверной при р
Результаты и обсуждение. У 57 (45,2%) больных острым интерстициальным панкреатитом при ультрасонографическом исследовании визуализировали наличие незначительного количества жидкости в парапанкреатических участках или свободной брюшной полости. Парапанкреатическая жидкость обнаружена у 56 (44,4%) пациентов, у четырех (3,2%) — в брюшной полости. Сочетанное расположение диагностировано у трех (2,4%) больных.
При тяжелом течении острого панкреатита парапанкреатическая, чаще всего в сальниковой сумке, жидкость диагностирована у 120 (85,1%) больных, в брюшной полости — у 83 (58,9%). Их сочетанная визуализация обнаружена у 74 (52,5%) больных. Таким образом, свободную жидкость при остром панкреатите обнаружено у 129 (91,5%) больных с некротической формой.
Следовательно, наличие свободной жидкости в парапанкреатических участках и свободной брюшной полости достаточно характерно для острого деструктивного панкреатиχта ( 2 = 48,97, p
2 = 93,94, p
Мы отметили, что наличие жидкости в парапанкреатических зонах, сальниковой сумке и в свободной брюшной полости достоверно коррелирует с наличием системных осложнений, в частности легочных, у больных острым панкреатитом, что может свидетельствовать о роли панкреатического выпота в патогенезе органной дисфункции у этих пациентов.
Исследования, преимущественно экспериментальные, свидетельствуют, что панкреатогенный асцит и парапанкреатические скопление жидкости, в частности в сальниковой сумке, содержат многочисленные медиаторы, которые причастны к развитию повреждений в отдаленных органах и системах. Панкреатогенный асцит вызывает активирование NF-κB, который вовлечен в высвобождение многих цитокинов.
Было проведено определение различных цитокинов у больных с тяжелым течением острого панкреатита в жидкости, которую получали при пункции брюшной полости под контролем ультрасонографии. Отмечено, что в панкреатогенном асците содержится высокий уровень провоспалительных цитокинов, в частности ИЛ-1β, ИЛ -6 и ИЛ-18. Одновременно концентрации интерлейкинов 1β и 18 существенно превышали их содержание в сыворотке крови (Таб.1).
Таблица 1
Таб.1.Уровни провоспалительных цитокинов в ПАЖ и сыворотке крови больных тяжелым острым панкреатитом (Х±m)
Итак, ПАЖ может способствовать поддержанию патологического процесса в поджелудочной железе, локальным и системным осложнениям. ПАЖ сама экспрессирует in vitro молекулы адгезии, такие как ICAM-1 и VCAM-1 [4], в сосудистом эндотелии, повышает экспрессию ИЛ-6 и ИЛ-8 в сосудистом эндотелии и мононуклеарных лейкоцитах [3] через активирование NF-κB. В эксперименте интраперитонеальная инъекция ПАЖ вызывает повреждение легких и снижает выживаемость [2]. ПАЖ активирует NF-κB и повышает экспрессию ФНО-α и ИЛ-1β в легких.
Поэтому в комплексное лечение больных некротическим панкреатитом мы считали целесообразным включение эвакуации ПАЖ. Удаление ПАЖ осуществляли с помощью пункций или катетеризации под контролем ультрасонографии, лапароскопического дренирования брюшной полости.
Небольшие скопления жидкости, особенно у больных отечным панкреатит, как правило, не требуют дополнительных вмешательств и исчезают после ликвидации воспалительного процесса в поджелудочной железе после проведенной адекватной терапии.
При легком течении острого панкреатита было выполнено только одно одномоментное пункционное удаление жидкости из сальниковой сумки в количестве 150,0 мл.
У больных деструктивным панкреатитом эвакуацию воспалительной панкреатогенной жидкости проводили 40 больным, из них тринадцати при лапароскопическом дренировании. За один раз удаляли от 100 мл жидкости до 4 л панкреатогенного асцита.
Контролированное исследование провели у 47 больных. Удаление ПАЖ было осуществлено у 31 больного острым деструктивным панкреатитом, контрольной группой служили 16 больных. В асцитической жидкости и сыворотке крови у больных определяли ИЛ-1β, ИЛ -6, ИЛ-8, ИЛ-18 во время лечения (Рис.1). В начале лечения концентрация многих интерлейкинов была выше в ПАЖ, чем в сыворотке крови.
Рис.1. Концентрации ИЛ-6, ИЛ-8, ИЛ-18, ИЛ-1β у больных острым некротическим панкреатитом.
Эвакуация экссудата улучшала общее состояние больного, уменьшала явления интоксикации (уменьшалась частота пульса, снижался лейкоцитоз и т.д.). У пациентов контрольной группы отмечено постепенное повышение уровней провоспалительных медиаторов в течение недели (рис.2), что коррелировало с появлением и прогрессированием органных осложнений, в частности, легочных, у 6 (37,5%) больных.
Рис.2. Динамика сывороточных концентраций ИЛ-6, ИЛ-8, ИЛ-18, ИЛ-1β у больных острым некротическим панкреатитом (контрольная группа).
У пациентов основной группы уровень циркулирующих медиаторов снижался уже на следующий день после удаления ПАЖ (рис.3), а появление и ухудшение полиорганной дисфункции констатировано только у 4 (12,9%) из них (χ2 = 3,81, р = 0,050).
Рис.3. Динамика сывороточных концентраций ИЛ-6, ИЛ-8, ИЛ-18, ИЛ-1β у больных острым некротическим панкреатитом после удаления ПАЖ.
Несмотря на одинаковую консервативную терапию, у 10 (62,5%) пациентов контрольной группы отмечено дальнейшее прогрессирование некротических изменений, что проявлялось при КТ: распространение зоны некроза, появление дополнительных парапанкреатических скоплений жидкости, что завершалось инфицированием панкреатических некрозов. В опытной группе инфицирование констатировано у 6 (19,4%) больных (χ2 = 8,75, р = 0,0031).
В общем проведено 40 эвакуаций парапанкреатической жидкости или панкреатогенного асцита у больных тяжелым острым панкреатитом. Надо отменить, что после этого только 6 (15%) больных нуждались в хирургическом вмешательстве по поводу инфицирования панкреатических некрозов или панкреатических и парапанкреатических абсцессов. У больных, у которых удаление панкреатогенной жидкости не проводили, открытые операционные вмешательства осуществлены у 41 из 89 (46,1%) пациентов. Таким образом, своевременная ликвидация панкреатогенных скоплений жидкости благотворно влияет на течение заболевания за счет своеобразной профилактики гнойных осложнений ОП (χ2 = 11,50, р = 0,0007).
Для изучения токсического воздействия панкреатит-ассоциированной жидкости была изучена эффективность удаления ПАЖ на функциональное состояние печени и почек. При этом определяли активность трансаминаз и концентрацию креатинина в сыворотке крови до и через 7-10 дней после эвакуации ПАЖ. Контрольные исследования проведены у больных, у которых эту процедуру не проводили. Отмечено, что после эвакуации ПАЖ значительно быстрее улучшалась функция печени и почек (Табл.2). Это свидетельствует о целесообразности данной манипуляции для улучшения течения заболевания у больных острым некротическим панкреатитом.
Таблица 2 Таб.2.Активность трансаминаз и концентрация креатинина в сыворотке крови больных острым панкреатитом при удалении
ПАЖ (Х±m)
Вывод
Эвакуация панкреатогенной жидкости у больных острым панкреатитом улучшает общее состояние пациентов, уменьшает явления интоксикации. При этом уже на следующий день после удаления ПАЖ снижается уровень циркулирующих провоспалительных медиаторов. Своевременная ликвидация панкреатогенных скоплений жидкости благоприятно влияет на течение заболевания за счет уменьшения местных и системных осложнений острого панкреатита, улучшения функционального состояния печени и почек.
1. Denham W., Yang J., Norman J. Evidence for an unknown component of pancreatic ascites that induces adult respiratory distress syndrome through an interleukin-1 and tumor necrosis factor-dependent mechanism // Surgery. – 1997. – Vol.122. – P.295-301.
2. Fujita M., Masamune A., Satoh A. et al. Ascites of rat experimental model of severe acute pancreatitis induces lung injury // Pancreas. – 2001. – Vol.22. – P.409–418.
3. Masamune A., Shimosegawa T., Fujita M. et al. Ascites of severe acute pancreatitis in rats transcriptionally up-regulates expression of interleukin-6 and -8 in vascular endothelium and mononuclear leukocytes // Dig. Dis. Sci. – 2000. – Vol.45. – P.429-437.
4. Masamune A., Shimosegawa T., Kimura K. et al. Specific induction of adhesion molecules in human vascular endothelial cells by rat experimental pancreatitis-associated ascitic fluids // Pancreas. – 1999. – Vol.18. – P.141-150
5. Satake K., Koh I., Nishiwaki H. et al. Toxic products in hemorrhagic ascitic fluid generated during experimental acute hemorrhagic pancreatitis in dogs and a treatment which reduces their effect // Digestion. – 1985. – Vol.32. – P.99-105.
6. Tsiotos G.G., Sarr M.G. Management of fluid collections and necrosis in acute pancreatitis // Curr. Gastroenterol. Rep. – 1999. – Vol.1. – P.139-144.
7. Ueda T., Ho H.S., Anderson S.E. et al. Pancreatitis-induced ascitic fluid and hepatocellular dysfunction in severe acute pancreatitis // J. Surg. Res. – 1999. – Vol.82. – P.305-311.
Источник