Можно тенотен принимать при язве желудка
Комментарии
В.В. Цуканов – д.м.н., проф., руководитель гастроэнтерологического отделения ГУ НИИ МПС СО РАМН
Е.Ю. Куперштейн – н.с., гастроэнтерологического отделения ГУ НИИ МПС СО РАМН, к.м.н.
В.Н. Шарыпова – врач гастроэнтерологического отделения ГУ НИИ МПС СО РАМН Красноярск
В настоящее время принято рассматривать язвенную болезнь как мультифактериальное заболевание, которое наиболее адекватно описывает теория весов, на которых находятся агрессивные и защитные факторы. Среди агрессивных факторов наибольшее значение придается инфекции Helicobacter pylori и кислотопродукции в желудке (1). Значительная роль Helicobacter pylori в возникновении язвенной болезни подтверждена присуждением Нобелевской премии в области медицины за 2005 г. австралийским ученым R. Warren и B. Marshall и рядом международных консенсусов по Helicobacter pylori-ассоциированным заболеваниям (2).
Вместе с тем, возвращаясь к многофакторности патогенеза язвенной болезни, в настоящее время принято относить к реальным компонентам патогенеза язвенной болезни его психосоматические аспекты. Исторически основоположником неврогенной концепции развития язвенной болезни является G. Bergman (1913). В 1952 г. К.М. Быков и И.Т. Курцин предложили кортико-висцеральную теорию патогенеза язвенной болезни, которая сейчас утратила свое значение в связи с недостаточным вниманием к гормональному звену регуляции, биохимическим процессам в организме и фактическим клиническим данным.
В настоящее время взаимосвязь язвенной болезни и нейроэндокринной сферы принято рассматривать в контексте психосоматической медицины. Современная психосоматическая медицина изучает взаимоотношения и взаимосвязи между эмоциональной жизнью человека и природой его соматических расстройств, значение индивидуальных факторов психики и окружающей среды в этиологии заболеваний. При этом она исходит из того, что условия жизни индивидуума в прошлом и настоящем, его эмоциональная жизнь могут оказать существенное влияние на функции внутренних органов. Не придавая психогенным воздействиям значения единственного и решающего фактора в этиологии соматических заболеваний, психосоматическая медицина поддерживает концепцию полиэтиологичности заболеваний человека (3).
Язвенную болезнь следует рассматривать как типичный пример психосоматического заболевания, при котором психо-эмоциональные и психосоциальные факторы играют существенную роль, предшествуя и способствуя образованию язвенного дефекта в желудке или двенадцатиперстной кишке (4, 5). Вместе с тем психические детерминанты являются лишь ко-факторами, которые приобретают причинное значение только при их сочетании с генетическими, внешнесредовыми (Helicobacter pylori), иммунными и местными факторами, реализующими развитие болезни (6, 7, 8).
Материал и методы. В исследование включены 102 больных с Helicobacter pylori-позитивной язвенной болезнью двенадцатиперстной кишки.
Все больные находились на лечении в течение 3 недель в гастроэнтерологическом отделении клиники ГУ НИИ медицинских проблем Севера СО РАМН и получали стандартное лечение, включавшее Омепразол – 20 мг х 2 раза в день, Маалокс в стандартной дозе и эрадикацию Helicobacter pylori по семидневной схеме с применением антибактериальных препаратов Кларитромицина 0,5 г х 2 раза в день и Амоксициллина – 1,0 г х 2 раза в день. Курс лечения составил 3 недели. Всем пациентам проводилась эзофагогастродуоденоскопия («Olympus-10») непосредственно перед госпитализацией, через 10 и 20 дней после начала стационарного лечения. При описании результатов ЭФГДС различали язву двенадцатиперстной кишки с описанием формы, размеров, локализации (луковица или нисходящая часть дуоденум), стадии заболевания (открытая язва, красный рубец, белый рубец). Наличие Helicobacter pylori определяли морфологическим и уреазным методами (9).
Динамика клинической симптоматики оценивалась ежедневно и регистрировалась в специальных анкетах. 49 больных (27 мужчин, 22 женщины), составивших группу А, дополнительно к основной терапии получали препарат Тенотен с противотревожной активностью (производство «Материа-Медика», Россия) в дозе 2 т х 3 раза в день. 53 пациента (29 мужчин, 24 женщины), составивших группу В, получали только стандартную терапию и не принимали Тенотен. Средний возраст пациентов в группе А составил 42,3 + 2,81 года, в группе В – 41,8 + 2,36 года. Уровень тревожности у всех больных в группах А и В оценивался в начале лечения, через 10 и 20 дней от начала лечения при помощи шкалы Цунга (субъективная оценка) и шкалы Гамильтона (объективная оценка).
Результаты и обсуждение. Наиболее значительная динамика в уровне тревожности была получена у пациентов группы А при использовании шкалы Гамильтона. В группе В через 20 дней от начала лечения уровень тревожности пациентов также снижался, что может быть объяснено положительной клинической динамикой при заживлении язвенных дефектов. Но при этом уровень тревожности как через 10 дней, так и через 20 дней от начала лечения в группе А был достоверно ниже, чем у пациентов в группе В (табл. 1).
Таблица 1
Оценка тревоги
| 1. Начало лечения | 2. Через 10 дней | 3. Через 20 дней | р | |
|---|---|---|---|---|
| по шкале Цунга | ||||
| Группа А n=49 | 48,29+4,06 | 40,54+3,39 | 37,43+3,12 | 1-2=0,1 -3=0,03 |
| Группа В n=53 | 47,61+3,9 | 44,37+3,6 | 41,19+3,24 | 1-2=0,5 1-3=0,2 |
| р | =0,9 | =0,4 | =0,4 | |
| по шкале Гамильтона | ||||
| Группа А n=49 | 23,43+1,8 | 14,93+1,26 | 10,5+0,98 | 1-2=0,0001 1-3<0,001 |
| Группа В n=53 | 24,15+1,9 | 20,62+1,7 | 17,4+1,1 | 1-2=0,2 1-3=0,002 |
| р | =0,8 | =0,007 | <0,001 | |
При использовании шкалы Цунга в группе А регистрировалось достоверное снижение уровня тревожности через 20 дней от начала лечения. В группе В не было зафиксировано значимого уменьшения уровня тревожности в процессе лечения (табл. 1). Таким образом мы получили результаты, свидетельствующие о различиях динамики уровня тревожности в группах А и В.
Мы проанализировали динамику купирования болевого синдрома в группах А и В. Боли в эпигастральной области до начала лечения регистрировались в 98,0% случаев в группе А и в 98,1% случаев в группе В. Через 10 дней лечения болевой синдром сохранялся у 10,2% пациентов в группе А и у 37,7% пациентов в группе В (р=0,001). Через 20 дней от начала лечения эти показатели составили, соответственно, 0% и 1,9% (р=0,3).
Через 10 дней лечения язвенные дефекты были обнаружены у 30,6% пациентов в группе А и у 41,5% пациентов в группе В (р=0,3). Через 20 дней лечения эти показатели составили, соответственно, – 0% и 1,9% (р=0,3).
Следует заметить, что различные аспекты психо-эмоционального статуса ранее исследовались у пациентов с язвенной болезнью. У больных язвенной болезнью чаще, чем при других психосоматических заболеваниях устанавливалось наличие психопатических нарушений, состояния эмоциональной напряженности, ипохондрии, пессимизма, отчужденности или, напротив, повышенной потребности в эмоциональной привязанности со стороны окружающих, прежде всего, членов семьи (10). При оценке «усредненного профиля личности» с помощью Миннесотского личностного теста Ф.И. Комаров и соавт. выяснили, что особенностью пациентов с язвенной болезнью является выраженный психовегетативный синдром, характеризующийся ипохондрическими и тревожнодепрессивными чертами личности, преимущественным повышением реактивного личностного уровня тревоги (11). Повышенный уровень тревожности у пациентов с язвенной болезнью отмечают также Е.Н. Ревенюк и соавт. (12). Э.И. Белобородова и соавт. при помощи шкалы Спилбергера-Ханина и Сокращенного многофакторного опросника личности (СМОЛ), подтвердили, что у лиц с язвенной болезнью выше уровень тревожности, пессимистичности, импульсивности и эмоциональной лабильности (13).
Резюмируя итоги нашего исследования, необходимо подчеркнуть, прежде всего, повышенный уровень тревожности у пациентов с обострением язвенной болезни, что, с одной стороны, совпадает с результатами ранее выполненных исследований, а, с другой стороны, само по себе указывает на целесообразность применения противотревожных препаратов в комплексной терапии. Весьма важным представляется также отчетливо более быстрая динамика снижения уровня тревожности и частоты болей в эпигастральной области при применении Тенотена в сравнении с контрольной группой, что позволяет повысить комплаентность контактов с больным и улучшить качество жизни пациентов. Все это, наряду с практически полным отсутствием побочных эффектов, позволяет рекомендовать Тенотен для активного использования в комплексной терапии пациентов с язвенной болезнью.
Список литературы:
- Peura D.A. Ulcerogenesis: integration the roles of Helicobacter pylori and acid secretion in duodenal ulcer / D.A. Peura // Am. J. Gastroenterol. – 1997. – V.92, N4. – P.8 – 13.
- Malfertheiner P., Megraud F. et al. Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report // Gut. – 2007. – V.56. – P.772-781;
- Маев И.В., Барденштейн Л.М., Антоненко О.М., Каплан Р.Г. Психосоматические аспекты заболеваний желудочно-кишечного тракта. Клиническая медицина. – 2002. – Т.80, №11. – С.8-13.
- Вейн А.М. Идеи невризма в гастроэнтерологии // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. – 1997. – №3. – С. 76-79.
- Adami H.-O., Bergstrom R., Nyren O. et al. Is duodenal ulcer really a psychosomatic disease? // Scand. J. Gastroenter. – 1987. – V.22, N 7. – P.889-896.
- Миронычев Г.Н., Логинов А.Ф., Калинин А.В. Психосоматические аспекты язвенной болезни // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. – 1996. – №3. – С. 35-40.
- Magni G. Di Mario F., Aggio L., Borgherini G. Psychosomatic factors and peptic ulcer disease // HepatoGastroenterol. – 1986. – V.33, N3. – P.131-137.
- Циммерман Я.С., Белоусов Ф.В. Психосоматическая медицина и проблема язвенной болезни // Клиническая медицина. – 1999. – Т.77, №8. – С.9-15.
- Лапина, Т.Л. Основные принципы диагностики Helicobacter Pylori / Т.Л. Лапина // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. – 1999. – №2. – С. 41 – 45.
- Craig N.K.J., Boardman A.P. Common mental health problems in primary case // Brit. Med. J. – 1997. – V.314, N31. – P.1609-1612.
- Комаров Ф.И., Вейн А.М. и др. Психовегетативные нарушения у больных язвенной болезнью двенадцатиперстной кишки в различные сезоны года // Клин. мед. – 1985. – №9. – С.36-41.
- Ревенюк Е.Н., Завилянская Л.И. и др. Психологическое исследование личностных особенностей больных психосоматическими заболеваниями // Врач. дело. – 1979. – №8. – С.97-100.
- Белобородова Э.И., Ласточкина Л.А., Плотникова Е.Ю., Наумова Е.Л. Вегетативные и психосоматические расстройства при заболеваниях органов пищеварения. – Кемерово, 2004. – 144 с.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Комментарии
В.И. Симаненков, Е.Г. Порошина, С.В.Тихонов, О.И. Соловьева, кафедра терапии и клинической фармакологии Санкт-Петербурской медицинской академии последипломного образования, г. Санкт-Петербург
Актуальность функциональных нарушений билиарной зоны отражена в Римском консенсусе, 1999, где принят термин «дисфункциональные расстройства билиарного тракта». Независимо от этиологии выделяют два типа расстройств: дисфункцию желчного пузыря и дисфункцию сфинктера Одди (4). В Международной классификации болезней (МКБ-10) в рубрику К82.8 включена «Дискинезия пузырного протока или желчного пузыря», а в рубрику К83.4 – «спазм сфинктера Одди». Характер функциональных нарушений и разнообразие клинической симптоматики связаны как со сложностью анатомического строения этого отдела пищеварительной системы, так и с особенностями нейрогуморальной регуляции (2).
Распространенность дисфункциональных расстройств билиарного тракта изучена мало (3). Эпидимиологические данные отсутствуют. Однако, по данным Римской группы по изучению этиологии и предупреждению холелитиаза, частота желчной колики при скрининговых обследованиях населения, у которых, по данным ультразвукового исследования, была исключена желчнокаменная болезнь, составила 7,6% у мужчин и 20,7% у женщин (5).
Традиционно терапия этих состояний помимо спазмолитиков, холеретиков и холикинетиков включает назначение психотропных средств(1). В зависимости от выраженности психопатологической симптоматики, назначаются анксиолитики, антидепрессанты в том числе растительные.
Для данного исследования был выбран отечественный препарат Тенотен. В инструкции Тенотен определяется как препарат, оказывающий анксиолитическое, антидепрессивное, антиастеническое действие, что позволяет его классифицировать, как дневной анксиолитик. Эффект Тенотена определяется модулирующим воздействием на биологическую активность мозгоспецефического белка S 100. Доказано участие этого белка в формировании нарушений эмоциональной сферы. Тенотен имеет высокий уровень безопасности, реализованный в отсутствии противопоказаний и побочных действий, присущих другим анксиолитикам.
Препарат тенотен не изучался у пациентов с дисфункциональными расстройствами билиарного тракта.
На кафедре терапии и клинической фармакологии было проведено клиническое исследование, целью которого являлось:
- изучение влияния препарата Тенотен на редукцию тревожной симптоматики у пациентов с дискинезиями желчевыводящих путей
- изучение характера влияния препарата Тенотен на соматическую симптоматику (боли, изжогу, отрыжку и горечь во рту) у этой категории больных
- изучение влияния препарата Тенотен на моторику желчевыводящих путей.
В исследование был включен 41 больной. Основную (1) группу составили 21 пациент с верифицированным диагнозом гипомоторная дискинезии желчевыводящих путей. Пациенты основной группы соблюдали диету, получали соматотропную терапию и препарат Тенотен (6–3 таблетки/сутки). Рандомизация проводилась методом «случайной выборки».
2 группа (контрольная) – 20 человек, с диагнозом гипомоторная дискинезия желчевыводящих путей, соблюдали диету и получали только идентичную соматотропную терапию, включавшую: дротаверин внутрь при болях, экстракт артишоков в дозе 200 мг 3 раза в день 4 недели.
Критерии включения:
- больные с 18 до 65 лет
- верифицированный диагноз гипомоторной дискинезии желчевыводящих путей
- наличие тревожно-фобических расстройств (генерализованное тревожное расстройство, смешанное тревожнодепрессивное расстрой ство, неврастения)
Критерии исключения:
- диффузные заболевания печени;
- острый панкреатит;
- обострение язвенной болезни;
- алкоголизм;
- желче-каменная болезнь;
- психозы;
- тяжелая сердечная недостаточность 3–4 классов по NYHA;
- острый инфаркт и острый инсульт;
- декомпенсированные заболевания почек
Методы обследования:
- оценка клинического статуса
- стандартное биохимическое обследование
- УЗИ желчевыводящих путей с нагрузочной пробой (2 куриных яйца)
- изучение психологического статуса с помощью шкалы самооценки Спилберга-Ханина, шкалы для оценки тревоги Гамильтона, астения оценивалась по шкале астении из опросника MMPI, адаптированной Малковой Л.Д. перед исследованием и через месяц использования препарата Тенотен
- аналого-визуальная шкала оценки эффективности терапии самим пациентом и исследователем.
Обследование больных по представленной программе осуществлялось в динамике: при поступлении в стационар и через месяц от начала терапии.
Как уже отмечалось, в 1 группу был включен 21 пациент. Группа состояла из 18 женщин и 3 мужчин, возрастной интервал от 23 до 63 лет. Средний возраст пациентов 41 год, 10 человек из 21 (47%) имеют высшее образование. Дискинезией желче-выводящих путей пациенты первой группы страдали, в среднем, 13 лет. Перед началом исследования пациенты предъявляли типичные жалобы на непереносимость жирной пищи, схваткообразные или тупые боли в правом подреберье, часто связанные с приемом пищи, тошноту; изжогу; неустойчивость стула. Также у всех больных имелись личностные расстройства, в виде снижения эмоционального фона, повышенной тревожности, утомляемости. Пациенты соблюдали диету, получали препарат Тенотен в течение месяца по схеме: 2 таблетки три раза в день в течение двух недель,1 таблетка три раза в день в течение следующих двух недель. В качестве симптоматической терапии принимался экстракт артишока в дозе 200 мг 3 раза в день в течение 4 недель. Для купирования болей в животе использовался дротаверин.
Одна из пациенток после четырех дней участия в исследовании от приема препарата Тенотен отказалась, сославшись на послабление стула и забывчивость, имевшуюся уже до начала исследования. Вследствие этого, больная была исключена из исследования. Приверженность (комплайнс) пациентов в данной группе через месяц лечения составил 78 процентов. По окончании исследования пациентам было предложено оценить свое лечение при помощи десятибалльной аналого-визуальной шкалы, где 0 – это очень плохая оценка, 10 – очень хорошая. В среднем пациенты оценили эффективность своего лечения на 7 баллов. По аналогичной шкале, клиническая оценка врачом результатов лечения в среднем равнялась 8 баллам. В приложении 1 представлена таблица, отражающая динамику жалоб пациентов, данных ультразвукового исследования желчного пузыря (нагрузочная проба), психологических тестов и опросников. Боль в животе, изжога, метеоризм оценивались по десятибалльной шкале, где 0 – это отсутствие симптома, 5 – средняя, 10 – сильная выраженность симптома. Стул оценивался по Бристольской шкале.
Контрольная группа (группа 2) состояла из 20 человек, 13 женщин и 7 мужчин. Возрастной интервал от 20 до 64 лет, средний возраст 35 лет. Пять человек из десяти (50 процентов) имеют высшее образование. В среднем дискинезией желчевыводящих путей страдают около 15 лет. Жалобы, предъявляемые пациентами контрольной группы перед началом исследования, сходны с жалобами пациентов основной группы. Таким образом, в клиническом плане пациенты основной и контрольной группы достоверно не отличались. В течение одного месяца пациенты соблюдали диету, принимали экстракт артишока в дозе 200 мг 3 раза в день, препарат дротаверин по требованию. По окончании исследования пациентам было предложено оценить свое лечение при помощи десятибалльной аналого-визуальной шкалы, где 0 – это очень плохая оценка, 10 – очень хорошая. В среднем пациенты оценили успешность своего лечения на 5 баллов. По аналогичной шкале, клиническая оценка результатов лечения в среднем равна также 5 баллам. В приложении 2 представлена динамика жалоб па циентов, психологических тестов и опросников. Боль в животе, изжога, метеоризм оценивались по десятибалльной шкале, где 0 – это отсутствие симптома, 5 – средняя, 10 – интенсивная (сильная) выраженность симптома. Стул оценивался по Бристольской шкале.
Данные результатов исследования были оценены при помощи программы СТАТИСТИКА 5.5. Статистически основная и контрольная группа до исследования были однородными.
В результате проведенного лечения в основной группе, в отличие от контрольной, достоверно снизился уровень депрессии, определяемой по шкале Гамильтона, которая не получала Тенотен.
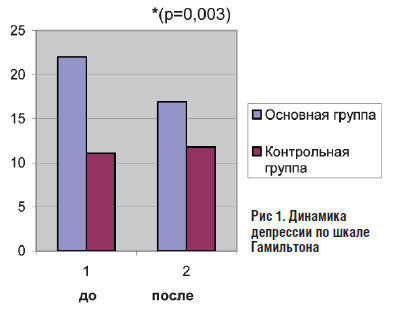
Рис 1. Динамика депрессии по шкале Гамильтона
В этой же группе достоверно снизилась реактивная тревожность по тесту Спилбергера – Ханина
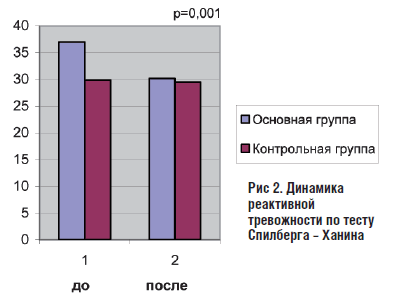
Рис 2. Динамика реактивной тревожности по тесту Спилберга – Ханина
Достоверное снижение уровня личностной тревожности по Спилберга – Ханина также отмечалось в группе, получавших Тенотен.
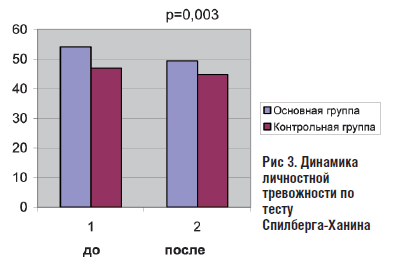
Рис 3. Динамика личностной тревожности по тесту Спилберга-Ханина
Снижение астенического синдрома наблюдалось в обеих группах и была достоверной. В основной группе снижении астении было более выраженным.
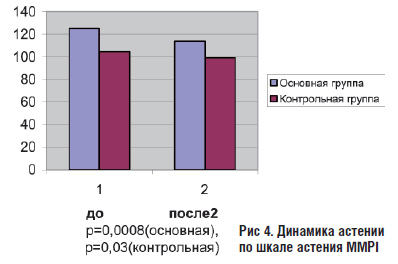 Рис 4. Динамика астении по шкале астения MMPI
Рис 4. Динамика астении по шкале астения MMPI
В основной группе, помимо коррекции психопатологической симптоматики отмечалось уменьшение таких клинических жалоб как боль в эпигастрии, отрыжка, изжога, метеоризм. В контрольной группе через месяц достоверной динамики в выраженности болевого синдрома отмечено не было. Кроме того, наблюдалось увеличение интенсивности и частоты изжоги.
Изменение стула по Бристольской шкале оказалось не достоверным(p=0,49)
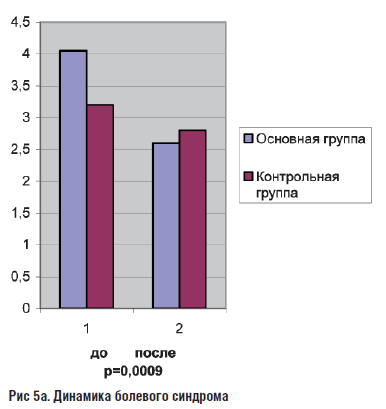
Рис 5а. Динамика болевого синдрома
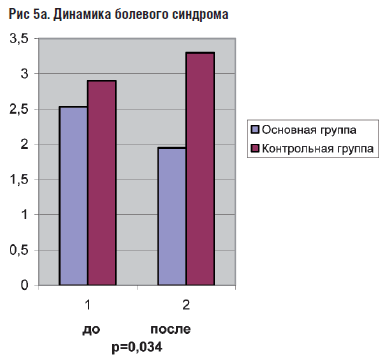
Рис 5б. Динамика интенсивности изжоги
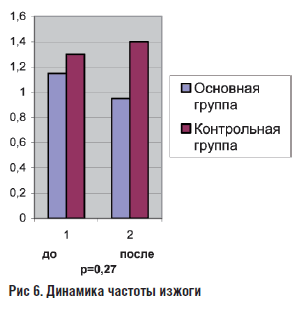
Рис 6. Динамика частоты изжоги
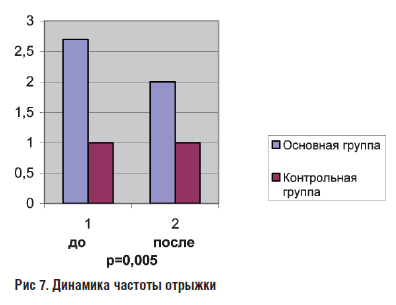
Рис 7. Динамика частоты отрыжки
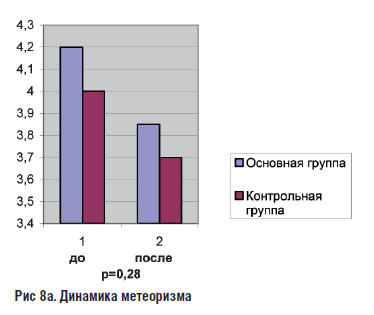
Рис 8а. Динамика метеоризма
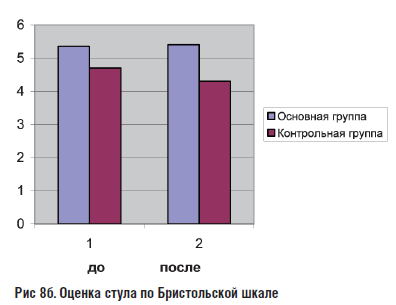
Рис 8б. Оценка стула по Бристольской шкале
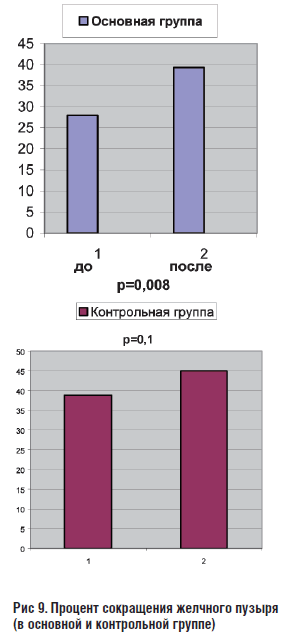
Рис 9. Процент сокращения желчного пузыря (в основной и контрольной группе)
Выводы
- Курсовая терапия Тенотеном приводит к достоверному улучшению психологического состояния пациентов, что отражается как в редукции клинической симптоматики, так и в достоверном снижении величин шкал депрессии и тревоги
- Уменьшение признаков социально-психологической дезадаптации и уменьшение клинических признаков дискинезии желчевыводящих путей, наблюдающиеся на фоне терапии Тенотеном, приводит к уменьшению выраженности астенических расстройств
- Позитивное влияние Тенотена на клиническую симтоматику, ассоциированную с нарушениями моторики верхних отделов желудочного кишечного тракта отражается в уменьшение выраженности изжоги и отрыжки
- Традиционная симптоматическая терапия не приводит к достоверным позитивным изменениям моторики желчного пузыря
- Гармонизирующее влияние Тенотена на моторику отражается в уменьшении дискинетических явлений, при одновременном усилении сократительной способности желчного пузыря и уменьшение выраженности болевого синдрома.
Приведенные данные свидетельствуют о позитивном влиянии Тенотена на течение дискинезии желчевыводящих путей у пациентов с тревожно-депрессивными личностными расстройствами. Представляется важным, что Тенотен не только позитивно влияет на психологический статус больных, но и приводит к редукции клинической симптоматики. Таким образом, имеются основания считать, что Тенотен с успехом может применяться при функциональных моторных расстройствах холангио-панкреато-дуоденальной зоны.
Литература
- Ильченко А.А. Дисфункции билиарного тракта и их медикаментозная коррекцияь http/www.gastrosait.ru.
- Калинин А.В., Буторова Л.И. Физиологические и клинические аспекты нарушений моторики тонкой кишки. Возможности фармакологической коррекции // Клин. перспективы гастроэнтерол., гепатол. – 2001. – № 4. – с. 25–34.
- Калинин А. В.Функциональные расстройства билиарного тракта и их лечение http/www.gastrosait.ru.
- Drossman D.A., Li Z., Andruzzi E. et al. US householder survey of functional gas-trointestinal dis-orders: prevalence, sociodemography and health impact
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник


