Выделяют варианты течения хронического панкреатита
Билиарнозависимый
Алкогольный
•
Дисметаболический
Инфекционный
Лекарственный
Идиопатический
2. Варианты хронического панкреатита по характеру клинического течения
Редко рецидивирующий
Часто рецидивирующий
С постоянно
присутствующей симптоматикой
3. Варианты хронического панкреатита по морфологическим признакам
Интерстициально-отечный
Паренхиматозный
Фиброзно-склеротический
(индуративный)Гиперпластический
(псевдотуморозный)Кистозный
4. Варианты хронического панкреатита по клиническим проявлениям
Болевой
Гипосекреторный
Астеноневротический
Латентный
Сочетанный
Наиболее
сложным разделом классификации является
разделение ХП
по морфологическим признакам. Авторы
в основу этих принципов положили данные
УЗИ и КТ.
Интерстициально-отечный
ХПна
высоте обострения (по данным
УЗИ и КТ) характеризуется умеренным
увеличением размеров ПЖ.
Вследствие отека собственно железы и
паренхиматозной клетчатки контуры
ПЖ визуализируются нечетко, структура
её представляется
неоднородной, встречаются участки как
повышенной, так и пониженной плотности;
отмечается неоднородная эхогенность.
По мере стихания
обострения размеры ПЖ становятся
нормальными, контуры четкими.
В отличие от острого панкреатита часть
морфологических изменений оказывается
стабильной (в большей или меньшей
степени
сохраняются участки уплотнения железы).
У большинства больных выраженных
изменений системы протоков не обнаружено.
Для
паренхиматозного варианта ХП характерна
значительная продолжительность
заболевания, чередование периодов
обострения и
ремиссии. Боли в период обострения менее
выражены, амилазный тест
оказывается положительным реже и уровень
повышения меньше.
Более чем у половины больных фиксируются
симптомы внешнесекреторной
недостаточности ПЖ: стеаторея, полифекалия,
склонность
к поносу, который относительно легко
купируется ферментными
препаратами. По данным УЗИ и КТ размеры
и контуры ПЖ существенно
не изменены, стабильно отмечается
равномерное уплотнение железы.
Изменений протоков у большинства больных
не выявляется.
Фиброзно-склеротический
вариант ХП—анамнез
продолжительный—более
15 лет. Практически у всех больных
фиксируется внешнесекреторная
недостаточность ПЖ, интенсивные боли,
не уступающие лекарственной терапии.
Исчезает четко выраженная грань между
обострением и ремиссией. Амилазный тест
в половине случаев оказывается
отрицательным. Осложнения часты, а
характер их зависит от преимущественной
локализации процесса (в головке—нарушения
пассажа желчи,
в хвосте—нарушение
проходимости селезеночной вены и
подпеченочная
форма портальной гипертензии). По данным
УЗИ и КТ—размеры
поджелудочной железы уменьшены, паренхима
повышенной эхогенности, значительно
уплотнена, контуры четкие, неровные,
нередко
выявляются обызвествления. У части
больных — расширение протоковой
системы железы.
Гиперпластический
вариант ХП—встречается
приблизительно у 5% больных. Заболевание
протекает длительно (обычно более 10
лет). Боли
носят выраженный характер и постоянны,
как правило, фиксируется
недостаточность внешнесекреторной
функции ПЖ. Иногда ПЖ может
пальпироваться; амилазный тест
положительный только у 50% больных.
По данным УЗИ и КТ—ПЖ
или отдельные её части резко увеличены.
В плане дифференциальной диагностики
с опухолью поджелудочной
железы целесообразно проведение пробы
с лазиксом, а также повторное
исследование сыворотки крови на
опухолевые маркеры.
Кистозный
вариант ХП
—
встречается в 2 раза чаще, чем
гиперпластический.
Выделяется он в отдельный вариант, так
как характеризуется
своеобразной клинической картиной —
боли умеренные, но почти
постоянные, амилазный тест, как правило,
положительный и сохраняется
продолжительное время. По данным УЗИ и
КТ—ПЖ
увеличена,
есть жидкостные образования, участки
фиброза и обызвествления,
протоки обычно расширены. Обострения
частые и не всегда имеют
«видимую» причину.
Реактивный
панкреатит — это реакция поджелудочной
железы на острую патологию, либо
обострение хронической патологии
органов, функционально,
морфологически связанных с поджелудочной
железой. Реактивный
панкреатит заканчивается при ликвидации
обострения основного
заболевания, но констатация его требует
проведения лечебных и профилактических
мероприятий, направленных на предупреждение
развития
хронического панкреатита. В качестве
хронической формы течения реактивный
панкреатит не существует и в диагноз
вынесен быть
не может.
Выделение групп
больных ХП по степени тяжести.
Легкое
течение заболевания.
Редкие
(1-2 раза в год) и непродолжительные
обострения, быстро купирующийся болевой
синдром. Функции ПЖ не нарушены. Вне
обострения самочувствие больного вполне
удовлетворительное. Снижение массы
тела не отмечается. Показатели
копрограммы в пределах нормы.
Средней
тяжести.
Обострения
3-4 раза в год с типичным длительным
болевым синдромом, с феноменом
панкреатической гиперферментемии,
выявляемой лабораторными методами
исследования. Нарушения
внешнесекреторной и инкреторной функции
поджелудочной железы
умеренные (изменение характера кала,
стеаторея, креаторея по
данным копрограммы, латентный сахарный
диабет), при инструментальном
обследовании — ультразвуковые и
радиоизотопные признаки поражения
поджелудочной железы.
Тяжелое
течение.Непрерывно
рецидивирующее течение (частые длительные
обострения), упорный болевой синдром,
выраженные диспепсические
расстройства, «панкреатические поносы»,
резкое нарушение
общего пищеварения, глубокие изменения
внешнесекреторной функции
ПЖ, развитие панкреатического сахарного
диабета, кист ПЖ. Прогрессирующее
истощение, полигиповитаминозы,
внепанкреатические обострения
(панкреатогенный выпотной плеврит,
панкреатогенная нефропатия,
вторичные дуоденальные язвы).
Клиническая
картина:
Боли в эпигастральной
области после приема пищи, иррадиирующие
в спину, которые могут продолжаться в
течение многих часов или нескольких
дней.Тошнота, рвота.
Потеря массы тела
(у 30—52% пациентов).Желтуха (у 16—33%
пациентов). Отек и развитие фиброза ПЖ
могут вызывать сдавление желчных
протоков и окружающих сосудов. Преходящая
желтуха возникает вследствие отека ПЖ
при обострениях хронического панкреатита,
постоянная—связана с обструкцией
общего желчного протока вследствие
фиброза головки ПЖ. При более легкой
обструкции наблюдается повышение
только уровня щелочной фосфатазы.Во время приступа
хронического панкреатита могут возникать
жировые некрозы, чаще поражается
подкожная клетчатка на ногах, что
проявляется болезненными узелками,
которые можно ошибочно принять за
узловатую эритему.Воспаление и
фиброз перипанкреатической клетчатки
могут приводить к сдавлению и тромбозу
селезеночной, верхней брыжеечной и
воротной вен, однако развернутая картина
портальной гипертензии наблюдается
редко.Формирование
псевдокист вследствие разрывов протоков
ПЖ, на месте предыдущего некроза ткани
и последующего скопления секрета. Кисты
могут быть бессимптомными или вызывать
боли в верхней половине живота, нередко
проявляются сдавлением соседних
органов.
Синдром
недостаточности внешнесекреторной
функции. При
длительном течении заболевания по мере
разрушения паренхимы ПЖ интенсивность
болевых приступов становится меньше
(однако продолжающийся прием алкоголя
может вызвать сохранение болей), и при
уменьшении объема функционирующей
паренхимы до 10% от нормы появляются
признаки мальабсорбции — полифекалия,
жирный стул, потеря массы тела. У пациентов
с алкогольным панкреатитом признаки
мальабсорбции возникают в среднем через
10 лет от появления первых клинических
симптомов.
Диагноз устанавливают
на основании характерного болевого
синдрома, признаков недостаточности
внешнесекреторной функции ПЖ у пациента,
регулярно принимающего алкоголь. В
отличие от острого панкреатита, при
хроническом редко наблюдается повышение
уровня ферментов в крови или моче,
поэтому если это происходит, можно
подозревать формирование псевдокисты
или панкреатического асцита Стойко
повышенный уровень амилазы в крови
позволяет сделать предположение о
макроамилаземии (при которой амилаза
образует крупные комплексы с белками
плазмы, не фильтрующиеся почками, и в
моче наблюдается нормальная активность
амилазы) или внепанкреатические источники
гиперамилаземии (табл. 2).
Таблица 2.
Внепанкреатические источники
гиперамилаземии и гиперамилазурии (по
W. В. Salt II, S. Schtnkor)
Почечная
недостаточность
Болезни слюнных
желез:
эпидемический
паротит
конкремент
радиационный
сиаладенит
Осложнения
челюстно-лицевои хирургии
Опухолевая
гиперамилаземия:
рак легкого
рак пищевода
рак яичников
Макроамилаземия
Ожоги
Диабетический
кетоацидоз
Беременность
Трансплантация
почки
Травма головного
мозга
Медикаментозное
лечение:
морфин
Болезни органов
брюшной полости:
болезни желчных
путей (холецистит, холедохолитиаз)
осложнения язвенной
болезни — перфорация или пенетрация
язв
непроходимость
или инфаркт кишечника
внематочная
беременность
перитонит
аневризма аорты
послеоперационная
гиперамилаземия
Методы визуализации
в диагностике хронического панкреатита
Рентгенография
области ПЖ.Трансабдоминальное
УЗИ (расширение протоков, псевдокисты,
кальцификация, расширение общего
желчного протока, воротной, селезеночной
вены, асцит).Эндоскопическое
УЗИ.ЭРХПГ (изменение
структуры протоков, псевдокисты).Компьютерная
томография (с внутривенным контрастированием)Сцинтиграфия с
введением гранулоцитов, меченных 99mТс
или 111Iп.
Обзорная
рентгенография
в 30-40% случаев выявляет кальцификацию
поджелудочной железы или внутрипротоковые
камни, особенно
при исследовании в косой проекции. Это
снимает необходимость
дальнейшего обследования для подтверждения
диагноза
ХП. Ультразвуковое
исследование (УЗИ)
позволяет оценить размеры
органа, расширение и неровность контура
протоков, псевдокисты. Эндоскопическая
ретроградная холангиопанкреотография
(ЭРХПГ)
позволяет выявить большую часть больных
ХП. Это исследование
дает возможность обнаружить изменения
главного панкреатического
протока и его ветвей (нерегулярное
расширение
протоков — «цепь озер»). Компьютерную
томографию (КТ) и ангиографию
обычно проводят для подготовки к
предстоящему хирургическому
вмешательству. Зоны некроза поджелудочной
железы
можно обнаружить с помощью использования
контрастирования
при КТ (отсутствие накопления контрастного
вещества), а также
с помощью новой методики — сцинтиграфии
поджелудочной
железы с введением взвеси меченых
гранулоцитов (накопление
радиоактивности в очаге некроза).
Копрологическое
исследование
является
основным
методом оценки внешнесекреторной
функции поджелудочной
железы. При выраженной
панкреатической недостаточности каловые
массы приобретают
серый оттенок, зловонный запах и жирный
вид. Увеличивается
общее количество каловых масс (в норме
масса составляет
50-225 г за сутки). Повышенное содержание
нейтрального жира
в кале — стеаторея — является показателем
выраженной экзокринной
панкреатической недостаточности.
Исследование должно
проводиться на фоне приема достаточного
количества жира пациентом
(100 г в cутки
в течение 2-3 дней до анализа), наиболее
характерно обнаружение крупных
капель (диаметром более 8 мкм).
Функциональные
тесты можно
разделить на три группы:
прямые тесты
секреции ПЖ. Проводят сбор и исследование
сока ПЖ или дуоденального содержимого
после стимуляции секреции ПЖ экзогенными
гормонами или гормоноподобными пептидами
(секретин-холецистокининовый
тест);непрямые тесты
— исследование. дуоденального содержимого
после пищевой стимуляции (тест Лунда);пероральные тесты
— проводят без канюлирования протока
ПЖ или введения зонда (тест с
N-бензоил-L-тирозил-парааминобензойной
кислотой — БТ-ПАБК; флюоресцеиндилауратный
или панкреатолауриловый тест; дыхательные
тесты с субстратом, меченным
радиоизотопами).
Секретин-панкреозиминовый
тест
является
«золотым стандартом» диагностики
нарушений внешнесекреторной
функции поджелудочной железы.
В
полученном секрете
определяют концентрацию бикарбонатов
и ферментов: амилазы,
трипсина, химотрипсина и липазы.
Наибольшее значение имеют
такие показатели, как максимальная
концентрация бикарбонатов,
дебит панкреатического сока (дуоденального
содержимого), максимальная концентрация
и дебит ферментов. При ХП обычно
обнаруживают снижение концентрации
бикарбонатов (<90
мэкв/л) и ферментов при нормальном объеме
аспирата (>2 мл/кг).
Уменьшение объема панкреатической
секреции при нормальной концентрации
бикарбонатов и ферментов позволяет
заподозрить
рак поджелудочной железы.
При
проведении теста
Лунда
стимуляцию секреции выполняют с помощью
жидкой пищевой смеси, содержащей 6%
жира,
5% белка
и 15% углеводов. Этот метод технически
более прост в проведении,
однако не позволяет оценить секрецию
бикарбонатов, а, кроме
того, его результаты зависят от состояния
тонкой кишки как места
выработки эндогенных стимуляторов.
Тест Лунда имеет меньшую
чувствительность и специфичность по
сравнению с секретин-панкреозиминовым
тестом, особенно при легкой степени
панкреатической
недостаточности.
В
последние годы все большее применение
находит метод определения
панкреатических ферментов (трипсин,
химотрипсин, эластаза,
липаза) в кале, прежде всего благодаря
своей неинвазивности.
Наибольшие преимущества имеет определение
эластазы в кале
иммуноферментным методом.Чувствительность
и специфичность эластазного теста у
больных с экзокринной
панкреатической недостаточностью
тяжелой и средней
степени приближаются к таковым
секретин-панкреозиминого
теста. При легкой степени внешнесекреторной
недостаточности
чувствительность метода составляет
63%.
Рисунок
2
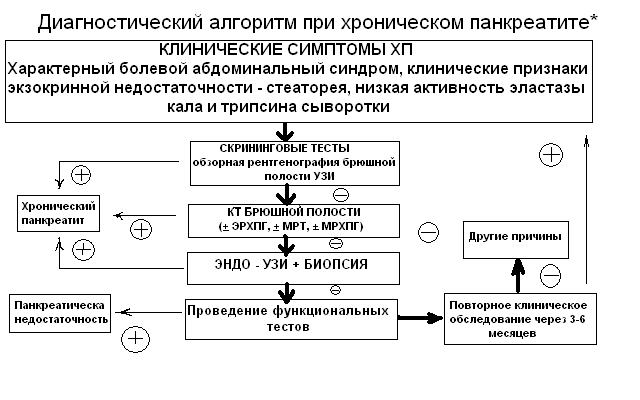
*рекомендации Европейской
многоцентровой группы по изучению
хронического панкреатита 2005 г.
Таблица 3.
Соседние файлы в папке metodichki
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Хронический панкреатит (ХП) — динамическая, плохо поддающаяся диагностике болезнь, эволюция которой обусловлена прогрессированием деструкции ткани поджелудочной железы (ПЖ) и возникновением осложнений. Динамическое наблюдение позволяет определить факты, влияющие на темп прогрессирования, стадию, характер и эффективность лечебных мероприятий. Большинство исследователей рассматривает ХП как прогрессирующее заболевание с повторяющимися обострениями хронического воспаления, развитием склероза и фиброза, приводящего к замещению секреторной ткани железы соединительной тканью и снижению внешнесекреторной функции ПЖ [2, 4]. Ведущими симптомами в клинической картине ХП являются боли и признаки недостаточности экзокринной функции ПЖ [3, 5].
Функционально-анатомической единицей ПЖ является ациноцит (ацинарная клетка). Они составляют от 70% до 90% клеточной массы ПЖ, собраны в альвеолярные образования разнообразной формы (ацинусы), которые состоят из 20–50 ацинарных клеток. Ацинусы между собой связаны протоковой системой ПЖ. Ациноциты синтезируют и секретируют в полость протоков белковый секрет, состоящий на 98% из ферментов: трипсина, химотрипсина, эластазы, коллагеназы, липазы, обладающих протео- и липолитической активностью. В ацинарных клетках и протоках ПЖ протеазы находятся в неактивной форме (трипсиноген, химотрипсиноген, проэластаза), и только после поступления панкреатического сока в просвет двенадцатиперстной кишки под влиянием энтерокиназ, цитокиназ кишечного сока и трипсина они переходят в активную форму. Из всего комплекса протеолитических ферментов особое положение занимает трипсин, который способен активировать сам себя и другие протеолитические ферменты, в том числе фосфолипазу. Секрет в протоках ПЖ содержит электролиты и бикарбонаты, его рН = 7,5–8,8. Максимум активности протеаз отмечен при рН = 7,0–8,0. Часть ферментов может быть активирована в зоне рН = 4,5–6,0, при сохранении протеолитической активности [7, 8].
Ткань ПЖ защищена от самопереваривания тем, что протеолитические ферменты синтезируются в неактивной форме. В клетке они находятся в зимогенных гранулах, и, кроме того, протеолитические ферменты прочно связаны с ингибиторами. В просвет протоков они поступают в неактивной форме. Но любое препятствие продвижения секрета (анатомическое сужение протоков, гипертензия, потеря «текучести» секрета ПЖ, наличие физического препятствия — камни, опухоль) может быть причиной внутрипротоковой активации протеолитических ферментов и аутолиза ткани ПЖ [11].
Транзиторное повышение уровня панкреатических ферментов (в два раза и более) во время болевого приступа указывает на наличие препятствия в протоках. Фармакотерапия в первую очередь должна быть направлена на снятие спазма гладкой мускулатуры. С этой целью используют ряд препаратов, обладающих спазмолитическим эффектом. Антихолинергические средства блокируют мускариновые рецепторы на постсинаптических мембранах органов-мишеней и, как следствие, снимают мышечный спазм. Часто используются спазмолитики: Метацин, Платифиллин, Бускопан и другие. Однако при приеме препаратов данной группы может наблюдаться ряд общеизвестных побочных эффектов.
Миотропные спазмолитики снижают тонус и двигательную активность гладкой мускулатуры. Основными представителями данной группы препаратов являются папаверин, дротаверин. Наиболее эффективным миотропным спазмолитиком в последнее время считается мебеверин (Дюспаталин) — мышечно-тропный, антиспастический препарат, который, блокируя натриевые каналы, обладает прямым действием на гладкую мускулатуру.
В контроле моторики и периферийной чувствительности участвуют многочисленные нейромедиаторы. Возмущающим эффектом для нарушения деятельности центральной нервной системы (ЦНС) (внутренний фактор) является воздействие внешних факторов — стресс, вызывающий чувство тревоги, социальная неустроенность, а на этом фоне любое нарушение диеты, употребление алкоголя, курение замыкают патогенетический «порочный круг», способствуя возникновению или поддержанию патологического процесса в ткани ПЖ.
ЦНС через ее вегетативный отдел выполняет координирующую функцию, вовлекая в этот процесс свои трансмиттеры: ацетилхолин (Ах) и серотонин (5-НТ) [9, 10], которые являются не только регуляторами воспаления и регенерации, но и стимуляторами секреторной активности ПЖ. У больных ХП, находящихся на стационарном лечении в ЦНИИГ, установлено повышенное содержание Ах и 5-НТ в крови. Нарушение регуляторных взаимоотношений является неблагоприятным фактором, влияющим на пато- и саногенез как острого, так и хронического панкреатита.
Серотонин играет важную роль в нарушениях моторики и в появлении висцеральной гиперчувствительности, наблюдающихся при этой патологии. Выделяемый локально из мастоцитов и энтерохромаффинных клеток, серотонин воздействует на рецепторы 5-НТ1 и 5-Т3, вызывая состояния висцеральной гиперчувствительности.
Несколько подтипов рецепторов 5-НТ располагаются не только на уровне нервных окончаний, но также и в клетках гладкой мускулатуры, иммунных клетках и энтероцитах.
Повышение активности холинергического нейронального контура энтеральной нервной системы приводит к усилению стимулирующего влияния серотонина на гладкие мышцы, меняя возбудимость всей функциональной системы, которая обеспечивает реализацию перистальтического рефлекса как нейронных сетей, так и гладких мышц.
Серотонин регулирует давление в протоковой системе путем действия на гладкомышечные волокна сфинктера Одди, поэтому преимуществом использования Дюспаталина при консервативном лечении ХП является то, что гладкомышечные сокращения подавляются не полностью, сохраняется нормальная перистальтика после подавления гипертонуса. Дюспаталин имеет преимущества: 1) избирательно действует на билиарный тракт и кишечник; 2) системные эффекты отсутствуют; 3) двойной механизм действия — устраняет спазм и не вызывает гипотонию; 4) действует только на гладкомышечную клетку; 5) не имеет атропиноподобного эффекта; 6) медленное высвобождение из капсул при пассаже по кишечнику (пролонгированное действие, минимум 12 часов) [3].
Для снижения болевого синдрома при обострении ХП используются и панкреатические ферменты. Обезболивающий эффект их связан (только в период обострения ХП, вариант А согласно классификации Лазебник Л. Б., Винокуровой Л. В. [1]) с тем, что попадание ферментов ПЖ, особенно трипсина, в двенадцатиперстную кишку приводит к разрушению регуляторных белков — релизинг-пептидов. Разрушение этих стимуляторов экзогенными ферментами снижает панкреатическую секрецию, что уменьшает давление в протоках и паренхиме ПЖ. Эталон по сочетанию и соотношению ферментативных препаратов — Креон (панкреатин) [2]. Креон является не только «золотым стандартом» ферментного препарата для заместительной терапии (вариант В и С течения ХП), но и эффективен для купирования панкреатической боли (вариант А). Положительное действие Креона по купированию боли осуществляется не только через релизинг-пептиды, но и через продукты гидролиза пищевых веществ [2, 3].
Таким образом, использование как ферментативных препаратов, так и спазмолитиков патогенетически обосновано при купировании болевого синдрома у больных ХП.
Классификация M-ANNHEIM (табл. 1) предусматривает выделение клинических стадий ХП [13].
Течение ХП разделяют на две фазы: бессимптомную и с наличием клинических проявлений, которая делится на четыре стадии (I, II, III, IV), в каждой из которых выделяют подстадии, включаются случаи с развитием тяжелых осложнений.
Одним из основных клинических проявлений ХП является абдоминальная боль, которая связана со сложным многоуровневым взаимодействием ноцицептивной и антиноцицептивной систем, возбуждение которых зависит от количества нейромедиаторов, дисбаланса нейрогормональной регуляции и структурных изменений ткани ПЖ. Обострение ХП на ранних стадиях заболевания сопровождается выраженным болевым синдромом, повышением 5-НТ и Aх, и секреторная активность осуществляется за счет Aх. При развитии склероза, фиброза, кальциноза, формировании кист и псевдокист остается высоким уровень 5-НТ и Aх, но секреторная активность регулируется за счет 5-НТ. Снижается роль парасимпатического отдела вегетативной нервной системы. Стимуляция секреторной активности ПЖ переходит на автономный тип регуляции, что является прогностически неблагоприятным фактором, так как способствует прогрессированию заболевания и формированию осложнений. При сопоставлении выявленных клинических, морфологических и лабораторных данных, как уже указывалось, выделено три варианта течения ХП [1] (табл. 2).
По интенсивности боли, длительности заболевания больных можно разделить на три группы. При сравнении этих двух параметров выявлена обратная зависимость между ними: чем больше длительность заболевания, тем выраженность боли меньше. В настоящее время для оценки наличия, степени и локализации боли в клинике используются психологические, психофизиологические и нейрофизиологические методы, большинство из которых основаны на субъективной оценке своих ощущений самими пациентами. Наиболее простыми способами количественной характеристики боли являются ранговые шкалы [6, 8, 12]. Числовая ранговая шкала состоит из последовательного ряда чисел от 0 до 10. Пациентам предлагается оценить свои болевые ощущения цифрами от 0 (нет боли) до 10 (максимально возможная боль).
Учитывая вышеизложенные данные, а также результаты клинических, инструментальных, лабораторных и морфологических исследований, были выделены три варианта течения хронического панкреатита.
Вариант А — длительность заболевания менее 5 лет, выраженный болевой синдром, уровень панкреатической эластазы кала (Е-1) снижен незначительно, но достоверно (р < 0,05), отмечается повышение содержания в крови Aх (р < 0,05) и 5-НТ (р < 0,05), высокий уровень провоспалительных цитокинов, умеренное повышение холецистокинина (ХЦК) и снижение секретина. В ткани ПЖ выявляются воспаление и отек.
Вариант В — длительность заболевания от 5 до 10 лет, значительно снижается уровень Е-1 (ниже 100 мкг/г), болевой синдром умеренный, начинает преобладать 5-НТ (р < 0,05) как стимулятор секреторной активности ПЖ. Остаются высоким ХЦК и низким секретин. Дальнейшее прогрессирование фиброзных изменений, выявляется кальциноз в ткани ПЖ.
Вариант С — длительность заболевания от 10 и более лет, мало выраженный болевой синдром, дальнейшее повышение концентрации 5-НТ, что приводит к декомпенсации регуляторных механизмов секреторной активности ПЖ. Сохраняется повышение ХЦК и снижение секретина. Защитные свойства слизи двенадцатиперстной кишки снижаются. На фоне снижения уровня эндогенного инсулина в 30% случаев развивается клиническая картина сахарного диабета. Таким образом, лечение ХП необходимо проводить с учетом того, что на первой стадии заболевания ферментная терапия в большей степени применяется для снятия болевого синдрома, а на более поздних стадиях в качестве заместительной терапии. Дозы ферментных препаратов назначаются индивидуально в зависимости от степени тяжести внешнесекреторной недостаточности ПЖ. Высокое содержание ферментов, в первую очередь, соотношение колипаза/липаза > единицы, наряду с наличием кислотоустойчивой оболочки, является обязательным условием, предъявляемым к современным ферментным средствам. Эталоном в этом отношении является препарат Креон, в котором соотношение колипазы/липазы оптимально (1,9) [2, 14].
Литература
Винокурова Л. В., Трубицына И. Е., Лазебник Л. Б. и др. Варианты течения хронического алкогольного панкреатита // Экспериментальная и клиническая гастроэнтерология. 2007. № 6. С. 6–9.
Губергриц Н. Б. Панкреатическая боль. Как помочь больному. М.: Медпрактика-М, 2005. 175 с.
Губергриц Н. Б., Загоренко Ю. А. Хронический алкогольный панкреатит //Ученые заметки. Материалы 2-го междисциплинарного российского конгресса. Человек, алкоголь, курение и пищевые аддикции,24–25 апреля 2008, c. 16–26.
Данилов М. В., Федоров В. Д. Хирургия поджелудочной железы. Рук-во для врачей. М.: Медицина, 1995. 512 с.
Козлов И. А. Хронический панкреатит с преимущественным поражением головки поджелудочной железы. Диагностика и хирургическое лечение. Автореферат дис. уч. ст. доктора мед. наук. М.,2005.46 с.
Кукушкин М. Л., Хитров Н. К. Общая патология боли. М.: Изд. Медицина, 2004. 141 с.
Маев И. В., Самсонов А. А. Болезни двенадцатиперстной кишки. М.: МЕДпресс, 2005. 511 с.
Маев В. И., Казюлин А. Н., Кучерявый Ю. А. Хронический панкреатит. М.: Москва, 2005. 504 с.
Трубицына И. Е., Дроздов В. Н., Руть М. В. Вариации и частота распределения количественного значения ацетилхолина холинестеразной активности в сыворотке и крови у здоровых лиц // Экспериментальная и клиническая гастроэнтерология. 2007. № 3 С. 78–81.
Уголев А. М., Тимофеева Н. М., Груздков А. А. Адаптация пищеварительной системы / Физиология адаптационных процессов: Рук. по физиологии. М.: Наука. 1986. С. 371–480.
Amman R. W. A clinically based classification system for alcoholic chronic pancreatitis summary of an international workshop on chronic pancreatitis // Pacreas. 1997. Vol. 14. P. 215–221.
Bonior J. et al. Does endotoxemia in the infant rats modulate apoptosis in the pancreatic acinar cells? // Pancreatology. 2008. Vol. 8 (3). P. 298.
Schneider A., Lohr J. M., Singer M. V. The M-ANNHEIN — classification of chronic pancreatitis: Introduction of a unifying classification system based on revien of previous classification of the disease // J. Gastroenterol. 2007. Vol. 42. P. 101–119.
Rudmann Ed. M. A. Creon. Hannover (Germeany): Solvay Pharmaceuticals GmbH, 2000. 84 p.
Л. В. Винокурова, кандидат медицинских наук
И. Е. Тубицына, доктор медицинских наук
ЦНИИ гастроэнтерологии, Москва
Контактная информация об авторах для переписки: gastroenter@rambler.ru
Варианты течения хронического панкреатита
Купить номер с этой статьей в pdf
Источник


