Ультразвуковым маркером острого панкреатита не является
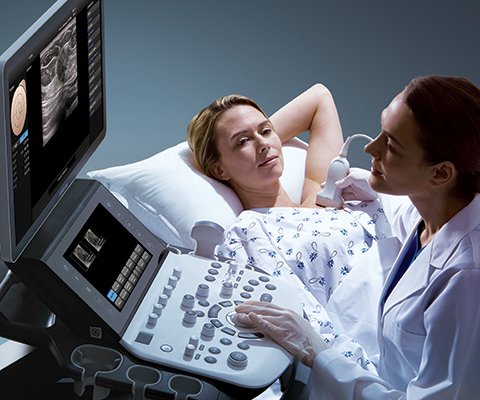
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
В России за последние годы отмечена тенденция к увеличению количества больных острым панкреатитом, частота которого достигает 2,5 — 8,4% среди пациентов с острыми хирургическими заболеваниями органов брюшной полости [1]. В странах Западной Европы, в частности, в Дании с 1979 по 1992 гг., частота острого панкреатита увеличилась с 26,8 до 35,4 на 100000 населения [15], т.е. на 25%. По данным М. В. Гринева [8], из всех больных с острым панкреатитом деструктивные формы отмечены у 16,2%, которые при прогрессировании приводят к летальности почти в 50% случаев [4].
Благодаря новым методам исследования (УЗИ, КТР, ЯМР) улучшилась ранняя диагностика острого панкреатита и его осложнений, появилась возможность динамического наблюдения за больными в процессе лечения. Для широкой практики особый интерес представляет ультразвуковая диагностика — неинвазивный, неионизирующий метод, который можно применять многократно, не причиняя вреда больному. С помощью эхографии стало возможным эффективно проводить не только диагностические, но и лечебные малоинвазивные вмешательства на поджелудочной железе — биопсию, дренирование патологических образований и т.д. [4, 6, 8].
Несмотря на интенсивное внедрение эхографии в практику и определенные успехи в изучении возможностей метода, в литературе еще недостаточно освещены вопросы, касающиеся деталей ультразвуковой семиотики острого панкреатита. Не конкретизирована эхографическая картина острого панкреатита в зависимости от стадии заболевания, мало отражены вопросы, касающиеся диагностики осложнений острого панкреатита, особенно редких, но клинически значимых [2, 5, 9 — 14, 16]. У пациентов, лечившихся оперативно по поводу острого панкреатита, актуальной остается проблема ультразвукового мониторинга в послеоперационном периоде. Практически не изучена роль данных ультразвукового исследования для выработки индивидуальной тактики лечения и прогнозирования возможных осложнений у каждого конкретного больного.
Материалы и методы
В основу работы положены данные 534 УЗ-исследований у 278 пациентов с острым панкреатитом, находившихся на лечении в городской клинической больнице N 9 за период 1992-1995 гг. Исследования проводились с помощью ультразвукового сканера, оснащенного конвексным датчиком 3,5 МГц и секторным — 5 МГц.
Результаты
На основе наших наблюдений выявлены следующие сонографические особенности острого панкреатита:
Изменения непосредственно в поджелудочной железе:
- увеличение размеров поджелудочной железы (рис. 1) — отмечено в 88% случаев. Нормальные размеры поджелудочной железы: головка 3-4,5 см; тело 2,5 — 3 см; хвост 3-4 см;
- нечеткость контуров — 90,6% случаев;
- увеличение расстояния между задней стенкой желудка и передней поверхностью поджелудочной железы свыше 3 мм и достигающее 10 — 20 мм, что характеризует отек парапанкреатических тканей, отмечено в 53% наблюдений (рис. 1);
- изменение эхогенности железы: повышение — 85,6% случаев (рис. 2); нормальная — 8,6% случаев; понижение — 5,8% случаев.
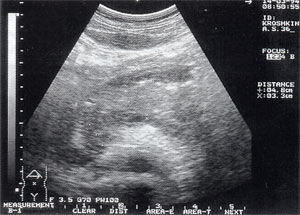
Рис. 1. Острый панкреатит, деструктивная форма. Увеличение размеров поджелудочной железы, нечеткость контуров, увеличение расстояния между задней стенкой желудка и поджелудочной железы.
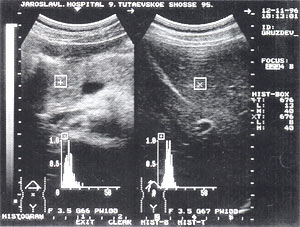
Рис. 2. Острый панкреатит, повышение эхогенности поджелудочной железы (по сравнению с эхогенностью печени).
Изменения в брюшной полости, являющиеся косвенными признаками острого панкреатита и относящиеся к его осложнениям:
Оментобурсит (рис. 3) встречается в 28,4% случаев (из них 48% у мужчин и 52% у женщин). Некоторые авторы обозначают эту патологию как «псевдокиста поджелудочной железы». Отмечен объем таких образований от 5мл (малые объемы необходимо дифференцировать с сосудистыми аневризмами) до 3 л и более. Скорость формирования оментобурсита при остром панкреатите от 2 — 4 дн. от начала заболевания до 2 — 4 нед. При ультразвуковом исследовании оментобурсит представлен в виде анэхогенного образования с четкими контурами, неправильной или округлой формы, чаще с однородной структурой, с толщиной стенок 0,2 — 0,4 см. При эхографическом мониторинге утолщение стенки до 0,5 — 1,0 см с появлением неоднородности структуры следует расценивать как сонографический признак абсцедирования.
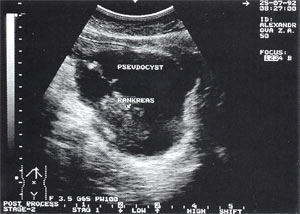
Рис. 3. Псевдокиста поджелудочной железы при остром панкреатите в виде анэхогенного образования с четкими контурами, однородной структурой, с наличием гиперэхогенных включений (детрит поджелудочной железы).
Свободная жидкость в брюшной полости — отмечена в 18% случаев (рис. 4), из них 80% у мужчин и 20% у женщин. Жидкость в объеме до 100 мл определяется только в одной анатомической области ( чаще в малом тазу), более 100 мл — по боковым каналам и в других отделах брюшной полости. В первые дни развития острого панкреатита жидкость гомогенная, после 6-12 сут. часто структура неоднородная из-за «нитевидных» включений (как правило, фибрин).
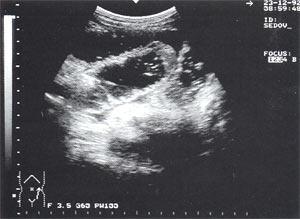
Рис. 4. Расширенные петли тонкого кишечника до 3,5 см, заполненные жидким содержимым на фоне свободной жидкости в брюшной полости.
Билиарная гипертензия — встречается в 13% случаев, из них 25% у мужчин и 75% у женщин. При эхографии отмечается расширение внутрипеченочных желчных протоков, общего печеночного протока и общего желчного протока. При отсутствии холедохолитиаза билиарная гипертензия как правило наблюдается при очаговом панкреонекрозе в области головки поджелудочной железы.
Инфильтраты брюшной полости — обнаруживаются в 5,4% случаев (рис. 5, 6), в том числе 64% у мужчин и 36% у женщин. Как правило, инфильтрируется большой сальник (оментит), визуализирующийся в виде образования повышенной эхогенности с нечеткими неровными контурами, неоднородной структурой, с участками пониженной эхогенности, которые могут свидетельствовать о формировании в нем абсцессов. Размеры инфильтратов от 5 до 15 — 20 см.
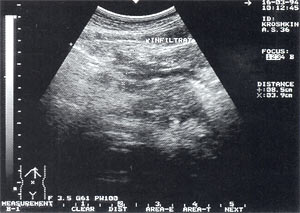
Рис. 5. Инфильтрат в брюшной полости в проекции большого сальника — представлен образованием неправильной формы с нечеткими контурами, неоднородной структурой, с наличием гипер- и гипоэхогенных участков. Размер инфильтрата 8,5 х 3,9 х 5,3см.
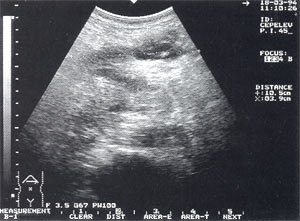
Рис. 6. Инфильтрат в проекции большого сальника с анэхогенным включением до 4 см (абсцедирование).
Забрюшинные флегмоны — встречаются в 4,3% случаев (рис. 7), из них 67% у мужчин и 33% у женщин. В 95% случаев диагностирована левосторонняя локализация флегмоны, которая определялась в виде анэхогенного или гипоэхогенного образования чаще щелевидной или овальной формы. Как правило, причиной развития данного осложнения является распространение панкреатического секрета по забрюшинному пространству из псевдокисты, иногда доходящее до паховой области. Панкреатогенный паранефрит можно рассматривать как вариант забрюшинной флегмоны.
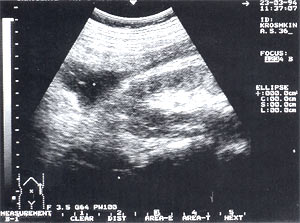
Рис. 7. Забрюшинная флегмона слева — анэхогенное образование неправильной формы с нечеткими контурами. Сканирование проведено из левой поясничной области.
Гидроторакс — встречается в 2,2% случаев, одинаково часто у мужчин и женщин, с преимущественно левосторонней локализацией.
Тромбоз в системе воротной вены — отмечается в 1,5% случаев (рис. 8 а, б) и достаточно хорошо может быть определен, по нашему мнению, без допплеровского исследования. При признаках портальной гипертензии обязательно должно выполняться прицельное ультразвуковое исследование сосудов системы воротной вены. Тромбы могут быть одиночными и множественными. Они локализуются как в самой воротной вене, так и в селезеночной и верхнебрыжеечной венах.
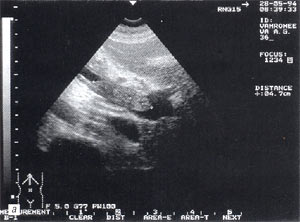
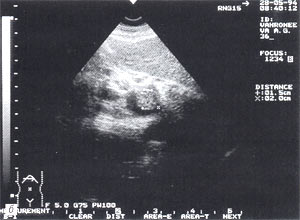
Рис. 8. Тромбоз воротной вены. Просвет вены полностью обтурирован изоэхогенным образованием с четкими контурами, неоднородной структурой, длиной до 4,7 см (а — cагиттальный срез, б — поперечный срез).
Парез кишечника — встречается в 1,4% случаев (см. рис. 4), из них 75% у мужчин и 25% у женщин. Характеризуется расширением петель тонкого кишечника до 3 — 5 см с заполнением их жидким содержимым и регистрируемой «маятникообразной» перистальтикой.
Гидроперикард — встречается в 0,4% случаев.
Восходящий медиастенит, отмечаемый другими авторами, нами не наблюдался.
Абсцессы поджелудочной железы — встречаются как правило на фоне уже имеющихся ультразвуковых признаков хронического панкреатита.
Разрывы псевдокист поджелудочной железы при ультразвуковой диагностике наблюдались у 2 больных (0,7%).
Кровоизлияние в псевдокисту поджелудочной железы с формированием организованной гематомы (рис. 9) отмечено у 1 пациента (0,35%).
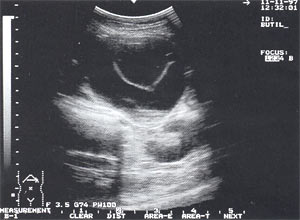
Рис. 9. Псевдокиста поджелудочной железы в виде анэхогенного образования с четкими контурами, в котором определяется другое анэхогенное образование с капсулой 0,2 — 0,3 см (на операции — псевдокиста с организовавшейся гематомой).
Псевдокисты поджелудочной железы с атипичной локализацией (в печени, селезенке, перидуоденально и т.д.) выявлены у 2 больных — 0,7% (рис. 10).
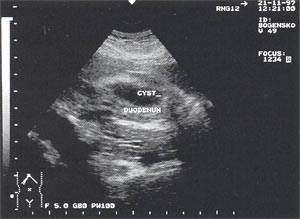
Рис. 10. Атипично расположенная псевдокиста поджелудочной железы (парадуоденально) в виде анэхогенного образования округлой формы с четкими контурами, однородной структурой, размером до 4,5 см, расположенного рядом с двенадцатиперстной кишкой.
Инфаркты селезенки (1 больная — 0,35%) — на фоне тромбоза воротной вены с портальной гипертензией.
Разрывы селезенки вследствие портальной гипертензии (нами не наблюдались).
Панкреатогенные паранефриты — обнаружены у 2 пациентов, что составило 0,7% (рис. 11).
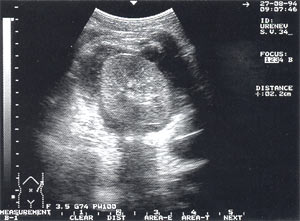
Рис. 11. Левосторонний панкреатогенный паранефрит, визуализирующийся в виде жидкостного образования, окружающего почку со всех сторон. Поперечный срез.
Заключение
Проведенное исследование показывает, что ультразвуковая диагностика должна быть обязательным элементом диагностического алгоритма у больных острым панкреатитом. Для повышения диагностической ценности эхографии необходима определенная последовательность в выполнении ультразвукового исследования: детальный осмотр парапанкреатических тканей и самой железы; осмотр всех отделов брюшной полости на предмет свободной жидкости и инфильтратов; осмотр плевральных полостей и полости перикарда на наличие выпота; детальный осмотр внутри- и внепеченочных желчных протоков; прицельный осмотр сосудов системы воротной вены; исследование забрюшинного пространства; динамическое наблюдение (частота повторного УЗИ определяется степенью тяжести заболевания и вероятностью развития осложнений).
Для улучшения получаемых результатов УЗИ могут быть рекомендованы следующие технические приемы:
- при плохой визуализации хвост поджелудочной железы лучше исследовать через селезенку или левую почку;
- для улучшения визуализации поджелудочной железы можно применять заполнение желудка 500 — 800 мл дегазированной жидкости (воды);
- использовать датчики с различной частотой излучения для более детального исследования патологических очагов, расположенных на разном расстоянии от датчика;
- использовать полипозиционное сканирование с дозированной компрессией на брюшную стенку для улучшения визуализации исследуемых органов, что позволяет «раздвигать» петли кишечника, создавая тем самым дополнительное «акустическое окно»;
- применять ультразвуковую фистулографию с жидкими и газообразующими растворами (фурацилин, новокаин, «Echovist») для определения полостей при наличии панкреатических свищей [7], что может быть предметом отдельных исследований.
Литература
- Скуя Н. А. Заболевания поджелудочной железы. — М.: Медицина, 1986.
- Зубарев А. Р., Григорян Р. А. Ультразвуковое ангиосканирование. — М.: Медицина, 1990.
- Филин В. И., Костюченко А. А.. Неотложная панкреатология. — СПб., 1994.
- Нестеренко Ю. А., Михайлусов С. В., Иманалиев М. Р. Ультразвук в диагностике и лечении панкреонекроза/ Сб. научн. тр. Пленума проблемной комиссии по неотложной хирургии. — М.: 1994. — С. 26 — 29.
- Баранов Г. А., Могутов М. С, Завьялова Н. И. Ультразвуковая диагностика тромбоза воротной вены как редкого осложнения острого панкреатита/ Сб. науч. тр. международной конференции «Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны». — М.: 1995. — С. 4 — 5.
- Белокуров ГО. Я., Уткин А. К., Жохов В. К., Белокуров С. Ю., Могутов М. С. Предпосылки использования прецизионной техники в лечении ложных кист поджелудочной железы/ Сб. научн. тр. международной конференции «Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны». М.: 1995. — С. 78.
- Буйлов В. М., Могутов М. С, Карпов Н. Р. Ультразвуковая фистулография с «Echovist-300» в хирургии и урологии. — Материалы II съезда Ассоциации специалистов ультразвуковой диагностики в медицине. — М.: 1995. — С. 80.
- Гринев М. В., Красногоров В. Б., Рысс А. С, Веселов В. С, Смелянский А. И., Алексеенко Е. Н. Эффективная тактика лечения деструктивного панкреатита на основе раннего плазмафереза и малоинвазивных хирургических вмешательств/ Сб. научн. тр. «Малоинвазивные вмешательства в хирургии». М.: 1996. — С. 257.
- McCormick P. A., Chronos N., Burroughs A. К., Mclntyre N., McLaughlinJ.E. Pancreatic pseudocyst causing portal vein thrombosis and pancreatico — pleural fistula.In: Gut (1990 May) 31(5):561-3.
- Fernandez-Cruz-L., Margarona-E., Llovera-J., Lopez-Boado-M. A., Saenz-HT. Pancreatic ascites. Hepatogastroenterology. 1993 Apr; 40(2): 150-4.
- Nishida-K., Terai-Y., Nojiri-L, Kato-M., Higashijima-M., Takagi-K., Adashi-R. A case of pancreatic pseudocyst with intracystic hemorrhage and repeated gastrointestinal bleeding. Nippon-Ronen-Igakkai-Zasshi. 1993 Aug; 30(8): 714-9.
- Sonak-R., Stock-W., Janzik-U., Hayduk-K., Borchard-F. Duodenal duplication cyst — a rare cause of acute recurrent pancreatitis. Leber-Magen-Darm. 1993 Sep; 23(5): 211-5.
- De-Ronde-T., Van-Beers-B., de-Canniere-L., Trigaux-JP., Melange-M. Thrombosis of splenic artery pseudoaneurysm complicating pancreatitis. Gut. 1993 Sep; 34(9): 1271-3.
- Hamm-B., Franzen-N. Atypically located pancreatic pseudocysts in the liver, spleen, stomach wall and mediastinum: their CT diagnosis. Rofo-Fortschr-Geb-Rontgenstr-Neuen-Bildgeb-Verfahr. 1993 Dec; 159(6): 522-7.
- Worning-H. Acute pancreatitis in Denmark. Ugeskr-Laeger. 1994 Apr 4; 156(14): 2086-9.
- Yasuda I., Tomita E., Nishigaki Y., Ino Y., Shimizu H., Yamada T., Kawamura H., Kuroda T., Takahashi T., Nagura K. A case of portal vein thrombosis subsequent to acute pancreatitis. Nippon Shokakibyo Gakkai Zasshi (1995 Apr) 92(4):820-5.

УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Источник
Клиническое обследование
Основные симптомы острого панкреатита — боль, рвота и метеоризм (триада Мондора).
Боль появляется внезапно, чаще вечером или ночью вскоре после погрешности в диете (употребление жареных или жирных блюд, алкоголя). Наиболее типичная её локализация — эпигастральная область, выше пупка, что соответствует анатомическому расположению поджелудочной железы. Эпицентр боли располагается по средней линии, но может смещаться вправо или влево от срединной линии и даже распространяться по всему животу. Обычно боли иррадиируют вдоль рёберного края по направлению к спине, иногда в поясницу, грудь и плечи, в левый рёберно- позвоночный угол. Часто они носят опоясывающий характер, что создает впечатление затягивающегося пояса или обруча. При преимущественном поражении головки поджелудочной железы локализация боли может напоминать острый деструктивный холецистит, при поражении её тела — заболевания желудка и тонкой кишки, а при поражении хвоста — заболевания селезёнки, сердца и левой почки. В ряде ситуаций резкий болевой синдром сопровождается коллапсом и шоком.
Практически одновременно с болями появляется многократная, мучительная и не приносящая облегчения рвота. Провоцирует её приём пищи или воды. Несмотря на многократный характер рвоты, рвотные массы никогда не имеют застойного (фекалоидного) характера.
Температура тела в начале заболевания чаще субфебрильная. Гектическая лихорадка указывает на развитие распространённых стерильных и разнообразных инфицированных форм панкреатита. На основании выраженности симптомов системной воспалительной реакции можно лишь условно судить о характере и распространённости деструктивного процесса.
Важным и ранним диагностическим признаком панкреонекроза считают цианоз лица и конечностей. Цианоз в виде фиолетовых пятен на лице известен как симптом Мондора, цианотичные пятна на боковых стенках живота (околопупочные экхимозы) — как симптом Грея-Тернера, а цианоз околопупочной области — симптом Грюнвальда. В поздние сроки заболевания цианоз лица может смениться яркой гиперемией — «калликреиновое лицо». В основе перечисленных признаков лежат быстропрогрессирующие гемодинамические и микроциркуляторные расстройства, гиперферментемия и неконтролируемый цитокинокинез.
При осмотре живота отмечают его вздутие, преимущественно в верхних отделах. При распространённом панкреонекрозе живот равномерно вздут, резко чувствителен даже при поверхностной пальпации. При глубокой пальпации боли резко усиливаются, порой носят нестерпимый характер. При пальпации поясничной области, особенно левого рёберно-позвоночного угла, возникает резкая болезненность (симптом Мейо-Робсона). В зоне повышенной чувствительности, обнаруживаемой при поверхностной пальпации, выявляют ригидность мышц передней брюшной стенки, что свидетельствует о наличии панкреатогенного выпота, богатого ферментами, и явлениях панкреатогенного перитонита. Часто наблюдают поперечную болезненную резистентность передней брюшной стенки в проекции поджелудочной железы (симптом Керте).
Одним из признаков деструктивного панкреатита считают феномен отсутствия пульсации брюшного отдела аорты вследствие увеличения в размерах поджелудочной железы и отёка забрюшинной клетчатки — симптом Воскресенского.
При локализации процесса в сальниковой сумке, мышечное напряжение выявляют преимущественно в эпигастральной зоне; при распространении воспаления за её пределы (на околоободочную и тазовую клетчатку, а также на брюшину) появляется выраженное мышечное напряжение и положительный симптом Щёткина- Блюмберга. Необходимо помнить, что при локализации некротического процесса в хвостовой части поджелудочной железы симптомы раздражения брюшины могут быть слабовыраженными, что связано с преимущественно забрюшинной локализацией процесса и отсутствием явлений перитонита. При поражении головки типично быстрое развитие синдрома желтухи и гастродуоденального пареза.
Притупление перкуторного звука в отлогих местах живота свидетельствует о наличии выпота в брюшной полости. Аускультация живота выявляет ослабление или отсутствие кишечных шумов вследствие развития паралитической кишечной непроходимости и панкреатогенного перитонита.
Лабораторная диагностика
Основное проявление острого панкреатита — функциональные расстройства поджелудочной железы, в частности, феномен гиперферментемии. Эту особенность патогенеза острого панкреатита на протяжении многих десятилетий традиционно используют в дифференциальной диагностике с другими неотложными заболеваниями органов брюшной полости. Определение в плазме крови активности амилазы (реже — липазы, трипсина, эластазы) — диагностический стандарт. Наиболее распространено в клинической практике определение активности амилазы и липазы в крови. Увеличение активности общей и панкреатической амилазы в 4 раза и липазы в 2 раза по отношению к верхней границе нормы свидетельствует о феномене панкреостаза.
Максимальные значения активности сывороточной амилазы характерны для первых суток заболевания, что соответствует срокам госпитализации в стационар большинства пациентов с острым панкреатитом. Определение активности липазы в крови — значимый диагностический тест в более поздние сроки от начала заболевания, поскольку её активность в крови больного острым панкреатитом сохраняется более длительное время, чем значения амилаземии. Этот феномен определяет более высокую чувствительность и специфичность липазного теста по отношению к амилазному.
В отечественной клинической практике традиционно используют определение амилазы в моче. Дополнительный тест — исследование активности амилазы в перитонеальном экссудате при лапароскопии (лапароцентезе). При использовании метода Вольгемута (определение суммарной амилолитической активности мочи), по которому нормальная активность амилазы в моче составляет 16-64 ед., можно обнаружить различные уровни её повышения — 128-1024 ед. и более. Метод Вольгемута недостаточно специфичен в отношении панкреатической α-амилазы, так как отражает суммарную активность гликолитических ферментов, которые содержатся в биологической среде, присланной на исследование.
Определение в крови активности трипсина и эластазы в диагностике острого панкреатита имеет меньшее клиническое применение, чем лабораторный мониторинг амилазы (липазы) в связи с трудоёмкостью и дороговизной методик.
Гипреамилаземия в динамике заболевания — важный маркёр сохранённой функции поджелудочной железы в условиях панкреостаза, что типично для интерстициального панкреатита или очагового (головчатого) панкреонекроза в первые дни заболевания. Дисферментемия (нарушение соотношений амилазы и липазы крови) свидетельствует о панкреонекробиозе, тогда как нормальный уровень амилазы в крови, гипоамилаземия (и даже аферментемия) наиболее характерны для панкреонекроза, свидетельствуя о распространённом характере деструкции поджелудочной железы и утрате ею экскреторной функции.
Прямая зависимость между уровнем амилаземии (амилазурии), распространённостью и формой панкреонекроза (интерстициальной, жировой, геморрагической) отсутствует. Результаты исследований ферментного спектра крови следует всегда рассматривать только в совокупности с данными других клинических, лабораторных и инструментальных методов обследования больного с острым панкреатитом.
Изменения в клиническом анализе крови при остром панкреатите не имеют строгой специфичности. В связи с этим широко известны существенные трудности лабораторной дифференциальной диагностики асептических и инфицированных форм панкреонекроза, что крайне важно с позиции своевременности оперативного лечения. Увеличение этих показателей в динамике заболевания более чем на 30% исходного уровня в совокупности с другими клинико-лабораторными данными достоверно подтверждает развитие панкреатогенной инфекции, но при этом, как правило, остаются упущенными 2-3 сут. Наиболее убедительно в пользу инфицированного характера панкреонекроза свидетельствуют пороговые числа лейкоцитов крови выше 15х109/л и лейкоцитарного индекса интоксикации более 6 ед.
Косвенными признаками инфицирования считают тромбоцитопению, анемию и ацидоз, их необходимо учитывать в совокупности клинических и инструментальных данных.
Биохимические изменения крови свидетельствуют о развитии синдрома гипер- и дисметаболизма, который наиболее выражен при деструктивных формах панкреатита. В этих ситуациях наиболее значимы такие изменения биохимического спектра крови, как диспротеинемия, гипопротеин и гипоальбуминемия, гиперазотемия и гипергликемия. Стойкая гипергликемия свидетельствует об обширном некрозе поджелудочной железы, а её значение больше 125 мг/дл (7 ммоль/л) — неблагоприятный прогностический фактор. В липидном спектре крови регистрируют гипертриглицеридемию, гипохолестеринемию, дефицит липопротеидов высокой плотности, увеличение концентрации жирных кислот.
C-реактивный белок наряду с гаптоглобином и α1-антитрипсином — белок острой фазы воспаления. При остром панкреатите содержание С-реактивного белка больше 120 мг/л в крови больного говорит о некротическом поражении поджелудочной железы. Концентрация С-реактивного белка отражает степень выраженности воспалительного и некротического процессов, что позволяет использовать этот тест для определения, с одной стороны, отёчного панкреатита или панкреонекроза, с другой — стерильного или инфицированного характера некротического процесса.
Применение прокальцитонинового теста при различных формах острого панкреатита показало, что у больных с инфицированным панкреонекрозом концентрация прокальцитонина достоверно выше, чем при стерильном деструктивном процессе.
Пороговой для распространённого панкреонекроза считают концентрацию С-реактивного белка более 150 мг/л, а прокальцитонина — больше 0,8 нг/мл. Распространённая панкреатогенная инфекция характеризуется концентрациями С-реактивного белка в крови больного больше 200 мг/л и прокальцитонина больше 2 нг/мл.
Среди других биохимических маркёров, характеризующих тяжесть острого панкреатита, перспективны исследования каталитической активности фосфолипазы А2, трипсиногена, уротрипсиногена-2, трипсин-активированного пептида, панкреатит-ассоциированного протеина, интерлейкинов 1, 6 и 8, фактора некроза опухолей и эластазы нейтрофилов. Установлено, что концентрация трипсин-активированного пептида в моче коррелирует с концентрацией С-реактивного белка и интерлейкина 6. Концентрация этого метаболита в перитонеальной жидкости прямо пропорциональна степени некроза поджелудочной железы.
Несмотря на то что содержание большинства биохимических субстанций резко увеличивается в крови больных панкреонекрозом уже в ближайшие сроки (24-48 ч) от начала заболевания, использование этих маркёров в клинической практике экстренной хирургии ограничено высокой стоимостью методик и отсутствием достоверно известного минимального порогового уровня. Своеобразным компромиссом в сложившихся материально-технических условиях представляется определение концентрации С-реактивного белка в любой биохимической лаборатории.
Гемоконцентрация наиболее характерна для деструктивных форм острого панкреатита. Гематокрит более 47% на момент госпитализации больного в стационар и отсутствие его снижения в течение 24 ч интенсивной терапии свидетельствует о развитии панкреонекроза.
Исследование спектра печёночных ферментов у больных острым панкреатитом, осложнённым развитием печёночно-клеточной недостаточности, характерной для панкреонекроза, позволяет выявить высокую активность аланиновой и аспарагиновой аминотрансфераз. Значительное увеличение активности лактатдегидрогеназы отражает крупномасштабное повреждение панкреацитов. С позиции дифференциальной диагностики необходимо помнить, что аналогичные изменения характерны для острого инфаркта миокарда, обширного инфаркта кишечника и гепатитов различной этиологии.
При билиарном панкреатите вследствие холедохолитиаза, а также при преимущественном поражении головки поджелудочной железы характерен синдром холестаза, выражающийся гипербилирубинемией с преобладанием прямой (связанной) фракции билирубина, высокой активности аспартатаминтрансферазы и щелочной фосфатазы.
О выраженных изменениях водно-электролитного баланса свидетельствуют гемоконцентрация, дефицит калия, натрия, кальция. При распространённых формах панкреонекроза снижение концентрации кальция в плазме крови обусловлено его депонированием в очагах стеатонекроза в виде солей жёлчных кислот.
B.C. Савельев, М.И. Филимонов, С.З. Бурневиг
Источник


