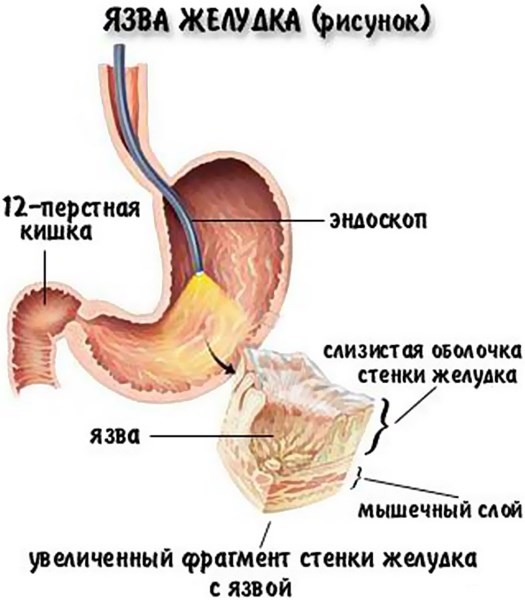
Сумамед при язве желудка
Комментарии
Опубликовано в журнале:
КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ И ТЕРАПИЯ »» 2000, 9 (1) В. А. Исаков, Л. В. Кудрявцева
Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского,
Лаборатория клинической микробиологии ЦКБ МЦ УД Президента РФ, Москва
В настоящее время антихеликобактерная терапия является стандартом лечения язвенной болезни, что отражено в международных и Российских рекомендациях [1, 2]. Согласно этим рекомендациям, наиболее эффективным режимом лечения считается тройная терапия, состоящая из базисного препарата (обычно препарат висмута или блокатор протонного насоса) и двух антибиотиков. Выбор антибиотиков имеет ключевое значение, так как именно они определяют эффективность, переносимость и стоимость лечения. Существуют несколько факторов, существенно влияющих на результат тройной терапии. Основным из них является резкое увеличение в популяции доли штаммов Н. pylori, устойчивых к антибиотикам, используемым в схемах лечения. Так, за 5 лет активного лечения заболеваний, ассоциированных с Н. pylori, в Гонконге доля штаммов H. pylori, резистентных к метронидазолу, увеличилась с 22 до 75 % [3]. Клинические исследования показывают, что эффективность схем тройной терапии, содержащих метронидазол, в среднем ниже на 30 %, если штамм Н. pylori устойчив к этому препарату.
Другой не менее важной проблемой является стоимость лечения. Чем она выше, тем больший процент эрадикации Н. pylori должна обеспечивать схема терапии, чтобы быть экономически выгодной. Стандартные схемы лечения были экономически выгодными при своей достаточно высокой стоимости, если частота эрадикации Н. pylori составляла 80 – 90 %. В настоящее время, когда распространенность штаммов Н. pylori, устойчивых к метронидазолу, достаточно высока, а эффективность стандартных схем лечения далека от идеальной, они перестают быть экономически выгодными.
В связи с этим, в схемах антихеликобактерной терапии стали широко использовать макролиды, главным образом кларитромицин. Однако, несмотря на высокую эффективность, препарат является дорогостоящим и вызывал ряд побочных реакций (диарея), которые ухудшали переносимость терапии в целом. Указанные обстоятельства послужили основанием для поиска макролидов, которые бы не уступали кларитромицину по эффективности, но стоили бы дешевле и давали меньше нежелательных эффектов. Одним из таких препаратов является азитромицин.
Азитромицин (Сумамед, «Pliva») — первый представитель новой группы макролидных антибиотиков – азалидов. Он обладает широким спектром противомикробного действия. Связываясь с 50S-субъединицей рибосомы, азитромицин подавляет биосинтез белков микроорганизма. Препарат активен в отношении ряда грамположительных (S. pneumoniae, S. pyogenes, S. agalactiae, стрептококков групп С, F и G, Staphylococcus aureus и S. epidermidis) и грамотрицательных микроорганизмов (Haemophilus influenzae, Н. parainfluenzae и Н. ducreyi, Moraxella catarrhalis, Bordetella pertussis и В. parapertussis, Neisseria gonorrhoeae и N. meningitidis, Brucella melitensis, Helicobacter pylori, Gardnerella vaginalis), а также чувствительных анаэробных микробов (Clostridium spp., Peptostreptococcus spp. и Peptococcus spp.). Кроме того, азитромицин обладает активностью в отношении внутриклеточных и других микроорганизмов, в том числе Legionella pneumophila, Chlamydia trachomatis и С. pneumoniae, Mycoplasma pneumoniae, Ureaplasma urealyticum, Listeria monocitogenes, Treponema pallidum, Borrelia burgdorferi. Препарат не действует на грамположительные бактерии, устойчивые к эритромицину.
При приеме внутрь азитромицин хорошо всасывается и быстро распределяется, причем в тканях достигаются высокие концентрации антибиотика. Обладает длительным периодом полувыведения и медленно выделяется из тканей. Указанные свойства позволяют применять препарат один раз в сутки в течение 3 дней с высоким эффектом. Хорошее проникновение внутрь клеток и накопление в фагоцитах, с помощью которых азитромицин транспортируется к месту инфекции, способствуют в свою очередь повышению эффективности азитромицина. Выводится в основном с желчью в неизмененном виде, небольшая часть выводится почками.
Азитромицин высоко активен в отношении Н. pylori: его МПК90 составляет всего 0,5 мг/л, а процент штаммов Н. pylori, устойчивых к препарату, в популяции очень низкий – 3,7 % [4]. В другом исследовании была изучена чувствительность 106 штаммов Н. pylori к азитромицину. 8,5 % штаммов были расценены как устойчивые (МПК>16 мг/л), однако треть из них восстановили чувствительность к азитромицину в присутствии лансопразола [5]. Это очень важный результат, поскольку он демонстрирует наличие синергизма между азитромицином и лансопразолом — блокатором протонного насоса, который широко используется в схемах антихеликобактерной терапии.
Наиболее важным преимуществом азитромицина перед другими макролидами является его распределение в плазме крови, желудочной слизи, желудочном соке и ткани желудка после однократного приема. Так, изучая эти показатели у 27 больных раком желудка, которым назначали азитромицин в дозе 500 мг за 24, 48, 72, 96 и 120 ч до гастрэктомии, исследователи обнаружили увеличение концентрации азитромицина в желудочном соке на протяжении 73 – 96 ч до 2,0 мг/л. При этом в желудочной слизи концентрация азитромицина была в два раза выше и сохранялась на протяжении 120 ч после приема препарата. Еще более высокие концентрации азитромицина наблюдались в ткани желудка (в 10 раз выше, чем в слизи, и в 20 раз выше, чем в желудочном соке), они сохранялись на протяжении 24 ч и медленно уменьшались в течение 5 дней [6]. К подобным выводам пришли и другие исследователи, показавшие, что концентрация азитромицина в слизистой оболочке желудка существенно превосходит таковую в крови [7].
В другом исследовании у больных хроническим хеликобактерным гастритом, получавших тройную терапию пантопразолом, метронидазолом и азитромицином (1-й день 500 мг и 2 – 5-й дни по 250 мг), ежедневно определяли концентрацию азитромицина в ткани желудка и желудочном соке [8]. За весь период лечения, а также спустя три дня после окончания приема азитромицина концентрация его в ткани желудка была не меньше 0,25 мкг/г (рис. 1) и, по мнению авторов, соответствовала МПК90, азитромицина для Н. pylori. Результаты данного исследования исключительно важны, так как они являются основанием для разработки схем лечения с низкими дозировками азитромицина. Полученные данные показали, что препарат может быть эффективным даже в дозе 250 мг/сут, а использование низких дозировок препарата снижает риск нежелательных реакций и стоимость лечения.
Рис. 1.
Динамика концентрации азитромицина в слизистой оболочке желудка. (цит. по 8).
Еще одним фактором, снижающим эффективность антихеликобактерной терапии, является способность Н. pylori к паразитированию внутри клеток. Полагают, что персистирование Н. pylori в эпителиоцитах, париетальных клетках и фагоцитах предохраняет микроорганизмы от воздействия антибиотиков и приводит к рецидиву инфекции вскоре после терапии. При специальном изучении влияния азитромицина на внутриклеточно расположенные Н. pylori в трех различных клеточных линиях было показано, что препарат существенно уменьшает количество клеток с внутриклеточно персистирующими Н. pylori, а обработка этих клеток азитромицином и лансопразолом полностью блокирует этот феномен [9, 10].
Число клинических исследований, в которых изучалась эффективность азитромицина в лечении хеликобактерной инфекции, невелико, однако с каждым годом оно увеличивается, что свидетельствует о возрастающем интересе к препарату как компоненту тройной терапии. По данным W. Dohmen и R. Seelis (1998), с 1990 по 1997 год было проведено 19 исследований, в которых азитромицин изучался в качестве компонента антихеликобактерной тройной терапии [11]. Частота эрадикации Н. pylori в этих исследованиях составляла 47 – 94 %. Такой широкий интервал указывает на то, что довольно часто изучались новые схемы лечения с эмпирически подобранными дозировками и кратностью приема препарата. Это не удивительно, так как фундаментальные работы, посвященные фармакокинетике азитромицина в слизистой оболочке желудка и желудочном соке, а также важные исследования синергизма азитромицина с различными базисными препаратами в отношении Н. pylori появились лишь в последние 2—3 года.
Открытые неконтролируемые исследования показали, что однонедельная тройная терапия омепразолом, азитромицином и метронидазолом приводит к эрадикации Н. pylori в среднем в 75 – 85 % случаев и рубцеванию более 95 % язв (в случае язвенной болезни) через 4 недели от начала лечения, что соответствует эффективности стандартных схем тройной терапии с использованием кларитромицина [11, 12]. При сравнении эффективности однонедельных схем лечения пантопразол (40 мг 2 раза в сутки)+амоксициллин (1000 мг 2 раза в сутки)+кларитромицин (500 мг 2 раза в сутки) или азитромицин (500 мг/сут в течение 6 дней) оказалось, что схема лечения с кларитромицином обеспечивала эрадикацию Н. pylori у 81 % больных, а с азитромицином — у 78 % (различия недостоверны) [13].
Наиболее интересны данные, полученные при изучении низкодозировочных или укороченных по времени режимов тройной терапии с использованием азитромицина и лансопразола, учитывая уникальный синергизм между двумя препаратами. Так, в сравнительном исследовании однонедельной тройной терапии омепразол 40 мг/сут+кларитромицин 500 мг/сут + тинидазол 1000 мг/сут и терапии лансопразол 30 мг/сут 7 дней + азитромицин 500 мг/сут 3 дня+метронидазол 500 мг/сут 3 дня частота эрадикации Н. pylori существенно не различалась (93,3 и 91,2% соответственно) [14]. В другом исследовании у 160 больных сравнивалась эффективность однонедельной тройной терапии (омепразол 20 мг/сут + кларитромицин 500 мг/сут + тинидазол 1000 мг/сут) с ультракоротким режимом лечения (лансопразол 30 мг/сут 1 – 4-й дни лечения, азитромицин 500 мг/сут 2 – 4-й дни лечения, тинидазол 2000 мг однократно на 3-й день). Частота эрадикации Н. pylori составила 85,5 и 80,8 % соответственно, а язвы к контрольному сроку зарубцевались у 100 и 97,8 % больных (различия недостоверны) [15]. В открытом исследовании такая же схема лечения обеспечивала эрадикацию Н. pylori у 86,3 % больных [16]. Следует отметить, что частота побочных реакций при использовании коротких схем лечения примерно такая же, как при использовании стандартных схем антихеликобактерной терапии или даже ниже. Важнейшим их достоинством является снижение затрат на лечение больного. Так, если сравнить стоимость эквивалентных по длительности схем лечения с использованием кларитромицина и азитромицина, то стоимость последнего оказывается примерно вдвое ниже, а в схемах с низкими дозами и укороченными сроками применения – в три раза ниже.
Все это, безусловно, делает азитромицин (Сумамед) одним из наиболее привлекательных представителей группы макролидов для включения в схемы антихеликобактерной терапии. Необходимо проведение сравнительных контролируемых исследований по изучению эффективности таких схем лечения (особенно ультракоротких).
1. Рекомендации по диагностике Helicobacter pylori у больных язвенной болезнью и методам их лечения. Росс. журнал гастроэнтерологии, гепатологии и колопроктологии, 1998, 1, 105–107.
2. Current European concepts in the management of Helicobacter pylori infection. The Maastricht Consensus Report. Gut, 1997, 41, 8–13.
3. Ling Т., Cheng A., Sung J. et al. An increase in Helicobacter pylori strains resistant to metronidazole: a five-year study. Helicobacter, 1996, 1, 57–61.
4. Gosciniak G., Kovacic D., Przondo-Mordarska A. In vitro susceptibility of Helicobacter pylori strains to Azithromycin. In: Proceedings of the 8th European Congress of Clinical Microbiology and Infectious Diseases, Lausanne, Switzerland, 1997, 945 (abstract).
5. Trautmann M., Riediger C., Moricke A. et al. Combined activity of azithromycin and lansoprazole against Helicobacter pylori. Helicobacter, 1999, 4, 113–120.
6. Harrison J.D., Jones J.A., Morris D.L. Azithromycin levels in plasma and gastric tissue, juice and mucus. Eur. J. Clin. Microbiol. Infect. Dis., 1991, 10, 862-864.
7. Blandizzi C., Malizia Т., Gherardi G. et al. Gastric mucosal distribution and clinical efficacy of azithromycin in patients with Helicobacter pylori related gastritis. J. Antimicrob. Chemother., 1998, 42, 75–82.
8. Krichhoff R., Laufen Н., Schacke G. et al. Determination of azithromycin in gastric biopsy samples. Int. J. Clin. Pharmacol. Ther., 1999, 37, 361–364.
9. Rigo R., Holmberg M., Engstrand L. Eradication of intracellular Helicobacter pylori in multidrug resistant monocytes using azithromycin and lansoprazole. Gut, 1996, 39 (Suppl. 2), A10.
10. Hulten К., Cars O., Hjelm E. Engstrand L. In-vitro activity of azithromycin against intracellular Helicobacter pylori. J. Antimicrob. Chemother., 1996, 37, 483–489.
11. Dohmen W., Seelis R.E. The role of azithromycin in the treatment of Helicobacter pylori infection — a retrospective report. Infection, 1998, 26, 256–262.
12. Vcev A., Vceva A., Ivandic A. et al. Omeprazole and azithromycin with and without metronidazole in the eradication of Helicobacter pylori in duodenal ulcer disease. Lijecnicki Vjesnik, 1997, 119, 210–213.
13. Vcev A., Stimac D., Ivandic A. et al. Pantoprazole, amoxycillin and either azithromycin or clarithromycin for eradication of Helicobacter pylori in duodenal ulcer. Aliment. Pharmacol. Ther., 2000, 14, 69–72.
14. Caselli M., Trevisani L., Tursi A. et al. Short-term low-dose triple therapy with azithromycin, metronidazole and lansoprazole appears highly effective for the eradication of Helicobacter pylori. Europ. J. Gastroenterol. Hepatol., 1997, 9, 45–48.
15. Trevisani L., Sartori S., Caselli M. et al. A four-day low dose triple therapy regimen for the treatment of Helicobacter pylori infection. Am. J. Gastroenterol., 1998, 93, 390–393.
16. Trevisani L., Sartori S., Galvani F. et al. Evaluation of a new ultrashort triple therapy for Helicobacter pylori disease. Aliment. Pharmacol. Ther., 1998, 12, 1269–1272.
Сумамед® — Досье препарата
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
При язве желудка и двенадцатиперстной кишки врач назначает антибиотики для угнетения бактерии хеликобактер. Антибактериальные препараты при попадании в организм направленно угнетают размножение и жизнедеятельность патогенных микроорганизмов.

Язвенная болезнь желудка и двенадцатиперстной кишки — это хроническая патология с периодами стихания и рецидивов. Болезнь склонна к активному прогрессированию и вовлечению других органов желудочно-кишечного тракта в патологический процесс.
При язвенной болезни могут назначаться следующие антибиотики: Клацид СР, Макмирор, Пилобакт, Метронидазол, Тетрациклина гидрохлорид, Сумамед, Амоксициллин. Каждый препарат выписывается врачом и не допускается к использованию по личному усмотрению больного.
Тетрациклина гидрохлорид и Хеликоцин
Комбинированный антибиотик Хеликоцин (пенициллин+метронидазол) выпускается в форме овальных таблеток, покрытых оболочкой. В каждой из них содержится 500 мг метронидазола и 750 мг амоксициллина. Это лекарство целенаправленно используется в качестве эрадикационной терапии (удаление хеликобактер пилори) при хронических гастритах, язве.
Препарат противопоказан людям с повышенной чувствительностью к действующим веществам, в случае патологии нервной системы, аллергических реакций, при нарушении кроветворения, инфекционном мононуклеозе, в период беременности и кормления грудью.

Тетрациклина гидрохлорид относится к одноименной группе противомикробных средств, выпускается в таблетированной форме по 0,1 активного вещества. Оказывает бактериостатическое действие, то есть тормозит активность и дальнейшее размножение H.Pylori. Используется только в составе комплексного лечения заболеваний ЖКТ, противопоказан детям.
Не назначается:
- при беременности, в период лактации;
- при склонности к аллергически реакциям на тетрациклиновую группу;
- пациентам с почечной недостаточностью.
Сумамед и Пилобакт
Сумамед (азитромицин) – антибактериальное средство широкого спектра действия, которое также угнетает и атипичные бактерии. При язвенной болезни антибиотик проявляет свою активность по отношению к бактерии хеликобактер пилори, но не является препаратом первой линии.

Особенности препарата Сумамед:
- короткий терапевтический курс;
- хорошая переносимость лекарства;
- минимальный риск побочных реакций;
- возможность лечения детей и пожилых людей;
- назначается по одному грамму в течение 3-10 дней;
- выпускается в форме порошка, капсул, и таблеток.
Средство Пилобакт – это комплекс из омепразола, кларитромицина и амоксициллина. Они являются основой первой схемы эрадикационного лечения хеликобактерассоциированных воспалений желудка, язвенных поражений органов ЖКТ.
Упаковка препарата рассчитана на 1 курс лечения. Один блистер содержит одну капсулу и две таблетки, которые нужно принимать в определенное время.
Макмирор и Клацид СР
Антибиотик Клацид СР наиболее предпочтителен для комплексного лечения язвы желудка, 12-перстной кишки. Он дает стабильный и быстрый результат за короткий антибактериальный курс. Лекарство высокоактивно по отношению к основному возбудителю патологий – бактерии хеликобактер.
Преимущества средства:
- Клацид СР хорошо переносится пациентами;
- всасывается в желудок независимо от приема пищи;
- медикамент устойчив к кислой среде, безопасен и удобен в использовании;
- благодаря наличию различных лекарственных форм антибиотик с успехом применяется и в детской гастроэнтерологии.

Выпускается лекарство в таблетках продленного действия по 0,25 г. Также его можно применять для внутривенных инъекций (производится во флаконах для приготовления раствора).
Препарат Макмирор содержит активное вещество — нифурател. Лекарство имеет выраженное противогрибковое, антибактериальное, противопротозойное действие. Оно угнетает бактерию хеликобактер, потому успешно применяется для лечения язвенной болезни. Его разрешено назначать детям в случае воспалительных заболеваний органов пищеварительной системы. Хороший терапевтический эффект достигается за счет высокой эффективности и хорошей переносимости медикамента.
Антибиотики Макмирор и Клацид СР популярны в гастроэнтерологии, что обусловлено коротким сроком лечения и возможностью назначения детям.
Хиконцил и Биноклар
Хиконцил имеет действующее вещество — амоксициллин, оказывает выраженное антибактериальное действие. Препарат можно назначать детям и взрослым, а также во время вынашивания плода. Целью назначения антибиотика является полное уничтожение бактерии хеликобактер.
Это современный вариант лечения язвенной болезни, который уже показал свою высокую эффективность. Выпускается в виде капсул и порошка для приготовления раствора. Одна капсула содержит 0,25 или 0,5 г амоксициллина.

Препарат Биноклар содержит в себе кларитромицин, выпускается в гранулах для приготовления суспензии, капсулах и порошке. Показан детям старше 12 лет и взрослым, средний курс лечения составляет от 6 до 15 дней. Это макролидный антибиотик широкого спектра активности, который также воздействует на хеликобактер.
Антибактериальная терапия язвенной болезни включает назначение нескольких препаратов для усиления действия.
Метронидазол
Метронидазол считается одновременно противомикробным и противопротозойным средством. Продается в таблетках по 500 мг. С успехом используется в составе тройной терапии против хеликобактерной инфекции, хотя многие врачи стали отмечать рост резистентных к метронидазолу штаммов бактерий.
Не назначается:
- при снижении лейкоцитов, эпилепсии;
- во время кормления грудью, в период беременности;
- при поражениях ЦНС, детям до 3-х лет.
Недостатки антибактериальных препаратов
Основным минусом антибактериальных препаратов является наличие риска побочных реакций. При их длительном приеме можно наблюдать изменения со стороны кишечника и нервной системы. Может появляться головокружение, галлюцинации, спутанность сознания, апатия, депрессия, судороги.
Возможные побочные эффекты:
- нарушение со стороны желудочно-кишечного тракта – диарея, дисбактериоз;
- аллергические реакции;
- нарушение работы почек и печени (при необоснованно длительном и бесконтрольном приеме, без перерыров).
Лечение антибиотиками при заболеваниях печени должно постоянно контролироваться специалистами.
Понравился материал: оцени и поделись с друзьями
Источник