Шок при хроническом панкреатите
Панкреатический шок является одним из самых опасных осложнений острого панкреатита. Наиболее часто он развивается на фоне некроза поврежденных тканей поджелудочной железы. Такое состояние характеризуется нарушением работы важных органов и систем организма, а также тяжелой интоксикацией.
Опасность панкреатического шока состоит в том, что практически в половине случаев он приводит к летальному исходу даже при условии современно оказанной медицинской помощи.
Что означает панкреатический шок?
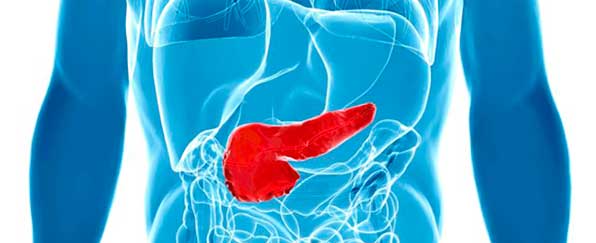
Панкреатический шок – очень тяжелое состояние организма, которое развивается вследствие осложнения острого панкреатита, чаще всего на фоне некроза значительного объёма тканей поджелудочной железы, и сопровождается снижением артериального давления, нарушением кровоснабжения, функционирования важных органов.
Такое состояние характеризуется критической недостаточностью кровоснабжения всех органов и тканей.
Самым опасным процессом при панкреатическом шоке является попадание в кровоток бактериальных токсических веществ, которые с кровью разносятся по всему организму и приводят к развитию эндотоксинового шока.
Именно такое осложнение считается основной причиной смертельного исхода при панкреатическом шоке.
Шок при остром панкреатите обычно развивается на фоне тяжелого, деструктивного течения болезни, которое сопровождается некротическим поражением значительного объёма тканей поджелудочной железы. Именно объем некроза считается основным критерием при расчете риска развития панкреатического шока.
В медицине выделяют ранний и поздний виды шока.
| Вид | Сроки | Особенности |
| Ранний шок | Зарождается на третьи сутки развития тяжелых деструктивных процессов, вызванных некрозом тканей и недостаточностью поджелудочной. | Основными причинами его появления является отмирание тканей ПЖ, просачивание поджелудочных ферментов и жидкости в рядом находящиеся органы, кровоток. |
| Поздний панкреатический шок | Когда на фоне некротических поражений железы в органе начинаются гнойные процессы, развивается сепсис. Такие процессы, в основном, развиваются на третью-четвертую неделю осложнения острого панкреатита некрозом тканей. | Основными возбудителями сепсиса считаются золотистые стафилококки и синегнойные палочки. Такое состояние считается очень опасным для жизни человека, потому что при попадании токсических продуктов патогенных микроорганизмов в кровоток происходит общая интоксикация и поражение всего организма. |
Симптоматическая картина

Острый некрозный панкреатический шок приводит к развитию деструктивных процессов во всем организме. Однако особенно негативно он отображается на кровообращении. Основными симптомами панкреатического шока являются:
- Повышенная (свыше 120 уд/мин) или пониженная (до 70 уд/мин) частота сердцебиения.
- Прогрессирующее снижение давления, не восприимчивое к общепринятой терапии.
- Централизация и децентрализация кровообращения, резкое снижение объёма циркуляции крови, неуправляемая гипотония.
- Холодные руки и стопы, цианоз кожных покровов.
- Острые болевые ощущение в области живота и подреберья.
- Тошнота.
- Рвота, не дающая облегчения.
- Повышенная температура.
- Обезвоживание.
- Небольшое количество выделения мочи.
- Отечность в области живота.
При позднем панкреатическом шоке может наблюдаться высокая (больше 38) или низкая (ниже 36) температура, критическая гипотония. Частота дыхания больше 20 вдохов-выдохов в минуту, частота сердечных сокращений больше 90 раз в минуту. Болевые ощущения очень выражены, пациент даже может потерять сознание.
В случае проявления симптомов панкреатического шока нужно немедленно вызывать скорую помощь, так как это состояние опасно для жизни человека.
Механизм развития патологического состояния
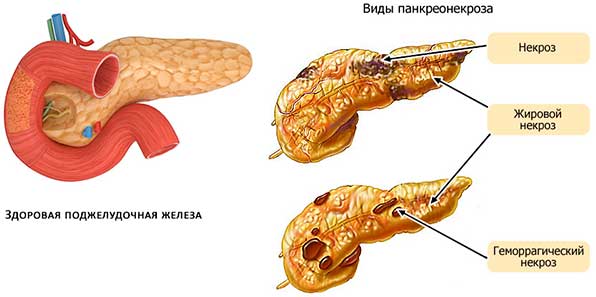
Шок при остром панкреатите, в основном, развивается вследствие некротического поражения большого объема тканей паренхимы поджелудочной железы, токсического воздействия на организм активированных в ней ферментов и патогенных бактерий. Так же отмечается:
- При ОП по причине отечности, спазмирования поджелудочного протока, забивания его желчью, пищеварительные ферменты не могут попасть в кишечник, поэтому они активизируются в железе и начинают ее разрушать. Со временем, поврежденные клетки поджелудочной отмирают, загнивают, вызывая развитие инфекционных процессов, сепсиса (заражение крови).
- Недостаточность поджелудочной, ферментный токсикоз и сепсис становятся причиной тяжелых деструктивных изменений в кровообращении и работе органов сердечно-сосудистой системы, что приводит к развитию панкреатического шока.
- Болевой шок, который развивается вследствие усиления выраженности болевых ощущений, приводит к сужению сосудов. Поэтому кровь начинает обильно прибывать к сердцу и головному мозгу. Вследствие сужения сосудов органы и ткани недополучают кислород, нарушается работа легких и мочевыделительной системы.
- Почки не могут продуцировать мочу, что приводит к отечности всех внутренних органов.
По причине обширного разрушения клеток поджелудочной содержащаяся в ней жидкость выходит в рядом находящиеся органы, а ферменты начинают разрушать кровеносные сосуды:
- Липаза и протеаза, воздействуя на стенки кровеносных сосудов, приводят к повышению их проницаемости, плазмопотерям, сгущению крови, отечности.
- Трипсины разрушают эритроциты.
Организм теряет жидкость, закупориваются сосуды, в них образуются тромбы. Повышенная свертываемость крови приводит к понижению общей кровяной циркуляции, неконтролируемому снижению артериального давления, нарушению работы сердца.
Причиной развития позднего панкреатического шока, самого опасного для жизни, является сепсис. Загнивание отмерших тканей поджелудочной приводит к развитию инфекционного процесса. Когда патогенные микроорганизмы и токсические продукты их жизнедеятельности попадают в кровеносную систему, развивается сепсис, который приводит к серьезной интоксикации всего организма. Как результат – поздний эндотоксивый панкреатический шок.
Неотложная помощь при приступе
Если приступ шока застал больного дома, ему нужно обеспечить покой. Человека следует уложить на ровную поверхность и вызывать скорую помощь. До приезда врачей важно соблюдать следующие правила:
- Пострадавшему нельзя давать никакое питье, еду, обезболивающие или другие лекарства.
- На область живота можно положить грелку либо бутылку с холодной водой, обмотанный тканью лед. Это немного уменьшит выраженность болевых ощущений.
- Важно помочь больному успокоится и расслабится, так как напряжение мышц живота, нервные переживания еще больше усиливают боль и дестабилизируют кровообращение, работу сердца.
Госпитализация и купирование приступа
Пациент с панкреатическим шоком подлежит госпитализации. В отделении экстренной помощи лечение такого состояния направлено, прежде всего, на:
- Очистку организма и крови от токсинов.
- Восполнение потерь жидкости.
- Восстановление кислотно-щелочного баланса.
- Нормализация вязкости, кислотности, химического состава крови.
- Снижение выраженности болевых ощущений и спазмов.
- Предупреждение развития инфекции.
С целью постепенного выведения из организма токсических веществ, устанавливается дренажная система. Если нужно очистить желудок, проводится зондирование. Также осуществляются меры по очистке крови от токсинов при помощи сорбентов.
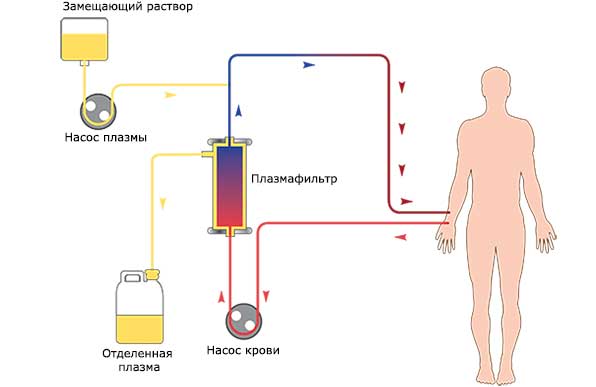
При необходимости может быть произведена:
- гемофильтрация (пропускание крови через гемофильтр с внутривенной ифузией замещающего раствора);
- плазмаферез (забор крови, ее очищение и возвращение обратно).
Эти процедуры также направлены на очистку крови от токсинов. Следует отметить, что сорбенты используются преимущественно на стадии панкреатического некроза, а при уже развитом шоке проводят гемофильтрацию или плазмоферез. Комбинация данных методик позволяет снизить риск летального исхода почти на 28%.
Для нормализации водного, кислотно-щелочного баланса, состава крови пациенту инфузионно вводят лекарственные растворы:
- Белково-электролитные потери восполняют при помощи коллоидных и кристаллоидных средств. Они также помогают нормализовать циркуляцию крови.
- С целью уменьшения выраженности болевых ощущений колют обезболивающие, спазмолитики.
- Для предупреждения развития либо дальнейшего распространения инфекционного процесса назначаются антибиотики.
- При необходимости дополнительно назначаются препараты, разжижающие кровь и предупреждающие образование тромбов.
В последнее время наиболее эффективным методом лечения септического шока считается детоксикация с параллельным введением иммуноглобулинов (например, Пентаглобин, Интраглобин, Лобулин). Иммуноглобулины подавляют жизнедеятельность инфекций и бактерий, что способствует быстрому купированию инфекционного и воспалительного процесса.
В первые дни лечения пациенту показано абсолютное голодание. В тяжелых случаях его могут перевести на искусственное питание.
Дальнейший прогноз
Патологическое состояние развивается у 9-22% пациентов.
Исследования также показали, что некротические процессы в поджелудочной вызывают стремительное снижение иммунитета. Число летальных исходов на фоне раннего панкреатогенного шока в среднем достигает 48%, а для поздней формы шокового состояния характерна повышенная частота развития осложнений – от 24 до 72%.
Загрузка…
Источник

Среди большого количества осложнений острого панкреатита выделяется тяжелое состояние, называемое панкреатогенным шоком.
Даже на современном этапе развития медицины, этот патологический процесс имеет высокую смертность: 48% среди ранних летальных исходов.
Подробную информацию о данном состоянии вы можете почитать ниже.
Что такое панкреатогенный шок?
Панкреатогенный шок – патологический процесс, возникающий в результате массивного поражения поджелудочной железы, сопровождающийся падением артериального давления (АД), снижением объема циркулирующей крови (ОЦК) и стойкими нарушениями гемодинамики в результате действия эндотоксинов.
Эндотоксинами в данном случае являются ферменты поджелудочной железы. Их действие на ткани органа является ключевым звеном патогенеза.
Симптомы
Среди симптомов панкреатогенного шока выделяют:
- резкое падение АД;
- кожные покровы бледные, холодные, покрыты липким потом (только вначале);
- острую боль в эпигастральной области;
- снижение ОЦК;
- нитевидный пульс;
- понижение вязкости крови;
- рвота;
- олигоурия, анурия;
- возможна полная непроходимость кишечника;
- нарушения психики: психомоторное возбуждение, бред, галлюцинации.
Следует обратить внимание на неспецифичный характер симптомов. Они свойственны и для других шоковых состояний, прободных язв и перитонита, из-за чего возможно ошибиться с диагнозом.
Причины возникновения
 К этиологическим факторам панкреатогенного шока относятся злоупотребление алкоголем, переедание.
К этиологическим факторам панкреатогенного шока относятся злоупотребление алкоголем, переедание.
Так же его развитию предшествует острый панкреатит.
Острый панкреатит – токсическое воспаление поджелудочной железы, возникшее в результате действия на железу ее собственных ферментов.
Патогенез:
Обильный прием пищи вызывает гиперстимуляцию железы, провоцируя высвобождение большого количества активных панкреатических ферментов, которые в норме должны быть неактивны. Преждевременная активация возникает в результате заброса желчи в выводящий проток железы.
В норме, желчь находится в просвете двенадцатиперстной кишки и взаимодействует с поджелудочным соком после его секреции в дуоденальное пространство. Заброс желчи возможен из-за частичной закупорки выводящего протока или разницы давления.
Активные ферменты начинают переваривать клетки железы, разрушая их мембраны и мембраны органоидов, в том числе лизосом. После деструкции мембран, лизосом, — происходит выход лизосомальных ферментов, которые лишь усугубляют процесс самопереваривания.
 Среди действующих ферментов наиболее важны:
Среди действующих ферментов наиболее важны:
- липазы – расщепляют липиды в составе клеточной мембраны;
- трипсин – активирует внутриклеточные ферменты;
- эластаза – расщепляет белки на аминокислоты.
Под действием алкоголя спазмируется сфинктер выводящего протока, что затрудняет отток ферментов с поджелудочным соком.
При ранней диагностике, панкреатогенный шок возможно отличить от других заболеваний, зная что симптоматика проявилась после приема пищи или алкоголя.
Аутолиз панкреатических клеток приводит к некрозу ткани, а соответственно и ее воспалению. Эти факторы обуславливают болевой синдром при панкреатогенном шоке. Воспалительный процесс сопровождается выделением медиаторов воспаления. В частности гистамин, кинины и гранулоцитарные белки, увеличивают проницаемость стенки сосудов микроциркуляторного русла. Начинается активный выход жидкости из просвета сосудов в прилежащие ткани, что на начальных этапах проявляется отеком железы.
При распространении в крови медиаторов воспаления, экссудация тканей приобретает массивный характер. Происходит потеря жидкости, кровь сгущается, возникает стаз с последующим сладжем и тромбозом. Тяжелым осложнением является ДВС-синдром, характеризующийся, распространенным по всему организму, свертыванием крови в микроциркуляторном русле. Кроме того, из-за обильной экссудации уменьшается ОЦК, падает АД, уменьшается сила сердечного выброса, пульс становится нитевидным.
 Чрезмерная болевая импульсация активирует симпато-адреналовую систему.
Чрезмерная болевая импульсация активирует симпато-адреналовую систему.
Адреналин суживает сосуды периферии и полости живота, обеспечивая обильный приток крови к жизненно важным органам – сердцу и головному мозгу.
Сужение остальных сосудов приводит к гипоксии тканей, лишенных нормального притока крови. Развиваются синдромы «шоковых» органов:
Не смотря на учащенное дыхание в качестве адаптационного механизма при гипоксии, кислород поступает в недостаточном количестве из-за нарушенного кровообращения, это приводит к образованию «шокового легкого». Дыхательная недостаточность приводит к гибели больного, если ему вовремя не оказана помощь.
Почки, не получая необходимого количества крови, не способны образовывать мочу, либо образуют, но в малом количестве и темного цвета – синдром «шоковой почки»
Кожа становится бледной, потоотделение происходит лишь вначале, когда потеря жидкости еще незначительна.
Отсутствие ферментов в двенадцатиперстной кишке приводит к остановке пищеварительного процесса. Клинически, застой в ЖКТ проявляется рвотой и кишечной непроходимостью.
 Существует несколько видов шоковых состояний и все они носят критический характер. Токсический шок встречается редко, но несет опасность для жизни человека.
Существует несколько видов шоковых состояний и все они носят критический характер. Токсический шок встречается редко, но несет опасность для жизни человека.
Что такое фокальная эпилепсия и как она проявляется, читайте тут.
Инсульт потенциально может развиться у каждого человека. Кома после геморрагического инсульта — крайне тяжелое состояние, которое может привести к смерти или тяжелой инвалидизации. Эта тема https://neuro-logia.ru/zabolevaniya/insult/gemorragicheskij/koma.html подробно описывает данное состояние.
Лечение
Лечение панкреатогенного шока включает в себя:
- Восполнение утраченной жидкости и компенсация ацидоза, путем введения противошоковых жидкостей. Восстанавливает реологические свойства крови: вязкость, химический состав, рН.
- Адекватное обезболивание. Необходимо для снижения активности симпатической системы и восстановления нормального тонуса сосудов.
- Дезинтоксикация.
- После перенесенного шока показано голодание.
- Установление дренажей для удаления токсических веществ.
- Зондирование желудка при необходимости его прочищения.
- Резекция органа. Объем удаляемой части поджелудочной железы зависит от площади ее поражения.
Панкреатогенный шок, как крайне тяжелое состояние, несет за собой множество поражающих факторов.
Действие большинства из них невозможно прекратить без оказания незамедлительной квалифицированной медицинской помощи. Ранняя диагностика и своевременная помощь – единственное, что на данный момент позволяет максимально снизить летальность патологии.
 Потеря человеком крови в количестве 10-40% от общего объема носит название геморрагический шок. От каких механизмов зависит тяжесть шока и насколько эффективно лечение опасного для жизни состояния, читайте на нашем сайте.
Потеря человеком крови в количестве 10-40% от общего объема носит название геморрагический шок. От каких механизмов зависит тяжесть шока и насколько эффективно лечение опасного для жизни состояния, читайте на нашем сайте.
Возможно, следующая тема будет интересной для вас — каковы шансы человека выжить при обширном инсульте головного мозга?
Видео на тему
Источник
Приступы боли в животе, подташнивание, метеоризм и диарея — одни из симптомов, которые могут встретиться при воспалении поджелудочной железы, или панкреатите. Но иногда проявления этой болезни совсем нетипичны и могут напоминать симптоматику аппендицита или даже сердечного приступа. Об отличительных признаках панкреатита, его формах, диагностике и лечении мы и поговорим в статье.
Симптомы панкреатита
Проявления панкреатита, как и его последствия для организма, зависят от формы заболевания. Острый панкреатит протекает стремительно и угрожает развитием необратимых изменений в структуре поджелудочной железы. Панкреатит в хронической форме — это воспалительное заболевание, протекающее с периодами обострений и ремиссий. По мере прогрессирования болезни железистая ткань замещается соединительной, что приводит к недостатку ферментов и, как следствие, сбоям в работе пищеварительной системы.
Острый панкреатит (ОП)
Первый и основной признак острого панкреатита — это боль. Как понять, что причина — воспаление поджелудочной, а не невралгия или почечные колики, например? Болевые ощущения при панкреатите очень сильные, стойкие. Они не проходят после приема спазмолитиков и обезболивающих. Обычно боль возникает в верхней части живота, отдает в спину, опоясывает тело. Часто возникает после приема алкоголя или острой жирной пищи.
Приступ, как правило, сопровождается тошнотой и рвотой, потом к ним присоединяются вздутие живота и жидкий стул. В 80–85% случаев острого панкреатита симптомы этим и ограничиваются, и болезнь проходит в течение недели. Это проявления ОП легкой степени, так называемого интерстициального или отечного панкреатита. У 15–20% больных ОП может переходить в среднюю степень с различными осложнениями: инфильтратом вокруг поджелудочной, образованием абсцессов и псевдокист, некрозом участков железы и последующим присоединением инфекции. Острый панкреатит тяжелой степени, который часто развивается при панкреонекрозе, сопровождается интоксикацией и поражением многих органов.
Опасность ОП еще и в том, что он может маскироваться под другие заболевания. В одном из исследований[1] был сделан вывод, что первые признаки панкреатита были типичными только у 58% пациентов. У других же ОП имел какую-либо «маску».
- В 10% случаев панкреатит проявлялся в виде печеночной колики (боли в правом подреберье) и даже желтухи.
- У 9% больных ОП начинался как кишечная колика — боли в нижней части живота.
- Еще 9% случаев имитировали приступ стенокардии или инфаркт — боль ощущалась выше, отдавала за грудину и под лопатку, иногда возникала одышка.
- Около 6% эпизодов ОП были похожи на приступ аппендицита.
- Другие 6% сопровождались резкой болью и напряжением стенки живота, как при перфорации желудка или кишечника.
- Наконец, 2% приступов панкреатита были похожи на острую инфекцию — с повышением температуры, головной болью, слабостью, тошнотой, рвотой и диареей.
Иногда симптомы сочетались или вообще проявлялись очень слабо. Во всех этих случаях для того, чтобы отличить панкреатит, потребовалось дополнительное обследование.
Хронический панкреатит (ХП) и его обострения
Лишь 10–20% пациентов переносят ХП в безболевой форме, у остальных 80–90% он проявляется типичным болевым приступом. Причем наблюдается два сценария. Первый, или тип А, — это короткие болевые приступы, повторяющиеся на протяжении десяти дней (не дольше), с последующими долгими безболевыми периодами. Второй, или тип В, чаще встречается при хроническом алкогольном панкреатите и представляет собой более долгие и тяжелые приступы боли с перерывами на один–два месяца. При обострении панкреатита симптомы обычно напоминают симптоматику острого процесса. Кроме этого, ХП сопровождается признаками дефицита панкреатических ферментов, о которых мы поговорим дальше.
Причины панкреатита
В целом ОП и ХП возникают под действием схожих факторов. Так, для острого панкреатита причины распределяются следующим образом[2]:
- лидирует злоупотребление алкоголем: 55% случаев ОП вызваны передозировкой спиртных напитков, а также неправильным питанием. Еще необходимо отметить, что нарушение диеты и алкоголь могут провоцировать обострение;
- на втором месте (35%) — попадание желчи в поджелудочную железу (острый билиарный панкреатит);
- 2–4% приходится на травмы поджелудочной, в том числе из-за медицинских вмешательств;
- остальные 6–8% случаев — отравление, аллергии, инфекции, прием лекарств, различные болезни пищеварения.
Причины хронического панкреатита наиболее точно отражены в специальной классификации TIGAR-O. Она была предложена в 2001 году и представляет собой первые буквы всех пунктов: Toxic-metabolic, Idiopathic, Genetic, Autoimmune, Recurrent and severe acute pancreatitis, Obstructive[3].
- Токсико-метаболический панкреатит связан с неумеренным употреблением спиртного (60–70% случаев), курением, приемом лекарств, нарушением питания и обмена веществ.
- Идиопатический панкреатит возникает по непонятным причинам и нередко сопровождается отложением кальция в поджелудочной железе.
- Наследственный панкреатит развивается, например, при мутациях в генах панкреатических ферментов.
- Аутоиммунный панкреатит вызван атакой собственного иммунитета на клетки железы, может идти в союзе с другими аутоиммунными болезнями.
- В хроническую форму может перейти повторяющийся или тяжелый острый панкреатит.
- Обструктивный панкреатит возникает при нарушении оттока желчи и секрета поджелудочной. Причиной может быть камень в желчном протоке, опухоль, аномалия развития.
Причины появления панкреатита могут различаться, но механизм развития всегда похож. Дело в том, что поджелудочная железа вырабатывает сильные ферменты, способные расщеплять поступающие с пищей белки, жиры и углеводы. Но из похожих соединений состоит и организм человека. И чтобы не произошло самопереваривание, существуют механизмы защиты: в поджелудочной железе ферменты находятся в неактивной форме, и работать они начинают только в двенадцатиперстной кишке, которая покрыта специальной слизистой оболочкой (как и вся внутренняя поверхность кишечника).
При панкреатите эта защита, как правило, не срабатывает (речь не идет о некоторых хронических формах, когда железа сразу подвергается склерозу или фиброзу). И в ситуации, когда ферментов слишком много, или они не могут выйти в кишечник, или имеют генетический дефект, происходит превращение из проферментов в активную форму, которая и рушит собственные клетки поджелудочной железы. Дальше происходит лавинообразная реакция: чем больше клеток погибает, тем больше из них при гибели высвобождается ферментов, которые тоже активируются. При этом железа отекает, возникает боль, а вслед за ней и все остальные проявления панкреатита.
Это важно
При ежедневном употреблении от 60 до 80 миллилитров алкоголя в течение 10–15 лет практически со стопроцентной вероятностью разовьется хронический панкреатит. Курение усугубляет действие спиртного, а наследственность, пол и другие факторы только определяют предрасположенность к болезни. Поэтому в любом случае врачи советуют отказаться от сигарет и злоупотребления алкоголем.
Диагностика панкреатита
Своевременное выявление и лечение панкреатита поможет избежать множественных осложнений. При возникновении «классических» симптомов на фоне приема алкоголя, нарушения питания или наличия камней в желчном пузыре стоит незамедлительно обратиться к гастроэнтерологу. Диагностика панкреатита, как правило, начинается с осмотра, опроса пациента, после чего назначают ряд дополнительных исследований.
- Лабораторные анализы. При подозрении на ОП специалисты могут назначить анализ крови или мочи. В крови можно обнаружить повышение активности ферментов, которые попадают туда при гибели клеток поджелудочной железы. В первую очередь это амилаза и липаза. Диагноз подтверждается, если норма превышена в три раза и более. Также можно определить амилазу в моче, иногда этот анализ называют диастазой. В случае ХП повышение ферментов практически не выявляется. Кстати, лабораторная диагностика панкреатита помогает подтвердить недостаточность работы поджелудочной, но об этом мы поговорим отдельно.
- Ультразвуковое исследование. Его преимущество — доступность, минус — в необходимости подготовки к исследованию, которая заключается в строгой диете на протяжении двух–трех дней. При панкреатите УЗИ-диагностику можно проводить и без подготовки, но тогда из-за наличия газов в кишечнике поджелудочную железу будет почти не видно. Также результат сильно зависит от возможностей УЗИ-аппарата и квалификации специалиста.
При ОП можно обнаружить увеличение размеров железы, снижение эхогенности и нечеткость контуров, а также наличие свободной жидкости в брюшной полости. Для диагностики ХП гораздо эффективнее эндоскопическое УЗИ, но его проведение требует оборудованного эндоскопического кабинета.
Трансабдоминальное УЗИ (через поверхность живота) при хроническом процессе имеет меньшую чувствительность и специфичность. Так, диффузные изменения в поджелудочной железе, трансформация ее размеров и контура не позволяют подтвердить хронический панкреатит. Диагноз подтверждают такие признаки, как псевдокисты или кальцинаты в поджелудочной железе, значительное расширение протока железы, уплотнение его стенок и наличие в нем камней. - Рентгенограмма брюшной полости — пожалуй, самое недорогое и доступное исследование. Рентгенограмма может помочь отличить кишечную непроходимость или обнаружить камни в желчном пузыре, что косвенно способствует постановке диагноза, но для определения панкреатита этот метод далеко не так информативен. В этом случае самым достоверным из рентгенологических методов является МСКТ — мультиспиральная компьютерная томография.
- Компьютерная томография при остром панкреатите обычно выполняется в сложных случаях, на 4–14 день болезни. КТ помогает найти очаги панкреонекроза, оценить состояние забрюшинной клетчатки, увидеть изменения в грудной и брюшной полости. Часто диагностику проводят накануне операции. О наличии хронического панкреатита говорят такие показатели, как атрофия железы, расширение протока и присутствие в нем камней, кисты внутри и вокруг железы, утолщение внешней оболочки. Косвенными признаками будут увеличение размеров железы, ее нечеткий контур или неоднородный рисунок.
- Еще один часто используемый метод при подозрении на острый панкреатит — диагностическая лапароскопия. Это хирургическая операция, которая позволяет достоверно оценить состояние органов в брюшной полости, а при необходимости сразу поставить дренаж или перейти к расширенному вмешательству.
Симптомы и диагностика ферментной недостаточности поджелудочной железы
Кроме самого панкреатита, обследование может обнаружить его последствия. Одним из основных будет нехватка ферментов поджелудочной железы, то есть экзокринная панкреатическая недостаточность. Что же она собой представляет?
Поджелудочная железа уникальна тем, что способна одновременно к внешней и внутренней секреции. Внешняя секреция — это выделение ферментов для пищеварения в кишечник, а внутренняя секреция — это выброс гормонов в кровь. В результате воспаления, некроза, склероза или наследственных болезней работа поджелудочной может нарушаться. И если повреждена эндокринная (гормональная) функция железы, у человека снижается уровень инсулина, что в конечном счете может привести к диабету. А если не работает экзокринная функция, то в кишечник не поступают панкреатические ферменты: амилаза, липаза и трипсин.
Памятка
Ферменты поджелудочной железы помогают переваривать почти все основные питательные вещества: трипсин расщепляет белки на аминокислоты, амилаза превращает сложные углеводы в простые ди- и моносахариды, а липаза отвечает за переваривание жиров.
Внешние признаки экзокринной недостаточности проявляются довольно поздно, когда уровень ферментов на 90–95% ниже нормы. В первую очередь виден дефицит липазы: нерасщепленные жиры выделяются с калом, стул становится жидким, жирным и частым. Такое состояние называется стеатореей. Также присутствует вздутие, метеоризм, возможны боли в животе, колики. Так как питательные вещества не перевариваются, они не могут усвоиться, и человек постепенно теряет вес. К тому же плохо усваиваются витамины. Их дефицит проявляется сухостью и шелушением кожи, ломкостью волос и ногтей и другими подобными симптомами. Обследование при ферментной недостаточности можно условно разделить на три направления:
- исследование трофологического статуса;
- определение содержания жира в кале;
- анализ активности ферментов.
Трофологический статус показывает, достаточно ли человек получает полезных веществ. Для этого определяют индекс массы тела, исследуют процентное соотношение жировой и мышечной ткани на специальных весах или измеряют толщину подкожно-жировой складки. Дефицит питания можно оценить и по анализам крови, которые показывают уровень общего белка, альбумина, гемоглобина, железа, витаминов и минералов.
Содержание жира в кале можно определить различными способами. Самый простой — это исследование кала под микроскопом при помощи окрашивания суданом III: капли нейтрального жира приобретают ярко красный цвет. «Золотым стандартом» считается определение количества жира в кале за 3–5-дневный период. В эти дни пациент ест специально подобранную пищу, содержащую ровно 100 граммов жира. Затем при анализе выясняют, сколько жира усвоилось, а сколько вышло. Если теряется более 15%, это подтверждает стеаторею. К сожалению, собирать и хранить кал три дня, потом везти его в лабораторию очень неудобно для пациента, а исследование такого количества кала технически сложно для лаборатории.
Самым логичным при диагностике ферментной недостаточности является измерение активности ферментов. Во-первых, с помощью зонда можно получить для анализа секрет поджелудочной железы. При этом выделение ферментов стимулируют или пищей, или уколом стимулятора. Во-вторых, можно выяснить активность ферментов по продуктам их работы. Так, существует дыхательный триолеиновый тест, который определяет метаболиты жира в выдыхаемом воздухе, а также бентирамидный тест, при котором продукты распада бентирамида обнаруживаются в моче. Наконец, третий путь — это определение ферментов в кале. Искомые ферменты должны быть стабильными и проходить через кишечник без изменений. Одна из методик — измерение содержания химотрипсина: его количество будет значительно снижено при нарушениях экзокринной функции. Наиболее часто в настоящее время используется тест на определение активности эластазы 1 с помощью иммуноферментного анализа.
Помимо соблюдения специальной диеты, исследования, как правило, требуют отмены ферментных препаратов, но все зависит от решения лечащего врача.
Клинические эффекты ферментных препаратов
«Формулу» лечения острого панкреатита легко запомнить — это «голод + холод + покой». Так, постельный режим помогает снизить болевые ощущения, прикладывание холода уменьшает нагрузку на железу, а благодаря временному отказу от пищи снижается выработка ферментов и, как следствие, уменьшается разрушение клеток, воспаление и отек.
К лечению можно добавить обезболивающие средства и спазмолитики. Из специфических препаратов врач может назначить гормон соматостатин, который подавляет собственную секрецию поджелудочной железы.
При стихании обострения пациент постепенно возвращается к полноценному питанию, и тогда ему могут назначить ферментные препараты. В настоящее время их существует довольно много, условно можно выделить несколько групп:
- препараты из слизистой оболочки желудка, содержащие пепсин;
- препараты, содержащие панкреатические ферменты — амилазу, трипсин, липазу;
- ферменты растительного происхождения, например папаин;
- другие протеолитические ферменты, например гиалуронидаза;
- комбинированные препараты.
Из них для заместительной терапии подходит группа панкреатических ферментов. Они могут различаться по активности, типу оболочки и размеру гранул. Специалисты Российской гастроэнтерологической ассоциации рекомендуют[4] обратить внимание на следующие моменты:
- препарат должен иметь кишечнорастворимую оболочку. Без нее ферменты потеряют свои свойства под действием кислого желудочного сока;
- препарат в виде гранул лучше перемешивается с пищевыми массами, чем целая таблетка, и действует эффективнее;
- принимать капсулы лучше во время приема пищи или сразу после него, запивать следует нещелочными напитками.
Эффект от приема ферментных препаратов оценивается врачом по трофологическому статусу. Но и сам пациент, как правило, чувствует ослабление вздутия и метеоризма, отмечает уменьшение тяжести в животе и нормализацию стула.
Обычно ферментные препараты переносятся хорошо, частота побочных эффектов в сумме — менее 1%. Среди них встречаются аллергические реакции, тошнота и рвота, диарея и запор. Одним из специфических побочных эффектов является повышение уровня мочевой кислоты при при?


