Морфологические изменения при хроническом панкреатите
© Хронический панкреатит — Маев И.В., Казюлин А.Н., Кучерявый Ю.А. / 2004 год. Патоморфология хронического панкреатита.
Прижизненное морфологическое исследование ПЖ (биопсия) производится редко ввиду трудности забора материала, обусловленной глубоким забрюшинным расположением органа и опасностью травматизации с возможностью активации ферментов и угрозой самопереваривания отдельных участков вокруг пункционного хода. Однако возможности современных методов диагностики, направленных на визуализацию структуры ПЖ, позволяют довольно точно судить о различных морфологических изменениях в ПЖ [2].
Возникающие при хроническом панкреатите морфологические изменения ткани ПЖ не являются только воспалительными. В развитии поражения ПЖ, эпизодов обострения ХП может иметь значение большое число самых разнообразных этиологических факторов, в то время как морфогенез хронического панкреатита в значительной мере однотипен.
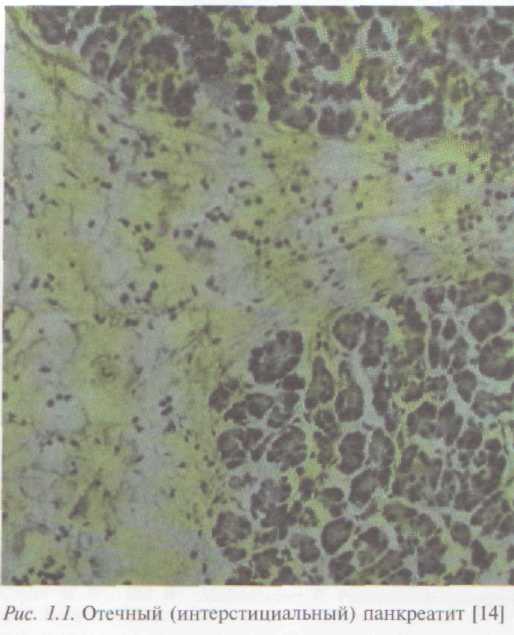
По мнению Н. Б. Губергриц и Т. Н. Христич, острый и хронический панкреатит обладают общностью этиопатогенеза, острый панкреатит может переходить в хронический, хронический часто сопровождается обострениями, особенно на ранних стадиях заболевания [2]. Поэтому морфологически острый панкреатит (или обострение хронического) характеризуется преобладанием альтеративных и экссудативных процессов (рис. 1.1). Легкие формы протекают с серозным воспалением (отечный панкреатит), которое может закончиться выздоровлением, рассасыванием экссудата и возвратом к норме или организацией его с появлением очагов фиброза. Хронический панкреатит характеризуется воспалением ПЖ с постепенно нарастающей гибелью, атрофией паренхимы и склерозом (фиброзом) стромы (рис. 1.2). ХП может протекать с обострениями, каждое из которых усугубляет эти процессы, или без них.
В начальном периоде заболевания патологический процесс может носить ограниченный характер и не распространяться на всю железу, что позволило подразделить ХП по локализации на левосторонний, локализующийся в хвосте; правосторонний, локализующийся в головке; парамедиальный, занимающий среднюю часть железы; диффузный, с поражением всех отделов органа [11]. Следует отметить, что последний вариант является исходом заболевания.
При ХП в патологический процесс вовлекаются все структуры ПЖ — ацинусы, островковый аппарат, протоковая система, сосуды, нервный аппарат, интерстициальная ткань.
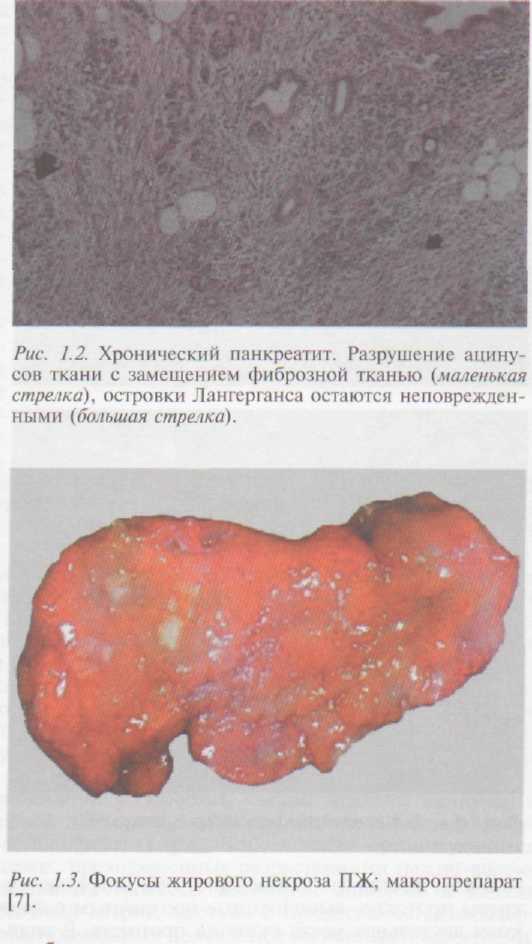
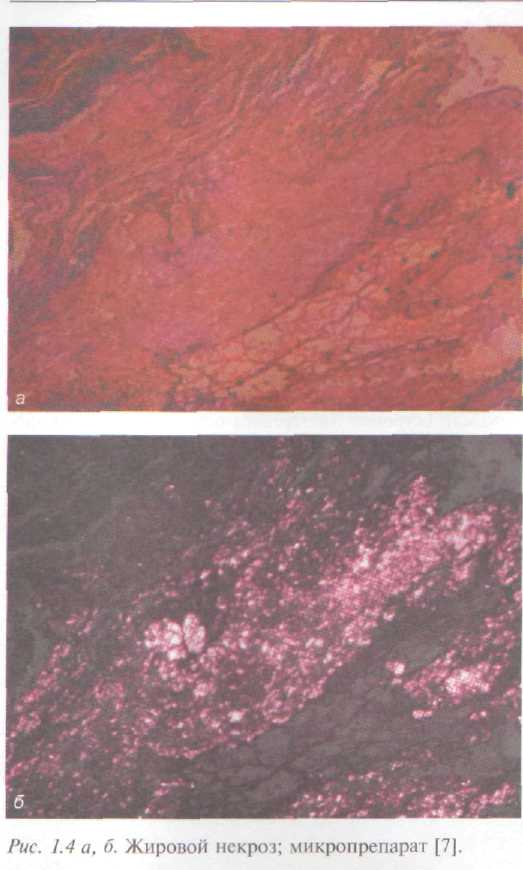
Макроскопически ПЖ чаще увеличена в размерах, плотная; фиброзная капсула склерозирована, местами под капсулой можно видеть старые фокусы жировых некрозов ярко-желтого цвета (рис. 1.З., 1.4). На разрезе: паренхима с обильными разрастаниями фиброзной ткани светло-серого цвета, подчеркнутым дольчатым рисунком. При вскрытии главного панкреатического протока, а также протоков первого порядка обращает на себя внимание неравномерное сужение и расширение их просветов, что соответствует области патологического процесса [7, 9].
Различают следующие разновидности расширения протоков [10]:
- глобальная дилатация;
- эктазия в области головки;
- биполярная эктазия;
- корпокаудальная эктазия;
- псевдокистозные изменения.
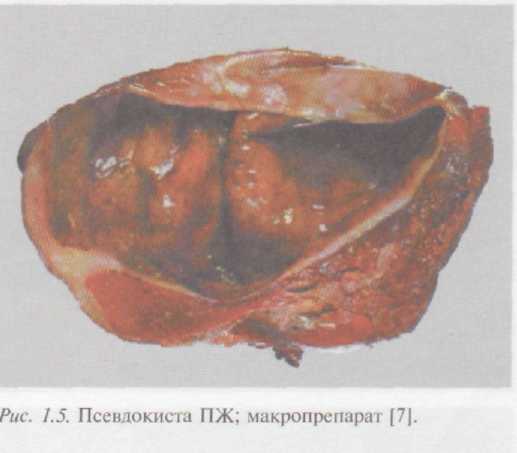
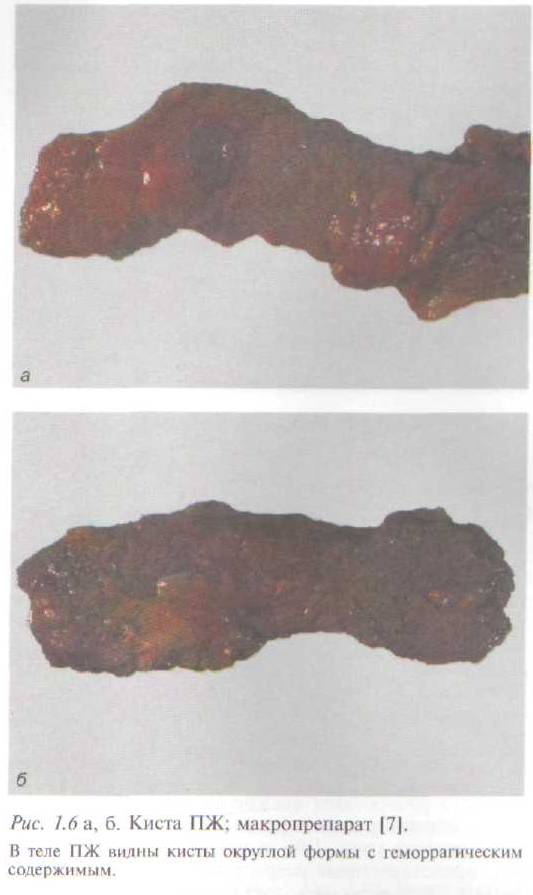
Поверхность железы может быть неровной за счет наличия в толще органа или в, подкапсульных отделах псевдокист (рис. 1.5), имеющих разное содержимое в зависимости от давности их образования. Содержимое относительно «свежих» кист представлено некротизированной тканью железы с примесью крови, богато протеоли-тическими ферментами; эпителиальная выстилка отсутствует. При нагноении содержимое кист мутное, серовато-зеленого цвета, иногда зловонное (рис. 1.6). Встречаются и мелкие ретенционные кисты протоков, выполненные прозрачным содержимым, которые образуются дистальнее места сужения протоков. В ряде случаев отмечается развитие пристеночного или обтурирующего тромбоза селезеночной артерии и вены.
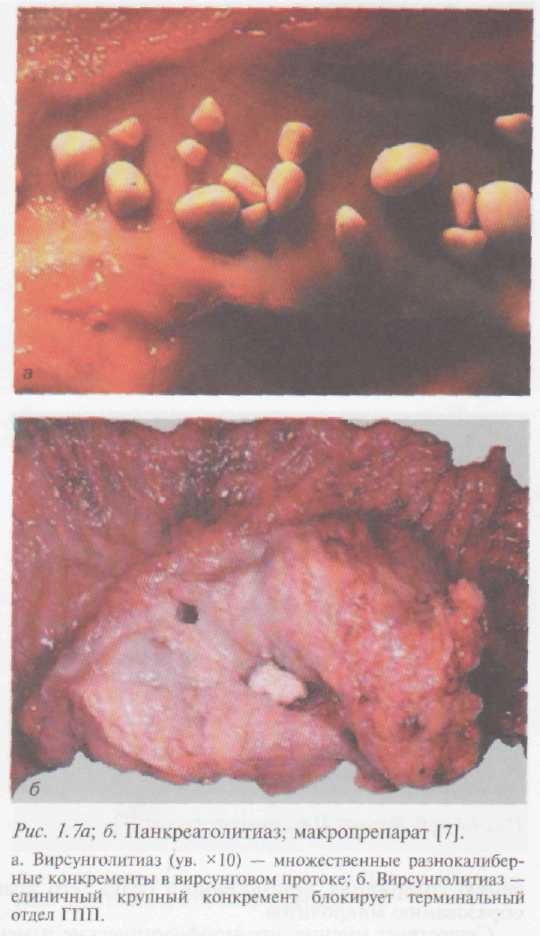
По прошествии нескольких лет от момента манифестации клинической симптоматики ПЖ бывает как увеличена в размерах, так и значительно уменьшена с выраженным склерозом капсулы и спаечным процессом на поверхности. Паренхима железы режется с трудом, в части случаев имеются отложения извести как в просвете протоков в виде формирования камней с зернистой поверхностью белесовато-желтого цвета (рис. 1.7), так и свободно лежащей среди разрастаний фиброзной ткани в местах бывшего некроза паренхимы. Обызвествление ткани ПЖ сочетается с рубцовой деформацией& железы. Количество экзокринной паренхимы значительно уменьшено, иногда она полностью отсутствует [9].
Основными гистологическими признаками являются прогрессирующая атрофия железистой ткани, распространение фиброза и замещение соединительной тканью клеточных элементов паренхимы поджелудочной железы. Существует мнение, что при различных этиологических вариантах ХП процесс начинается преимущественно в протоках ПЖ, фиброзная
трансформация дебютирует именно с этой структурной части органа [1]. В то же время рядом авторов подчеркивается значимость прогрессирующей атрофии и фиброзных изменений именно железистых элементов ПЖ [12,13].
Склеротические изменения ведут к нарушению проходимости протоков, внутрипротоковой гипертензии, прогрессирующим некрозам ацинарной ткани и образованию кист. Необходимо отметить, что кистозные изменения ткани ПЖ рассматриваются как конечный результат перенесенного острого панкреатита, а не как обязательный атрибут хронического [4].
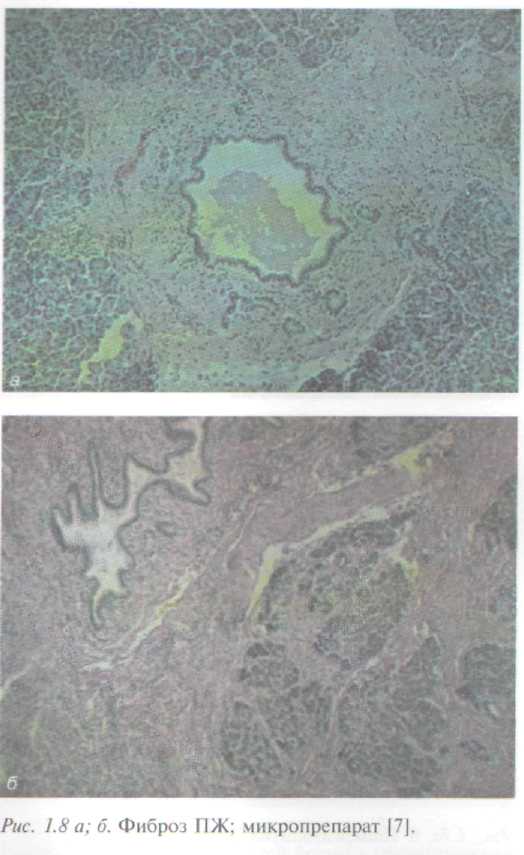
При гистологическом исследовании отмечают, что экзокринная паренхима представлена дольками неодинаковой величины, имеется много сформированных ложных долек за счет диффузного разрастания соединительной ткани между предсуществующими дольками и в толще их (рис. 1.8).
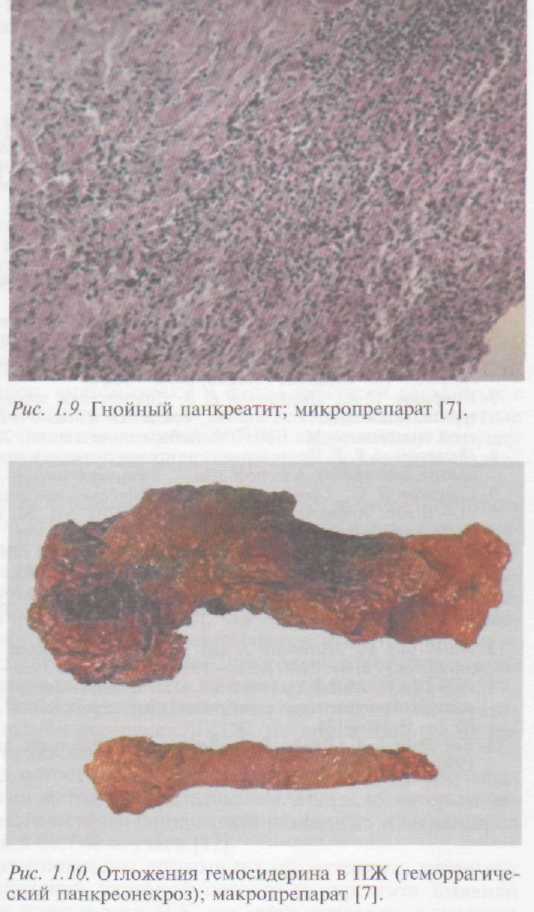
В толще долек неравномерно разбросаны свежие некрозы ацинусов и их групп с сегментоядерной лейкоцитарной инфильтрацией, иногда фокусы нагноения (гнойный панкреатит) (рис. 1.9), а также организующиеся фокусы некроза паренхимы, представленные разрастаниями нежно-волокнистой соединительной ткани. Просветы некоторых ацинусов и мелких протоков содержат клеточный детрит, местами с примесью сегментоядерных лейкоцитов. На фоне нормальных долек с неизмененными ацинусами, клетки которых богаты зимогенами, отчетливо видны дольки и их фрагменты, где клетки ацинусов дискомплексированы, лишены зимогенов. Цитоплазма таких клеток вакуолизирована, богата липидами; в некоторых клетках гранулы зимогена располагаются в базальных отделах, в отличие от апикальных в норме.
Строма органа представлена разрастаниями широких пластов соединительной ткани разной степени зрелости, местами молодой, отечной, расположенной в зонах некроза паренхимы, местами грубоволокнистой, инфильтрированной лимфоцитами, гистиоцитами, плазмоцитами и сегментоядерными лейкоцитами. Воспалительная инфильтрация распространяется и внутрь долек.
Встречаются свежие и старые очаги жировых некрозов.
Протоки всех калибров эктазированы в разной степени, содержат или жидкий эозинофильный секрет, или гноевидный. Стенки протоков с явлениями острого и хронического воспаления, очаговыми разрастаниями грануляционной ткани; эпителий уплощен, на отдельных участках изъязвлен [7, 9].
В паренхиме имеются отложения гемосидерина (рис. 1.10), свидетельствующие о прошлых кровоизлияниях. Венозные сосуды расширены, полнокровны. Наличие микроциркуляторных изменений типа микроангиопатий, дезорганизации базальных мембран капилляров, снижение транскапиллярного обмена позволяют считать сосудистый компонент одним из основных патогенетических факторов [6, 7).
При электронно-микроскопическом исследовании выявляются исчезновение микроворсинок в апикальных отделах протокового эпителия, десквамация эпителия в просвет протоков и гиперплазия с появлением многослойных структур [3]. Наряду с этим была отмечена перестройка протокового эпителия за счет появления очень высоких клеток циллиндрического эпителия с выраженной продукцией нейтральных мукополисахаридов.
Описана непроходимость панкреатических протоков, обусловленная метаплазией эпителия [8]. При этом возникает постепенная дегенерация ацинусов и замещение их соединительной тканью. В поздних стадиях заболевания процесс становится настолько выраженным, что нормальная ткань представлена островками, заключенными в каркас из грубой соединительной ткани. Наличие пролиферативных процессов в малых протоках и трудноразличимые микроскопически нормальные структуры ПЖ вызывают подозрение на наличие опухолевого процесса. Это в большей степени относятся к так называемой псевдотуморозной форме хронического панкреатита. Е. Б. Медвецкий и Т. А. Кадощук при электронно-микроскопическом исследовании ПЖ при хроническом псевдотуморозном панкреатите и раке ПЖ отметили полное отсутствие количественных различий между компартментами клеток протокового эпителия и злокачественными клетками. Это указывает на то, что бластоматозные клетки при дапьнейшей диффе-генцировке используют структурно-функциональный интеграл лротокового, а не ашшарного эпителия.
К. Richter (1981) при электронно-микроскопическом исследовании ацинозных клеток при экспериментальном панкреатите обнаружил, что при деструкции базальных мембран в ацинусах происходит тотальная или субтотальная гибель отдельных клеток, а при сохранении базальных мембран ацинарных клеток — метаплазия ацинарного эпителия, который по своему морфологическому состоянию становится промежуточным между ацинарной клеткой и протоковым эпителием. При этом получаются так называемые ацинодуктулярные структуры, которые при световой микроскопии имеют вид первичных выводных протоков (цит. по [9]).
Нервные стволы, проходящие в прослойках соединительной ткани, гипертрофируются, около них иногда обнаруживают воспалительные инфильтраты, нервные ганглии дистрофически изменены. Возможно, подобные изменения интрамуральнои нервной системы могут объяснить постоянный характер болей.
При кальцифицирующих панкреатитах строма представлена мощными разрастаниями соединительной ткани с умеренным хроническим воспалением, иногда воспалитель ная инфильтрация может полностью отсутствовать. Отмеча ется выраженная пе рестройка сосудов, как артериальных, так и венозных, в виде перекалибровки их просвета за счет раз растания и склероза внутренней оболочки. Гипертрофия нервных стволов увеличивается, дистрофические изменения нервных ганглиев нарастают, количество нервных клеток в них уменьшается. Еще большей перестройке подвергается протоковая система железы. Пальцевидные и «клапанные» выбухания фиброзной ткани стенок протоков почти полностью перекрывают их просвет, что приводит к нарушению оттока секрета. Повышенная десквамация протокового эпителия приводит к увеличению содержания незимогенного белка, его коагуляции и способствует образованию микролитов.
Существует мнение, что морфологические изменения при ХП алкогольной и билиарной этиологии имеют дифференциально значимые особенности [6]. Так, морфогенез алкогольного ХП состоит в нарушении белкового и энергетического обмена ацинарной клетки, снижении синтеза и накоплении секреторных гранул, деформации ацинусов за счет метаплазии ацинарных клеток в протоковые, эпителиально трубчатой деформации ацинусов с атрофией и гибелью этих структур. Характерны прогрессирующая атрофия ацинарной ткани с выраженным фиброзом органа, протоковая пролиферация с перидуктальным склерозом и нарушением дренажной функции, скопление густого секрета в кистозно расширенных протоках. Морфогенез билиарного ХП состоит в преимущественно липидно-жировой дистрофии ацинарных клеток при сохранении способности к синтезу ферментов в протоковую систему с застоем секрета и кистозным расширением центроацинарных протоков. Характерны повышенное содержание гранул зимогена в анинарных клетках с последующим снижением синтеза панкреатических ферментов, атрофия ацинарных клеток с протоковой метаплазией и их гибелью, заместительный склероз и липоматоз с незначительным перидуктальным склерозом крупных выводных протоков.
С течением времени количество островков в большинстве случаев уменьшается, что проявляется клинической картиной эндокринной недостаточности; размеры клеток сохранившихся островков и их ядер при этом увеличиваются, что следует расценивать как проявление компенсаторной гипертрофии [9].
По данным Ю.А. Нестеренко и соавт. [6] при атрофии ацинарной паренхимы эндокринная ткань ПЖ не только не подвергалась атрофическому изменению, а отмечалась гиперплазия островкового аппарата с обычным клеточным составом. В таких островках среди эндокринных клеток встречались ацинарные клетки с отсутствием четких мембран и секреторными гранулами, свойственными как эндокринным, так и экзокринным клеткам. В отдельных атрофичных дольках попадались крупные островки эндокринной ткани, иногда превышающие по размерам оставшиеся участки экзокринной ткани; в островках Лангерганса отмечалась неоднородность клеточного состава. В структуре отдельных островков частично или полностью преобладали крупные клетки со светлой цитоплазмой и пикнотичным ядром. По мнению авторов, такое разнообразие в Строении эндокринных клеток островков указывает на то, что у больных ХП преобладают не только процессы гиперплазии эндокринной ткани, но и изменяется их функциональная активность с гиперпродукцией различных гормонов.
СПИСОК ЛИТЕРАТУРЫ
- Багненко С. Ф. Диагностика и хирургическое лечение хронического билиарного панкреатита: Дис. … д-ра. мед. наук — СПб., 1998.— 328 с.
- Губергриц Н. Б., Христин Т. П. Клиническая панкреатология — Донецк: ООО «Лебедь», 2000.—416 с.
- Мажута П. М., Миннебаев М. М., Ерзин М. А. Роль лимфатической системы в патологии поджелудочной железы // Клин.мед.— 1972.— № 6.— С.6—18.
- Мараховский Ю. X. Хронический панкреатит. Новые данные об этиологии и патогенезе. Современная классификация. Успехи в диагностике и лечении // Русск. мед.журн.— 1996.-Т.4, № 3.- С.156-160.
- Медвецкий Е. Б., Кадощук Т. А. Функция и морфология поджелудочной железы при остром ее воспалении // Здравоохр. Белоруссии.— 1980.— № 8.— С.48—50.
- Нестеренко Ю. А., Глабай В. П., Шаповальянц С. Г. Хронический панкреатит: Монография.— М.: Издатель Мокеев, 2000,— 182 с.
- Панфилов С. А., Панфилова Е. В. Диагностика заболеваний печени, билиарного тракта, поджелудочной железы, селезенки и надпочечников с курсом патологической анатомии,— М.: БИНОМ. Лаборатория знаний, 2003.— 215 с.
- Пигаревский В. Е. Исследование эпителия поджелудочной железы (к проблеме метаплазии эпителиев): Автореф. дис. … канд. мед. наук.—Л., 1950.— 16 с.
- Саркисов Д. С, Саввина Т. В. Патологическая анатомия хронического панркеатита.— В кн.: Хронический панкреатит / Под ред. М. И. Кузина, М. В. Данилова, Д. Ф. Благовидова.— М.: Медицина, 1985.— С. 29—46.
- Czernobilsky В., Mikat К. The diagnostic significance of interstitial pancreatitis found at autopsy // Am. J. Clin. Pathol.— 1964.- Vol. 41,- P. 35.
- Leger L., Claret Y., Louvel A. Le canal de Wirsung dans les pancretites chroniques chirurgicales: etude radiologique et anatomique // Nouv. Presse Med.—1978.—Vol. 7.— P. 3115—3118.
- Mallet-Guy P., Michoulier J. Les pancretites chroniques recidivantes parenchymateuses primitives // Helv. Chir. Acta,— 1973.- Vol. 30.— P. 268-271.
- Puig-Divi V., Molero X., Vaquero E. et al. Ethanol feeding aggravates morphological and biochemical parameters in experimental chronic pancreatitis // Digestion.— 1999.—Vol. 60, № 2.- P. 166-174.
- Van Dyke J. A., Stanley R. J., Berland L. L. Pancreatic imaging // Ann. Intern. Med.— 1996.-Vol. 102.-P. 212-217.
Автор материала: Маев И.В., Казюлин А.Н., Кучерявый Ю.А.
Источник
Прижизненное морфологическое исследование ПЖ (биопсию) выполняют редко, что связано с трудностью забора материала, обусловленной глубоким забрюшинным расположением органа, опасностью его травматизации, сопровождающейся активацией ферментов и угрозой развития острого посттравматического панкреатита. Возможно проведение пункционной биопсии ПЖ под контролем УЗИ или КТ. В большинстве случаев её выполняют для дифференциальной диагностики индуративных панкреатитов и очагового поражения ПЖ (опухоли, паразитарное поражение, туберкулёз, очаговая форма аутоиммунного панкреатита и др.).
Разработаны критерии определения тяжести ХП по результатам УЗИ, КТ, ЭРХПГ, позволяющие с достаточной точностью определить выраженность структурных нарушений. При ОП риск от выполнения инвазивного вмешательства (пункции) значительно превышает диагностическую значимость морфологического исследования, особенно если принять во внимание высокую точность современных методов визуализации ПЖ и весь арсенал современных биохимических методов исследования (диагностика феномена уклонения ферментов в кровь, определения уровня экспрессии цитокинов и др.), позволяющих достоверно диагностировать ОП.
Необходимо отметить, что в большинстве случаев выполняют тонкоигольную биопсию ПЖ, позволяющую провести только цитологическое исследование, т.е. получить отдельные группы клеток, что неактуально для диагностики панкреатитов. Пункция ПЖ толстой иглой, позволяющая осуществить забор значительного количества материала для гистологического исследования, чрезвычайно травматична и грозит серьёзными осложнениями (деструктивный постманипуляционный панкреатит). Именно поэтому в настоящее время считают, что прямых показаний к проведению пункции ПЖ у больных панкреатитами нет.
Прижизненное морфологическое исследование проводят во всех случаях после резекции ПЖ, панкреатэктомии и открытой биопсии ПЖ. Подавляющее большинство исследований, посвященных изучению патоморфологии панкреатитов, выполнено на аутопсий ном материале.
Острый панкреатит
Первое систематическое описание морфологии ОП было сделано R. Fitz ешё в 1889 г. Спустя семь лет Н. Chiari выдвинул предположение, состоящее в оценке ОП как процесса самопереваривания.
При ОП возникают изменения в структуре ацинарных клеток и нарушение их функции, развивается острая местная и системная воспалительная реакция. Основой патоморфологических изменений при ОП считают повреждение ацинарных клеток, в результате которого возникает интерстициальный отёк. При этом ПЖ увеличивается в размерах, могут возникать небольшие зоны очагового некроза, располагающиеся как в самом органе, так и вокруг него (в забрюшинной клетчатке).
Острая воспалительная реакция прогрессирует достаточно быстро (в течение нескольких минут). Начальный иммунный клеточный ответ характеризуется периваскулярной полиморфноклеточной инфильтрацией в ПЖ. В течение часа начинается прогрессирующая миграция мононуклеарных лейкоцитов (включая макрофаги и лимфоциты) в очаг воспаления. Радикалы кислорода и другие вещества, выделяемые фагоцитами, усугубляют повреждения, воздействуя, в частности, на эндотелиальные клетки капилляров ПЖ. В результате увеличивается проницаемость сосудов, что облегчает доступ циркулирующим форменным элементам крови (нейтрофилам, моноцитам, тромбоцитам) и различным гуморальным факторам (например, компонентам комплемента и цитокинам) к микроокружению ацинарных клеток.
Микроскопически отёк может быть как интерлобулярным, так и интралобулярным. Скопления ацинарных клеток выглядят рассредоточенными и разделёнными прослойками сравнительно редкой соединительнотканной матрицы (см. рис. 4-1). Хотя ОП в большинстве случаев завершается благоприятно для больного и морфологически характеризуется только отёком, в 5—10% случаев он прогрессирует до панкреонекроза — необратимого локального процесса, в ряде случаев сопровождающегося полиорганной недостаточностью.

Рис. 4—1. Гистологические изменения при остром панкреатите (микрофотограмма): а — перидуктальная воспалительная реакция; б — воспаление ограничено периметром долек, видны небольшие очаги некроза
В этом случае возникает длительная нетрудоспособность, высока частота летальных исходов. Гистологически обнаруживают обширные некрозы паренхимы, зоны микроабсцессов, тромбоз в микрососудистом русле, очаговые кровоизлияния (см. рис. 4-2). Все указанные нарушения, как правило, прогрессируют из первичных отёчных изменений.

Рис. 4—2. Гистологические изменения при остром деструктивном панкреатите (микрофотограмма): а — панлобулярный некроз; б — острый геморрагический панкреатит; экзокринная ткань поджелудочной железы (слева) в значительной степени сохранена, в то время как прилежащая жировая ткань (в центре и справа) распадается, при этом видны только клеточные остатки и кровоизлияние. Некротизированный жир имеет сильное сродство к кальцию, который быстро откладывается в нём; базофилия некротизированной ткани (внизу) — показатель наличия кальция
При прогрессирующем ОП деструктивно-воспалительные изменения обнаруживают не только в ПЖ (собственно панкреатит), но и в забрюшинной клетчатке (парапанкреатит), брюшине (перитонит) и её связках (лигаментит), большом и малом сальнике (оментит), сальниковой сумке (оментобурсит), жировых подвесках толстой кишки (эпиплоит). Нередко панкреатические ферменты повреждают жёлчный пузырь, в результате чего возникает ферментативный острый холецистит.
В развитии морфологических изменений при прогрессирующем ОП выделяют четыре периода и восемь фаз (табл. 4-1). Начальными считают периоды альтерации паренхимы ПЖ с возможным формированием очагов некроза, что выражается интенсивной экссудацией в интерстиций органа, забрюшинное клеточное пространство (иногда с геморрагическим пропитыванием) и полость брюшины. Во втором периоде происходит тромбирование сосудов ПЖ и забрюшинной клетчатки с резким ослаблением и прекращением экссудации. Завершающая фаза второго периода морфологических изменений при ОП — образование некрозов и их эволюция.
Таблица 4-1. Периоды тканевой деструкции при остром панкреатите

За периодом образования очагов некрозов следует период реактивных изменений в них, приводящих к развитию перифокального воспаления. В его первой фазе наблюдают воспалительный отёк и инфильтрацию, а в последующих — ферментативное расплавление, инфильтрацию и секвестрацию некротизированных тканей. Присоединение эндогенной или экзогенной инфекции при неоправданных ранних хирургических вмешательствах на повреждённой ПЖ превращает зоны повреждения в очаги гнойно-гнилостного расплавления (нагноение клетчаточных пространств) и секвестрации. Если альтерация ПЖ и возникает в этих обстоятельствах, то её считают вторичной.
В периоде репарации структура паренхимы и функция ПЖ могут восстановиться полностью (отёчный панкреатит) либо частично, с формированием рецидивирующего панкреатита, свищей, псевдокист ПЖ или сочетанием этих изменений (см. рис. 4-3). В последнем случае возможно развитие функциональных нарушений

Рис. 4—3. Псевдокиста поджелудочной железы, возникшая в исходе острого панкреатита (фотография при лапаротомии): округлая полость с геморрагическим содержимым
В соответствии с клинико-морфологической классификацией выделяют различные морфологические формы ОП.
• Интерстициальный ОП:
— серозный;
— серозно-геморрагический.
• Некротический ОП:
— преимущественно жировой;
— преимущественно геморрагический.
• Гнойно-некротический ОП.
Указанные морфологические формы могут последовательно переходить друг в друга.
Под влиянием благоприятных факторов (например, раннего полноценного лечения уже на догоспитальном этапе) развитие морфологических изменений может остановиться на ранней стадии отёка и интерстициального ОП. При некротическом ОП в ранние сроки в ПЖ обнаруживают смешанный некроз с преобладанием геморрагического или жирового компонента (см. рис. 4-4). Происходит достаточно быстрая резорбция геморрагического компонента некроза.

Рис. 4—4. Смешанный панкреонекроз с преобладанием геморрагического компонента (макропрепарат): обширные зоны некроза паренхимы, фокусы кровоизлияний и небольшие очаги стеатонекроза
На поздних сроках обнаруживают преимущественно жировой некроз, который в асептических условиях рассасывается очень медленно. Эффективное лечение может предупредить переход некротической формы в гнойно-некротическую (наиболее опасную) и обеспечить быстрое наступление периода реституции.
Паренхиматозный некроз, характеризующийся преимущественным поражением ацинарных клеток, относят к разряду колликвационного. Обычно он протекает с выраженными геморрагическими изменениями не только в ПЖ и забрюшинной клетчатке, но и в отдалённых отделах брюшной полости. Некротизированные ткани при такой форме некроза быстро расплавляются, образуя гноевидную серую массу с большим содержанием протеолитических ферментов.
Жировой некроз (стеатонекроз) вызывает фосфолипаза. Чаще всего он возникает в условиях лимфостаза, нарастающего по мерс развития альтерации в ПЖ. Его обнаруживают как в самой ПЖ, так и в тканях, содержащих большое количество клетчатки, чаще — в забрюшинном пространстве и большом сальнике (см. рис. 4-5). Стеатонекроз, относящийся к разряду коагуляционного (сухого) некроза, вызывает резкую перифокальную воспалительную реакцию. В отличие от кровоизлияний стеатонекрозы рассасываются медленно, в местах их локализации образуются мелкие или крупные перифокальные инфильтраты. Массивные жировые некрозы могут вызывать реактивный асептический перитонит.

Рис. 4—5. Жировой некроз при остром панкреатите (макропрепарат при аутопсии): а — большие зоны некроза, захватывающие сальник и хвост поджелудочной железы; б — множественные просовидные фокусы стеатонекроза на брыжейке и сальнике
При тяжёлом течении прогрессирующего ОП наблюдают признаки системного воспалительного ответа или синдрома множественных органных дисфункций. Возникают панкреатогенные поражения сердца, лёгких, печени, почек и других органов.
Маев И.В., Кучерявый Ю.А.
Опубликовал Константин Моканов
Источник