Клинический случай хронического панкреатита
архив
подписка
Понедельник, 01 Май 2017 14:03
Хронический панкреатит (клинический случай)
Автор
Super User
УДК: 616.37-002-036.12:616.151: 577.152.321
Сайфутдинов Р.Г., Дворянкина Т.В., Хадеева В.З.,
Валитова Р.Р., Сайфутдинова Т.В.
ГБОУ ДПО КГМА Минздрава России. 420012, г. Казань, ул. Муштари, 11
ОАО «Городская клиническая больница №12». 420036, г. Казань, ул. Лечебная, 7
Хронический панкреатит (клинический случай)
Резюме: Хронический панкреатит – персистирующее воспаление поджелудочной железы, приводящее к ее фиброзу и стриктурам протока. Данные изменения снижают эндокринную и экзокринную функцию поджелудочной железы. В статье представлен клинический случай хронического панкреатита с атипичным течением – сохранение гиперамилаземии и гиперамилазурии на фоне клинического улучшения состояния больного.
Ключевые слова: панкреатит, гиперамилаземия, гиперамилазурия, клинический случай.
Контактное лицо:
Сайфутдинов Рафик Галимзянович
д.м.н., профессор, зав. кафедрой госпитальной и поликлинической терапии ГБОУ ДПО КГМА Минздрава России; 420073, г. Казань, ул. Муштари, 11; тел.: (843) 564-27-92,
Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Saifutdinov R.G., Dvorjankina T.V., Xadeeva V.Z.,
Valitova R.R., Saifutdinova T.V.
Kazan State Medical academy for Postdegree Education, 11 Mushtary street, 420012, Kazan, Russian Federation
City clinical hospital № 12. 7, Lechebnaja street, 420036, Kazan, Russian Federation
Сhronic pancreatitis (a clinical case)
Abstract. Chronic pancreatitis – the persistent inflammation of a pancreas leading to its fibrosis and strictures of a duct. These changes reduce endocrine and exocrine function of a pancreas. In article the clinical case of chronic pancreatitis with an atypical current – conservation of a hyperamylasemia and hyperamylasuria against clinical improvement of a condition of the patient is presented.
Keywords: pancreas, hyperamylasemia, hyperamylasuria, a clinical case
Contact person:
Saifutdinov Rafik Galimzijanovich
DM, professor, head of the chair of hospital and ambulatory therapy, Kazan State Medical Academy for Postdegree Education; 11 Mushtary St., 420012, Kazan, Russian Federation; tel.: (843) 564-27-92, e-mail:
Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Пациент З., 63 лет, в плановомпорядке поступил в гастроэнтерологическое отделение ОАО ГКБ №12 г. Казани 15.03.2016 с жалобами на ощущение тяжести в области эпигастрия, появляющееся после еды, вздутие живота, «тугой» ежедневный стул. Диспепсический синдром мало выражен. Аппетит сохранен. Имеется потеря веса на 10 кг в течение 2лет.
Anamnes morbi: Считает себя больным не менее 5 лет, когда появилась тяжесть в области эпигастрия после еды, «тугой» стул. Для купирования болипринималсамостоятельнокреон,но-шпу.Такжелечился стационарно по поводу обострений хронического панкреатита с положительным эффектом. Ухудшение состояния в течение недели, причины не знает. Обратился к участковому терапевту, былнаправлен на плановуюгоспитализацию.
Anamnes vitae: Перенесенные заболевания: простуда до 3-4 раз в год, в 2009 г проведеналевосторонняя нефрэктомия по поводу рака левой почки в Республиканском клиническом онкологическом диспансере (РКОД). Инфекционный гепатит, венерическиезаболевания, туберкулез, аллергические реакции отрицает. Гемотрансфузий не было. Наследственность не отягощена. Служил в пограничных войсках. Не работает. Группа инвалидности II бессрочная. Не курит, алкоголь не употребляет 1.5 года (ранее злоупотреблял). Женат, имеет 2-х здоровых детей. Отец и мать умерли, причину назвать не может. Братьев, сестер нет.
Status praesens objectives: Рост — 180см, вес- 93кг. Индекс массытела — 29. При поступлении состояние средней степени тяжести. Сознание ясное. Кожные покровы нормальной окраски. Высыпаний нет. Периферические лимфоузлы неувеличены. Отеков нет.Костно–мышечная система. Суставы внешне не изменены. Болезненности при пальпации мышц, суставов и костей нет.
Система органовдыхания. Дыхание через нос свободное. Форма грудной клетки нормостеническая. Перкуторный звук легочный. Дыхание везикулярное. ЧДД 16вминуту. Сердечно-сосудистая система. Область сердца не виднеизменена. Перкуторно относительные границы сердца не расширены. Тоны сердца нормальной звучности, ритмичные, шумов нет. ЧСС –84уд/ мин. АД 130/80 мм.рт.ст. Пульсация на периферических сосудах сохранена. Шумов на них нет. Система органов пищеварения. Язык влажный, обложен белесоватым налетом по всему языку. Зев интактен, зубы санированы. Живот ассиметричный, имеется послеоперационный рубец по белой линии живота. Положительные симптомы Боде (локальное вздутие брюшной стенки в надчревной области), Керте (регидность передней брюшной стенки в надчревной области в проекции поджелудочной железы), Раздольского (болезненность при перкуссии над поджелудочной железой), Махова (гиперестезия выше пупка). Печень по М.Г.Курлову — 10х8х7см, селезенка по В.П.Образцову — 6х8см. Стул оформленный, ежедневный, с предшествующим натуживанием.
Система органов мочевыделения. Область почек визуально не изменена. Симптом Ф.И. Пастернацкого отрицательный с обеих сторон. Мочеиспускание безболезненное, диурез в норме.
Данные лабораторных и инструментальных методов исследования (в скобках указаны принятые в клинике нормы) до госпитализации.
ОАК 10.03.2016: Эритроциты: 4,4×1012/л (3.3–5.5 ×1012/л); Гемоглобин: 137 г/л (120-140г/л); Цветовой показатель — 0,94 (0.86–1.05); Лейкоциты: 6,0 ×109/л (4 -8 ×109/л); СОЭ-11 мм/час; Лейкоформула: П/я — 2% (4%); С/я — 63% (63%); Лимфоциты – 25% (26%); Моноциты — 6% (6%); Эозинофилы — 4% (2%); ОАМ от 10.03.2016: цвет светло– желтый, прозрачная, удельный вес — 1012 (1008–1016), Реакция кислая, белок отрицательный, лейкоциты единичные в поле зрения (1-2-3), эритроциты 0 в поле зрения, эпителий плоский единичный в поле зрения (1-2-3).
Биохимический анализ крови от 10.03.2016: Билирубин общий — 10,2 (5-21мкмоль/л); Билирубин прямой — 1,1 (до 3,4мкмоль/л); Билирубин непрямой — 9,1 (1,7-17мкмоль/л); Глюкоза крови — 8,2 (3,3-5,5ммоль/л); Мочевина крови — 6,8 (2,8-7,2ммоль/л); Общий холестерин — 6,4 (до 5,2ммоль/л), β — липопротеиды — 3,67 (до 3,3ммоль/л); амилаза крови — 201 (22-80ед/л); липаза – 85 (<60ед/л); АЛТ — 17 (<=40ед/л); AST – 20 (<=40ед/л), общий белок — 74,8 (66-83г/л), щелочная фосфатаза — 56 (30-120 МЕ/л), креатинин крови — 99 (59-104 мкмоль/л). Кал на я/глист от 10.03.2016 — не обнаружены. МРП от 10.03.2016 — отрицательно. ЭКГ от 10.03.2016: Ритм синусовый с ЧСС — 68 уд/мин. Положение ЭОС нормальное.
Был выставлен предварительный диагноз: Хронический панкреатит, средней степени тяжести, непрерывно рецидивирующее течение, болевая форма. Левосторонняя нефрэктомия.
Назначено лечение: омепразол (ультоп) 20 мг + натрия хлорид 0.9% — 200 мл внутривенно капельно №2; метоклопрамид 0.5% — 2,0 внутримышечно №2, затем по 10 мг 3 раза в день перорально; ферментный препарат (панкреатин) 25000 ЕД 3 раза в день во время еды, перорально; метамизол натрия + питофенон + фенпивериния бромид (спазмалин) 5,0 внутримышечно в 21:00 №3.
В течение недели вышеуказанные жалобы сохранялись 23.03.16 после дуоденального зондирования отмечал двукратный жидкий стул без патологических примесей.
Данные лабораторных и инструментальных методов исследования, проведенные в стационаре.
α-амилаза мочи 16.03.2016 08: 16:00: — 225 (42-321е/л);
α-амилаза сыворотки крови 23.03.2016: — 247 (22-80е/л);
α-амилаза мочи 23.03.2016: — 410 (42-321е/л);
Сахарная кривая 25.03.2016: 8ч:00 — 5,4ммоль/л; 11ч:00 — 4,7ммоль/л; 13ч:00 — 7,2ммоль/л; Ат к ВГС и HBs-Ag от 15.03.2016 — не выявлены.
Флюрография от 26.03.2015 (ОАО «ГКБ № 12») — органы грудной клетки в норме.
Копрограмма 16.03.2016: Форма и плотность кала: неоформленный; цвет светло-коричневый; слизи нет, крови нет, гноя нет; крахмал ++; остатки растительной пищи 1-4; бактерии +; дрожжевые клетки +; яйца глист, паразиты, цисты лямблий не обнаружены; соскоб на энтеробиоз (острицы) и реакция Грегерсена – отрицательна.
Фракционное дуоденальное зондирование 22.03.2016: признаки гипомоторной функции желчного пузыря.
УЗИ гепатобилиарной системы 16.03.2016. Печень: правая доля — 149 мм (до 120мм); Левая доля — 74 мм (до 60мм); контуры ровные; эхогенность — норма; эхоструктура — однородная; внутрипеченочные желчные протоки не расширены; сосудистый рисунок не изменен; желчный пузырь: размеры: 72х28мм (70х30мм); стенки уплотнены; содержимое негомогенное; холедох — 4мм (до 5мм); поджелудочная железа: размеры — не увеличены; контуры ровные; эхогенность повышена; эхоструктура однородная; воротная вена — 9мм (менее 12 мм); селезеночная вена — 5мм (до 6 мм); селезенка: размеры: 104х43мм (до 100х50 мм); контуры: ровные; структура однородная.
Фиброгастродуоденоскопия (ФГДС) диагностическая 17.03.2016. Пищевод: свободно проходим на всем протяжении, слизистая нормальная, кардиальный жом смыкается полностью. Желудок: содержит желчь в небольшом количестве, слизистая антрального отдела гиперемированная, складки не утолщены, привратник проходим, луковица двенадцатиперстной кишки без особенностей. Заключение: поверхностный гастрит. Дуодено-гастральный рефлюкс.
25.03.16. Консультирован зав. кафедрой госпитальной и поликлинической терапии КГМА, главным гастроэнтерологом МЗ РТ проф. Сайфутдиновым Р.Г. Учитывая жалобы пациента, анамнез жизни, повышенный уровень липазы крови, амилазы крови и мочи, копрограммы, данные инструментальных исследований выставлен диагноз: хронический панкреатит, рефлюксный, обострение. ЖКБ. Хронический гастрит тип «С», ДГР, обострение. Т.к. у больного имеется повышение уровня липазы крови, но соотношение клиренсов амилазы (клиренс а) и креатинина (клиренск) – 2,49 (<4%), т.е. норма, макроамилаземия мало вероятна. Рекомендовано провести КТ брюшной полости для уточнения плотности камней по Хаунсфилду для решения вопроса о медикаментозной терапии ЖКБ.
Спиральная компьютерная томография органов брюшной полости с мультипланарной и трехмерной реконструкцией 28.03.2016. Протокол: аксиальные томограммы с реконструкцией 1,5мм. Выявленные изменения: печень с четкими ровными контурами, не увеличена, гомогенной структуры, денситометрические показатели составляют 43-70ед.HU. Внутри- и внепеченочные желчные протоки не расширены. Желчный пузырь 28х50мм, стенки не утолщены, уплотнены, содержимое неоднородное за счет наличия мелких включений плотностью 86ед.HU. Поджелудочная железа не увеличена, поперечный размер хвоста составляет 20мм, тела — 25мм, головки — 35мм. Плотность паренхимы от 66 до 79ед. HU. Структура не однородна за счет наличия жировых включений. Контуры железы ровные, четко дифференцируются на фоне парапанкреатической жировой клетчатки. Селезенка с четкими ровными контурами, не увеличена, однородной плотности. Надпочечники без особенностей. Почки: правая — обычной формы, размеров и положения, плотность паренхимы однородная. Конкрементов не выявлено. Полостная система не расширена. Левая почка удалена – рак левой почки. Абдоминальный отдел аорты обычного диаметра. Забрюшинные лимфоузлы не увеличены. Костно- деструктивных изменений на уровне исследования не определяется. Заключение: камни в желчном пузыре, состояние после левосторонней нефрэктомии.
28.03.16. На фоне проводимого лечения имеется положительная клиническая динамика: нет болевого синдрома, уменьшились проявления диспепсического синдрома, но сохраняется повышенный уровень амилаз крови и мочи.
30.3.16. В результате проведенного лечения пациент выписывается домой в удовлетворительном состоянии с рекомендациями. Необходим амбулаторный контроль уровня амилазы крови и мочи, наблюдение участкового терапевта. Рекомендован прием препаратов УДХК в дозе 10 мг/кг (всю дозу принимать на ночь). Контроль УЗИ желчного пузыря через 3 месяца для решения о дальнейшей тактике ведения.
Интерес к ферментемиям существует давно. Повышение уровня различных ферментов в крови и моче, например АЛТ, АСТ при патологии печени, КФК с ее фракциями при остром коронарном синдроме и мозговых ишемических атаках, уровень амилазы, липазы при панкреатитах и иных ситуациях требуют внимания клинициста. Это возникает либо из-за выхода ферментов из разрушенной ткани, либо из-за повышенной проницаемости клеточной мембраны, либо задержки ферментов мембраной почечного клубочка.
Данный клинический пример интересен тем, что у пациента с хроническим панкреатитом остался повышенный уровень амилазы в крови и моче при наступившей ремиссии болезни. Это не макроамилаземия (МАЕ). В 19б7 г. J.E. Berk и соавт. [3] описали 3-х пациентов с длительной бессимптомной гиперамилаземией и предложили термин «макроамилаземия» (МАЕ). По их мнению, данное состояние возникает вследствие присутствия в кровотоке активных в ферментном отношении макромолекулярных комплексов, включающих амилазу. Указанные комплексы вследствие большого размера плохо фильтруются почками и задерживаются в кровотоке, что подтверждалось высокой активностью амилазы крови и низкой активностью этого фермента в моче.
В литературе, периодически появляются работы о гиперамилаземии как при панкреатитах [10, 12, 11, 4, 1], так и других патологических состояниях. Ее описывают при ревматоидном артрите [2], целиакиях [5,6], СКВ [7], острой порфирии [9] и даже при беременности [8].
У нашего пациента более вероятная причина гиперамилаземии – воспалительный процесс, идущий в поджелудочной железе. На спиральной компьютерной томографии от 28.03.2016 в структуре поджелудочной железы обнаружены жировые включения. Возможно, при наличии ЖКБ (которая вероятнее всего и была причиной обострения панкреатита) при нарушении диеты возобновляется воспалительная реакция поджелудочной железы, что периодически и вызывает гиперамилаземию.
Литература1. Губергиц Н.Б. Макроамилаземия у больных с хроническим панкреатитом / Губергиц Н.Б., Голубова О.А. // Вопросы реконструктивной и пластической хирургии. – 2014. — №1(48). – С.75-80.
2. AokiA.Acasereportofmacroamylasemiawithrheumatoidarthritis/AokiA., Hagiwara E., Atsumi Y. et al. // Ryumachi. – 1989. – V. 29. – P.207–212.
3. BerkJ.E.Macroamylasemia//Bockusgastroenterology/Ed.W.S.Haubrich,F. Schaffner, J.E. Berk. – 5th ed. – Philadelphia: WB Saunders, 1995. – P.2851–2860.
4. ChoS.Y.Overlappingpresenceofmacroamylasemiaandhyperamylasemiain acute pancreatitis / Cho S.Y., Lee A., Lee H.J., Suh J.T. Overlapping // Korean J Lab Med. – 2011. – V. 31 (2). – P.98–100.
5. Deprettere A.J. Disappearance of macroamylasemia in a celiac patient after treatment with a gluten-free diet / Deprettere A.J., Eykens A., Van Hoof V. / J Pediatr Gastroenterol Nutr. – 2001. – V. 33 (3). – P.346–348.
6. Depsames R. Macroamylasemia as the first manifestation of celiac disease / Depsames R., Fireman Z., Niv E., Kopelman Y. // Case Rep Gastroenterol. – 2008.
– V. 2 (2). – P. 196198.
7. Goto H. Simultaneous macroamylasemia and macrolipasemia in a patient withsystemiclupuserythematosusinremission/GotoH.,WakuiH.,KomatsudaA. et al. // Intern Med. – 2000. – V. 39 (12). – P.1115–1118.
8.HeadleyA.J.Diagnosisofmacroamylasemiainapregnantpatient/HeadleyA.J., Blechman A.N. // J Natl Med Assoc. – 2008. – V. 100 (11). – P.1359–1361.
9. Hedger R.W. Transient macroamylasemia during an exacerbation of acute intermittent porphyria / Hedger R.W., Hardison W.G.M. // Gastroenterology. – 1971. – V. 60. – P.903–908.
10. MifflinT.E.Rapidquantitative,specificmeasurementofpancreaticamylase inserumwithuseofamonoclonalantibody/MifflinT.E.,BenjaminD.C.,BrunsD.E.// Clin Chem. – 1985. – V. 31 (8). – P.1283–1288.
11. Mifflin T.E. Interaction of immobilized anti-salivary amylase antibody with human macroamylases: implications for use in a pancreatic amylase assay to distinguishmacroamylasemiafromacutepancreatitis/Mifflin T.E.,ForsmanR.W., Bruns D.E. // Clin Chem. – 1989. – V. 35. – P.1651–1654.
12. Warshaw A.L. Puzzling persistent hyperamylasemia, probably neither pancreatic nor pathologic / Warshaw A.L., Hawboldt M.M. // Am J Surg. – 1988.
– V. 155. – P. 433–456.
Источник
В статье рассматриваются основные причины возникновения острого и хронического билиарнозависимого панкреатита и особенности его лечения. Проанализирован клинический случай острого билиарного панкреатита, развившегося на фоне лечения желчнокаменной болезни, с дальнейшим формированием хронического панкреатита в результате персистирования билиарного сладжа.
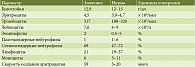
Таблица 1. Клинический анализ крови
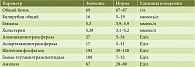
Таблица 2. Биохимический анализ крови
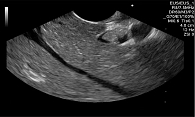
Замазкообразная желчь в терминальном отделе общего желчного протока
Как показали результаты ретроспективного (20-летний период) исследования, посвященного анализу причин развития острого панкреатита, билиарнозависимый панкреатит встречается у 26,9% пациентов [1]. Основной причиной его развития является желчнокаменная болезнь (ЖКБ). Острый панкреатит рассматривается как одно из основных осложнений ЖКБ [2].
Последние десятилетия во всем мире наблюдается тенденция к увеличению частоты развития билиарного панкреатита в результате роста заболеваемости ЖКБ [3]. Так, по данным разных авторов, частота развития билиарного панкреатита у больных ЖКБ составляет 25–90% [4].
Ведущим фактором в патогенезе билиарного панкреатита является повышение давления в желчных протоках вследствие возникновения механического препятствия (конкремент, билиарный сладж, стриктура, опухоль и др.), особенно дистальнее места слияния общего желчного с главным панкреатическим протоком, либо дисфункции сфинктера Одди. Развитие на этом фоне патологического билиопанкреатического рефлюкса и нарушение оттока панкреатического секрета могут привести к возникновению острого билиарного панкреатита [5].
Билиарнозависимый панкреатит отличается от панкреатита иной этиологии (алкогольный, алиментарный, посттравматический) тем, что этиологический фактор, как правило, не устраняется. Его воздействие продолжается на фоне развивающегося процесса в поджелудочной железе (ПЖ) и парапанкреатической клетчатке [6].
Особое значение в развитии билиарного панкреатита придается билиарному сладжу. Частота его выявления у больных с идиопатическим панкреатитом составляет 30–75%. При исследовании желчи в течение первых суток от начала панкреатической атаки билиарный сладж выявляется в 80% случаев [7].
В одном из исследований ученые наблюдали за 104 пациентами с билиарным сладжем в течение 630 дней (21 месяц). У 25 (24%) больных развились осложнения, такие как холелитиаз, холецистит, холедохолитиаз и панкреатит. При этом у 12 пациентов отмечался некалькулезный холецистит, у двоих – острый калькулезный холецистит. Зарегистрировано шесть случаев холецистолитиаза, один случай холедохолитиаза, четыре – панкреатита [8].
Таким образом, клиническое значение билиарного сладжа переоценить сложно, поскольку он:
- служит источником камнеобразования: желчные камни образуются у 5–20% пациентов за 1–3-летний период;
- способствует развитию стриктур терминального отдела общего желчного протока и/или стенозирующего папиллита;
- может приводить к развитию острого холецистита, холангита, отключению желчного пузыря (при наличии замазкообразной желчи);
- является причиной билиарного панкреатита.
Кроме того, билиарный сладж, содержащий микролиты, может свободно проходить по протоковой системе и вызывать необъяснимые боли в правом подреберье у 83% больных [9].
Билиарный сладж формируется в желчном пузыре в результате дестабилизации физико-химического состояния желчи и преципитации ее основных компонентов.
К факторам, способствующим персистенции билиарного сладжа, относятся гипотония желчного пузыря и гипертонус сфинктера Одди. Постоянный пассаж сладжа по желчным путям приводит к повреждению слизистой оболочки, главным образом в области сфинктера Одди. Травматизация слизистой оболочки вызвана микролитами, составляющими основную часть билиарного сладжа. Как следствие, сначала развивается вторичная дисфункция сфинктера Одди, затем формируется стенозирующий папиллит [4].
Помимо конкрементов и билиарного сладжа обострения панкреатита могут быть вызваны дисфункцией сфинктера Одди [10], в том числе у больных после холецистэктомии [11]. Так, у 18,8% пациентов с хотя бы одним эпизодом острого панкреатита или хроническим идиопатическим панкреатитом выявляется панкреатический тип дисфункции сфинктера Одди [11].
Фармакотерапия билиарнозависимого панкреатита может быть этиологической и патогенетической. При наличии показаний (ЖКБ, обструкция желчного потока) проводится эндоскопическое или хирургическое лечение.
Этиологическая терапия предполагает использование препаратов урсодезоксихолевой кислоты (УДХК). Патогенетическая зависит от типа преобладающих нарушений. При гипомоторных нарушениях назначают прокинетики (домперидон, итоприд), при гипермоторных – спазмолитики (мебеверин). Применяют также комбинированные препараты, оказывающие одновременно и холеретическое, и спазмолитическое действие.
По механизму действия спазмолитики подразделяют на нейротропные и миотропные. Нейротропные блокируют процесс передачи нервных импульсов в вегетативных ганглиях и нервных окончаниях, стимулирующих гладкомышечные клетки. Они осуществляют блокаду М1-, М2- и М3-холинорецепторов гладкой мышечной клетки. Среди нейротропных спазмолитиков выделяют:
- природные: атропин, гиосциамин, препараты красавки, платифиллин, скополамин;
- синтетические центральные: адифенин, апрофен, апринал, циклозил;
- полусинтетические периферические: гиосцина бутилбромид.
Миотропные спазмолитики уменьшают мышечный тонус за счет прямого воздействия на гладкомышечные клетки. К таким спазмолитикам относятся блокаторы ионных каналов, ингибиторы фосфодиэстеразы (ФДЭ) 4-го типа, нитраты. Миотропные спазмолитики подразделяют:
- на селективные:
- блокаторы кальциевых каналов (пинаверия бромид, отилония бромид);
- блокаторы натриевых каналов (мебеверин) и донаторы оксида азота (изосорбида динитрат, нитроглицерин, натрия нитропруссид);
- неселективные: ингибиторы ФДЭ (дротаверин, папаверин, аминофиллин, бенциклан) [12].
Что касается патогенетической терапии, препаратом выбора для пациентов с функциональными заболеваниями билиарного тракта являются лекарственные средства, селективно релаксирующие гладкую мускулатуру органов желудочно-кишечного тракта. Препараты этой группы, в частности мебеверин, обладают релаксирующей селективностью в отношении сфинктера Одди, в 20–40 раз превышающей эффект папаверина. При этом мебеверин оказывает нормализующее действие на мускулатуру кишечника, устраняя функциональный дуоденостаз, гиперперистальтику, спазм и не вызывая при этом нежелательной гипотонии [13].
Рассмотрим клинический пример, демонстрирующий результат успешного лечения билиарнозависимого панкреатита за счет назначения этиологической и патогенетической терапии.
Больная К. 76 лет была госпитализирована в отделение патологии поджелудочной железы и желчевыводящих путей Московского клинического научно-практического центра им. А.С. Логинова для обследования и лечения по поводу неоднократного обострения хронического панкреатита.
При поступлении – жалобы на боли в верхней половине живота с иррадиацией в спину и грудную клетку, усиливающиеся после еды, тошноту, отрыжку, снижение массы тела на 16 кг за два года.
Из анамнеза известно, что боли в животе впервые появились несколько лет назад. Больная была госпитализирована с болевым синдромом. Диагностированы холедохолитиаз, механическая желтуха. Проведены эндоскопическая папиллосфинктеротомия, экстракция конкремента холедоха, осложнившаяся панкреонекрозом. Проведено консервативное лечение. Через полгода отмечалось повторное ухудшение – интенсивный болевой синдром. Пациентка была вновь госпитализирована. Диагноз: хронический панкреатит, обострение. Через два года выполнена лапароскопическая холецистэктомия. В течение года боли не беспокоили, однако через год они возобновились. Последующие полгода пациентка с диагнозом «обострение хронического панкреатита, транзиторный холедохолитиаз» находилась на стационарном лечении.
При объективном осмотре состояние удовлетворительное, кожные покровы и видимые слизистые оболочки чистые, обычной окраски. Тургор снижен. Отеков нет. В легких дыхание везикулярное, хрипов нет. Тоны сердца приглушены, ритм правильный. Частота сердечных сокращений – 76 уд/мин. Артериальное давление – 120/80 мм рт. ст. Язык влажный, обложен белым налетом. Живот обычной конфигурации, в эпигастральной области и правом подреберье звездчатые рубцы. При пальпации живот мягкий, болезненный в эпигастральной области. Печень у края реберной дуги, селезенка не пальпируется.
Лабораторно-инструментальные исследования. Клинический анализ крови без патологических отклонений (табл. 1). В биохимическом анализе крови умеренный холестаз (табл. 2). Фекальная эластаза – свыше 200 мкг/г. Эзофагогастродуоденоскопия. Парапапиллярный дивертикул. Состояние после папиллотомии.
Ультразвуковое исследование органов брюшной полости. Признаки диффузного заболевания печени. Билиарная гипертензия. Расширение гепатикохоледоха. Не исключен холедохолитиаз, хотя конкремент не визуализируется. Диффузные изменения поджелудочной железы (признаки хронического панкреатита).
Для определения дальнейшей тактики лечения выполнена эндосонография панкреатобилиарной зоны. Визуализирована замазкообразная желчь в общем желчном протоке (рисунок).
Вероятно, именно замазкообразная желчь в терминальном отделе общего желчного протока стала причиной частых обострений хронического билиарнозависимого панкреатита.
Для уменьшения литогенности желчи больной назначили препарат УДХК Эксхол® 500 мг в делимых таблетках в дозе 750 мг/сут в три приема. Благодаря такой форме выпуска Эксхол® 500 мг можно гибко дозировать, сокращая количество принимаемых таблеток [14]. При выборе препаратов УДХК это очень важно. Не менее значимый фактор – экономическая составляющая. Выбор препарата в рассматриваемом случае был обусловлен доступностью длительного курсового лечения.
С целью купирования болевого синдрома, устранения спазма и улучшения пассажа желчи в кишку был назначен Спарекс® по 200 мг в два приема перед едой. Через три месяца лечения отмечалась положительная динамика в виде полного купирования болевого синдрома, нормализации биохимических показателей. Наблюдение за больной в последующие шесть месяцев показало отсутствие рецидивов билиарнозависимого панкреатита.
По данным Н.А. Агафоновой и соавт. [14], российский препарат мебеверина Спарекс® не только купирует боль, но и улучшает реологические свойства желчи при ЖКБ.
Оценка безопасности и переносимости мебеверина проводилась в исследованиях, включивших свыше 3500 больных [13]. Во всех исследованиях отмечалась хорошая переносимость препарата без развития побочных эффектов, в том числе при увеличении дозы. Мебеверин не вызывает гематологических и биохимических изменений, не оказывает типичных антихолинергических эффектов, в связи с чем может назначаться пациентам с гипертрофией предстательной железы и глаукомой [13], что актуально для пожилых больных.
Таким образом, несмотря на проведенную папиллосфинктеротомию, отток желчи был нарушен, что в свою очередь провоцировало обострения хронического панкреатита. Данных о формировании стриктур не получено. В связи с этим хирургическое вмешательство было нецелесообразным. Ситуация была разрешена путем применения препарата УДХК (Эксхол®) и селективного миотропного спазмолитика (Спарекс®).
Источник

