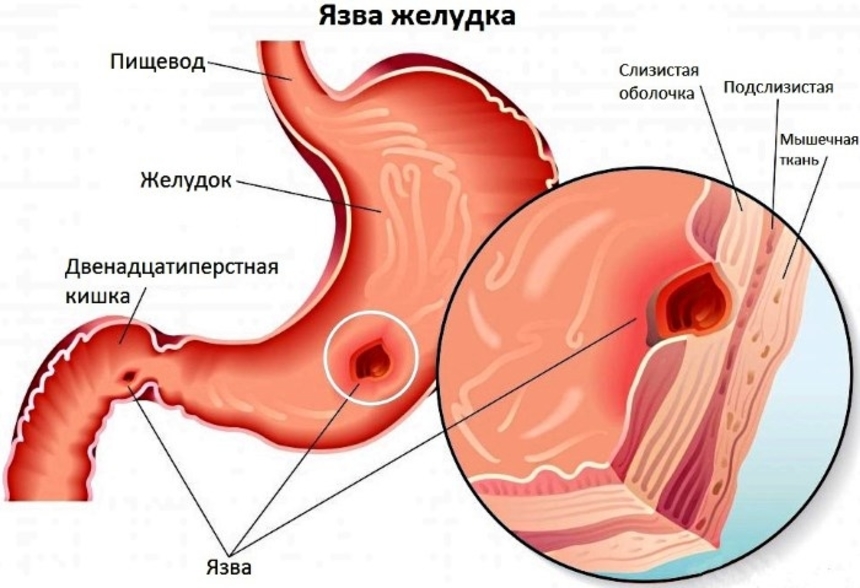
Бактериофаги от язвы желудка
Изобретение относится к области медицинской вирусологии и микробиологии. Предложен новый штамм бактериофага Helicobacter pylori №МЦКМ F-07. Штамм, обладающий литической активностью в отношении бактерий Helicobacter pylori. Предложен также способ получения противогастритного и противоязвенного средства на основе нового штамма бактериофага. Способ предусматривает получение очищенной суспензии бактериофага Helicobacter pylori №МЦКМ F-07 с литической активностью 109 БОЕ/мл и добавление в нее раствора 1% хинозола. Кроме того, в данное средство можно дополнительно вводить сорбит и желатозу, а полученную смесь замораживают и лиофилизируют. Предложенное изобретение позволяет получать высокоэффективное противоязвенное и противогастритное средство, которое может быть использовано в медицине. 2 н. и 1 з.п. ф-лы, 1 табл.
Изобретение относится к медицинской вирусологии и микробиологии, а именно к выявлению нового специфического штамма бактериофага для получения противогастритного и противоязвенного средства.
Известна роль бактерий Helicobacter pylori в патогенезе поражений желудка и двенадцатиперсной кишки. При исследованиях, проведенных у пациентов с острыми гастритами или обострениями хронической патологии, выявлено большое число бактерий, локализующихся в участках воспаления, обычно в антральной части. Проникая через слой слизи, Helicobacter pylori прикрепляются к эпителиальным клеткам (чаще в области межклеточных ходов), проникают в крипты и железы слизистой оболочки. Активность бактерий приводит к разрушению слизистого слоя и обусловливает контакт желудочного сока со стенкой органа. Антигены микроорганизмов стимулируют миграцию нейтрофилов и способствуют развитию острого воспаления. Локализация Helicobacter pylori в области межклеточных ходов обусловлена хемотаксисом к местам выхода мочевины и гемина, образующихся из разрушающегося гемоглобина эритроцитов в микроциркуляторном русле. Под действием бактериальной уреазы мочевина превращается в аммиак, повреждающий слизистую оболочку желудка и двенадцатиперсной кишки.
Известны штамм бактериофага Bacteriophagum salmonellae, обладающий противосальмонелезной активностью (Патент РФ №2080384, МПК С 12 N 7/00, опубл. 27.05.97); штамм бактериофага Enterobacter aerogenes для диагностики, профилактики и лечения инфекции, вызываемой Enterobacter aerogenes (Авторское свидетельство СССР №1685998, МПК С 12 N 7/00, опубл. 23.10.91); штамм бактериофага Pseudomonas aeruginosa ГНЦ ПМ №02, используемый при изготовлении поливалентного препарата против синегнойной палочки (Патент РФ №2113476, МПК С 12 N 7/ 00, опубл. 20.06.98).
Однако вышеуказанные штаммы бактериофагов не обладают литической активностью в отношении бактерий Helicobacter pylori.
Штаммов бактериофагов Helicobacter pylori, используемых для получения противогастритного и противоязвенного средства, в настоящее время не известно (объект изобретения на штамм прототипа не имеет).
Известно, что для лечения гастритов или язвенных болезней, обусловленных деятельностью Helicobacter pylori, используют такие антибиотики, как метронидазол и фуразолидон, или амоксиклав, цефокситин и эритромицин. или тетрациклин (М.Д.Машковский. Лекарственные средства. — М.: Медицина, 1987, часть 2, — с.157, 183, 246, 293).
Однако применение препаратов-антибиотиков сопряжено с различными побочными эффектами (Белобородова Н.В., Богданов М.Б. и Черненькая Т.В. Алгоритмы антибиотикотерапии. Руководство для врачей. — М., 1999, с.17):
— появление резистентных (антибиотикоустойчивых) бактерий Helicobacter pylori при длительном применении антибиотиков;
— развитие дисбактериозов, усугубляющих гастрит и язвенную болезнь желудка и двенадцатиперсной кишки.
Наиболее близким аналогом (прототипом) является способ получения жидкой и сухой препаративной формы «Стрептофагин» на основе бактериофага, включающий получение очищенной суспензии фага Streptococcus bovis путем стерилизующей фильтрации с последующей фасовкой жидкого препарата и его герметизацией. Для получения сухой формы к суспензии добавляют сульфат аммония и пищевые сорбенты с последующей лиофильной сушкой препарата (Патент РФ №2059723, МПК С 12 N 7/00, опубл. 10.05.96).
Однако вышеуказанные препараты на основе бактериофага Streptococcus bovis не обладают литической активностью в отношении бактерий Helicobacter pylori.
Техническим результатом предлагаемого изобретения является штамм бактериофага Helicobacter pylori, обладающий литической активностью в отношении патогенных бактерий Helicobacter pylori, а также способ получения противогастритной и противоязвенной препаративной жидкой и сухой формы на его основе, обеспечивающей лечение гастрита и язвы желудка без применения антибиотикотерапии.
Указанный технический результат достигается получением штамма бактериофага Helicobacter pylori (авторское название НР-7Ф-Х).
Указанный технический результат достигается также разработкой способа получения противогастритного и противоязвенного средства, включающего получение очищенной суспензии бактериофага и введение в него дополнительных компонентов, согласно изобретению в качестве очищенной суспензии бактериофага используют суспензию бактериофага Helicobacter pylori (НР-7Ф-Х) №МЦКМ F-07 с литической активностью не менее 109 БОЕ/мл, а в качестве дополнительных компонентов используют раствор хинозола при следующем конечном содержании ингредиентов полученного средства, мас.%:
очищенная суспензия бактериофага Helicobacter
pylori с литической активностью 109 БОЕ/мл 10,0-20,0
1%-ный раствор хинозола 0,5-1,0
вода ocтальное до 100%
Кроме того, в средство дополнительно вводят сорбит и желатозу, полученную смесь замораживают со скоростью 0,1-3,0°С в минуту до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда, а процесс сушки средства производят лиофилизацией при следующем конечном содержании компонентов в сухом средстве, мас.%:
сорбит 20,0-25,0
желатоза 20,0-25,0
хинозол 0,03-0-06
сухая масса бактерифага остальное до 100%
Желатоза — частично гидролизованная желатина (белок), обладающая амфотерными свойствами, которая является стабилизатором для биологически активных компонентов биопрепарата. Желатоза разрешена к использованию в пищевой и фармацевтической промышленности.
Сорбит обладают стабилизирующими и защитными свойствами в процессе сушки и хранения биологически активных веществ.
Хинозол — мелкокристаллический порошок лимонно-желтого цвета является антибиотиком, обладающим антибактериальной и противогрибковой активностью, малотоксичен.
Штамм бактериофага Helicobacter pylori (авторское название НР-7Ф-X) выделен из спонтанно лизировавшейся культуры Helicobacter pylori в процессе наработки ее биомассы на Колумбиа агаре при ее биохимических исследованиях. Штамм фага НР-7Ф-Х депонирован в Коллекции Межрегионального центра коррекции микроценоза человека (г.Новосибирск) под номером №МЦКМ F-07.
Проведена селекция штамма в течение 27 пассажей в присутствии 1,0 мг/мл хинозола, который можно использовать в качестве бактериостатика при получении препаративной формы.
Химический состав фага НР-7Ф-Х. Для оценки типа нуклеиновой кислоты очищенную суспензию фага окрашивают акридиновым оранжевым. Характер флуоресценции образцов при ультрафиолетовом облучении свидетельствовал о том, что фаг НР-7Ф-Х содержит ДНК. Белковый состав вириона исследован на основе электрофореза в 10%-ном полиакриламидиом геле. Выявлено 7 белков с молекулярными массами (в килодальтонах): 70; 67; 59; 47; 38; 27 и 34.
Физико-химические свойства фага. Суспензия фата НР-7Ф-Х не инактивируется при температуре 60°С в течение 40 минут. Литическая активность фага не изменяется в пределах рН 5-9. Фаг устойчив к антибиотику хинозолу.
Морфология негативных колоний. Фаг НР-7Ф-Х на газоне индикаторного штамма Helicobacter pylori образует округлые с четким краем негативные колонии от 0,5 до 1,5 мм в диаметре.
Вирулентность. Из 147 исследованных культур Helicobacter pylori, полученных из биоптатов слизистой оболочки желудка и двенадцатиперсной кишки больных хроническим гастритом и язвенной болезнью, все они оказались чувствительны к данному фагу.
Скорость и степень адсорбции. При множественности инфекции, равной 0,5, и инкубации адсорбционной смеси при 39°С за 5 минут адсорбируется 97% фага.
Латентный период и урожай фага. Латентный период более 25 минут и менее 30 минут. Средний урожай фага составляет 70 фаговых частиц на одну клетку. Титр фага в нативном фаголизате варьирует в пределах 1010 БОЕ/мл.
Способ размножения. Размножается на бактериальных клетках Helicobacter pylori на твердой питательной среде Колумбиа агаре и на жидкой питательной среде.
Способ хранения. Суспензия фага (НР-7Ф-Х) хранится в жидком виде 1 год и лиофильном (сухом) виде при температуре +(2-10)°С в течение 2-х лет.
Для практического использования на базе фага (НР-7Ф-Х) созданы жидкая и сухая препаративные формы.
Пример 1. Приготовление жидкой формы препарата на основе штамма бактериофага Helicobacter pylori (НР-7Ф-Х)
Вначале берут культуру Helicobacter pylori, полученную из биоптатов слизистой оболочки желудка и двенадцатиперсной кишки больных хроническим гастритом и язвенной болезнью и производят ее посев на поверхность питательной среды, содержащей Колумбиа агар с 10%-ной сывороткой лошадиной крови и ингибиторами роста посторонней микрофлоры. Оптимальный состав газовой смеси: N2 85-87%; О2 5%; СО2 8-10% (микроаэрофильные условия). Культивирование производят в течение 4-х суток в микроаэрофильных условиях при температуре 37°С. В результате культивирования в течение 2-х суток появляются мелкие колонии размером менее 0,5 мм, гладкие, блестящие, выпуклые, прозрачные. На третьи сутки рост бактериальных клеток максимальный, колонии имеют размер 1 мм. По истечении 4-х суток колонии пересевают на новые (свежие) питательные среды или используют в качестве посевного материала для наработки бактерий Helicobacter pylori в суспензии на жидкой среде следующего состава. В 1 литре дистиллированной воды растворяют, (г): триптический гидролизат кормовых дрожжей 30,0; натрия пируват 0,2; натрия метабисульфит 0,2; железо сернокислое закисное 0,2; натрия глютамат 1,3; натрий хлористый 4,0; агар 10,0; натрий углекислый 0,15; до рН 7,2. Раствор кипятят 2-3 минуты, отфильтровывают через ватный фильтр, стерилизуют при 1 атм (121°С) в течение 20 минут и охлаждают до +37°С. В культуральную среду вносят посевную дозу Helicobacter pylori до конечной концентрации 5·107 КОЕ/мл и выращивают в микроаэрофильных условиях (состав газовой смеси: N2 85-87%; О2 5%; СО2 8-10%) при температуре 37°С до концентрации не менее 109 КОЕ/мл. После этого в биомассу бактерий вводят суспензию бактериофага Helicobacter pylori (НР-7Ф) с концентрацией фага 106 БОЕ мл и культивируют в том же режиме в течение 24 часов до полного лизиса бактериальной популяции. Суспензию центрифугируют 20 минут при 8000 об/мин и фильтруют. Концентрация фага составляет 1010 БОЕ/мл. Перед фасовкой в препарат вводят 1%-ный раствор хинозола при следующем конечном содержании ингредиентов полученного средства, мас.%:
очищенная суспензия бактериофага Нelicobacter
pylori с литической активностью 1010 БОЕ/мл 10,0-20,0
1%-ный раствор хинозола 0,5-1,0
вода остальное до 100%
Далее жидкую форму бактериофага фасуют в стерильных условиях и хранят при температуре +(2-10)°С.
Пример 2. Получение сухой формы препарата на основе жидкой формы бактериофага Helicobacter pylori (НР-7Ф-Х)
Стерильную вируссодержащую жидкость получают, как в примере 1. К стерильной вируссодержащей жидкости и со специфической активностью не менее 1010 БОЕ/мл при непрерывном перемешивании одновременно вводят сорбит (5,0 мас.%), стерильные водные растворы 25%-ной желатозы (мол. вес 3000) до конечной концентрации (5,0 мас.%). Полученный жидкий полуфабрикат препарата разливают в ампулы по 0,5 мл в каждую и замораживают при температуре -60°С в течение 18 часов. Продукт лиофильно высушивают в течение 48 часов в стерильных условиях при следующем конечном содержании компонентов в сухом средстве, мас.%:
сорбит 20,0-25,0
желатоза 20,0-25,0
хинозол 0,03-0,06
сухая масса бактерифагa ocтальное до 100%
После окончания сушки ампулы заполняют инертным газом (аргоном) и запаивают.
Ниже в таблице приведены данные по хранению жидкой и сухой препаративных форм фага Helicobacter pylori (НР-7Ф-Х) №МЦКМ F-07.
| Таблица | |||
| Данные по хранению заявляемых препаративных форм фага Н. Pylori | |||
| Показатель | Температура хранения, °С | Препаративная форма фага | |
| Жидкая, БОЕ/мл | Сухая, БОЕ/г | ||
| Лигич. активность фагов после приготовления препарата | +(4-7) | 4,5·109 | 2,5·109 |
| Литич. активность фагов после 1 года хранения | +(4-7) | 1,0·109 | 2,0·109 |
| Литич. активность фагов после 2-х летнего хранения | -(4-7) | 8,5·108 |
Из таблицы видно, что жидкая препаративная форма фага сохраняет литическую активность в течение 1 года, а сухая — в течение 2-х лет.
Исследование препарата фага на животных. В эксперименте на животных (свиньях) воспроизведен гастрит путем введения микроорганизмов Helicobacter pylori в желудок указанным животным. Лечение животных осуществлялось путем смешивания с кормом (отруби) препаративной формы фага Helicobacter pylori (НР-7Ф-Х) в дозе 1 г препарата на 1 кг корма и скармливания его животным в течение 1 недели. Вскрытие одной группы животных до лечения и другой группы после лечения показало высокую эффективность действия как жидкой, так и сухой формы заявляемого препарата.
1. Штамм бактериофага Helicobacter pylori, депонированный в коллекции Межрегионального центра коррекции микроценоза человека (МЦКМЧ) под регистрационным номером МЦКМ F-07, обладающий литической активностью в отношении бактерий Helicobacter pylori.
2. Способ получения противогастритного и противоязвенного средства, включающий получение очищенной суспензии бактериофага и введение в него дополнительных компонентов, отличающийся тем, что в качестве очищенной суспензии бактериофага используют суспензию бактериофага Helicobacter pylori №МЦКМ F-07 по п.1 с литической активностью не менее 109 БОЕ/мл, а в качестве дополнительных компонентов используют раствор хинозола при следующем конечном содержании ингредиентов полученного средства, мас.%:
Очищенная суспензия бактериофага Helicobacter
pylori с литической активностью 109 БОЕ/мл 10,0-20,0
1%-ный Раствор хинозола 0,5-1,0
Вода Остальное
3. Способ по п.2, отличающийся тем, что в средство дополнительно вводят сорбит и желатозу, полученную смесь замораживают со скоростью 0,1-3,0°С/мин до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда, а процесс сушки средства производят лиофилизацией при следующем конечном содержании компонентов в сухом средстве, мас.%:
Сорбит 20,0-25,0
Желатоза 20,0-25,0
Хинозол 0,03-0,06
Сухая масса бактериофага Остальное
Источник
БАКТЕРИОФАГИ КАК АЛЬТЕРНАТИВА АНТИБИОТИКАМ В ЛЕЧЕНИИ ИНФЕКЦИЙ
Бактериофаги — вирусы бактерий, естественные микроорганизмы, которые, размножаясь внутри бактериальной клетки, ведут к ее быстрой гибели.
Из истории открытия
В 1896 году английский бактериолог Э. Ханкин, исследуя антибактериальное действие воды индийских рек, пришел к выводу о существовании агента, проходящего через бактериальные фильтры и вызывающего лизис холерных вибрионов. Российский микробиолог Н. Ф. Гамалея в 1897 году наблюдал лизис бацилл сибирской язвы. Однако первой научной публикацией о фагах стала статья английского микробиолога Ф. Туорта, в которой он в 1915 году описал инфекционное поражение стафилококков, значительно изменявшее морфологию колоний. В 1917 году канадский бактериолог Ф. Д’Эрелль независимо от Туорта сообщил об открытии вируса, «пожирающего» бактерии — бактериофага.
Интересный факт: при нанесении бактериофага на влажные слизистые он за 20 минут очищает их от определенного вида бактерий, например от стафилококка. Так быстро не работает ни один антибиотик.
Действие бактериофагов отличается от действия антибиотиков:
- Для определенного вида бактерий существует свой определенный бактериофаг. Но стоит отметить, что не ко всем бактериям есть бактериофаги (это основной недостаток этих препаратов). Для решения вопроса, какую терапию выбрать для лечения инфекции, врач должен сначала взять материал для посева на флору с точным определением вида возбудителя и только после получения анализа на чувствительность микроорганизма к бактериофагам выбрать препарат.
- Бактериофаги не действуют на нормофлору (нормальные бактерии), поэтому лечение бактериофагами экологично и не требует коррекции нормофлоры.
- Бактериофаги не влияют на организм человека, поскольку не способны проникнуть в клетки человека. Поэтому бактериофаги не токсичны и не вызывают побочных эффектов.
- После уничтожения патогена элиминируются (самовыводятся) из организма.
- Бактериофаги просты в применении: большинство их производится в жидком виде. Доступно наружное орошение при местном применении, полоскании, в виде микроклизм при кишечных инфекциях. Но действуют бактериофаги только местно, то есть именно там, где вы их применяете при полоскании, орошении и закапывании. В отличие от антибиотиков, которые при приеме внутрь распределяются по организму и действуют во всех органах и тканях.
- Бактериофаги стимулируют местный иммунитет, так как частицы уничтоженных бактерий побуждают иммунную систему к выработке специфических антител. Из-за этого свойства бактериофаги являются препаратом выбора в лечении бактерионосительства (например, стафилококконосительства) и хронических форм бактериальных инфекций.
- Сочетаются с другими препаратами, в том числе с антибиотиками. Их совместное применение ведет к быстрому выздоровлению от бактериальной инфекции.
- По совокупности описанных свойств бактериофаги применимы как основной препарат для лечения бактериальных инфекций у беременных, детей с рождения и людей пожилого возраста, а также в тех случаях, когда имеется полирезистентность микроорганизма к антибиотикам.
В лаборатории KDL предлагается 2 варианта посевов на флору с определением чувствительности выделенной культуры микроорганизма к препаратам бактериофагов и разным наборам антибиотиков в зависимости от ситуации пациента (выбирает врач), например:
Посев на микрофлору отделяемого урогенитального тракта женщины с определением чувствительности к основному спектру антибиотиков и бактериофагам, в т.ч. Кандида
Посев на микрофлору отделяемого урогенитального тракта женщины с определением чувствительности к расширенному спектру антибиотиков и бактериофагам, в т.ч. Кандида
Какие инфекции можно лечить бактериофагами:
- кожные, ожоговые и раневые инфекции;
- инфекции ЛОР органов;
- инфекции урогенитального тракта;
- отдельные инфекции желудочно-кишечного тракта.
Возбудителями этих инфекций могут быть такие бактерии, как золотистый стафилококк, синегнойная палочка, патогенные формы кишечной палочки, сальмонеллы, стрептококки.
В Новосибирском научном центре технологии персонализированного лечения бактериофагами в большой коллекции бактериофагов есть уникальные штаммы, способные бороться с недавно появившимися и уже получившими широкое распространение возбудителями больничных инфекций, такими как грамотрицательные бактерии Acinetobacter baumanii, Stenotrophomonas maltophilia и др.
Последние годы ознаменовались широкими исследованиями бактериофагов из-за нарастающей проблемы антибиотикорезистентности микроорганизмов, которые находят всё новые применения не только в терапии и профилактике, но и в биотехнологиях. Их очевидным практическим результатом должно стать возникновение нового мощного направления персонализированной медицины, а также создание целого спектра технологий в пищевой промышленности, ветеринарии, сельском хозяйстве и в производстве современных материалов. Мы ждем, что второе столетие исследований бактериофагов принесет не меньше открытий, чем первое.
Источник